Tài liệu cung cấp thông tin về nhiễm trùng sơ sinh và những yếu tố nguy cơ nghiêm trọng đối với trẻ chưa trưởng thành hệ miễn dịch. Nó nhấn mạnh tầm quan trọng của việc nhận biết sớm các dấu hiệu nhiễm trùng và thực hiện các xét nghiệm cần thiết để chẩn đoán và điều trị kịp thời. Đồng thời, tài liệu cũng liệt kê các tác nhân gây nhiễm trùng và hướng dẫn điều trị kháng sinh phù hợp cho trẻ sơ sinh.





![235
Xét Nghiệm
Đánh giá xét nghiệm
Trước chuyển
Các xét nghiệm sau cần được làm trước khi chuyển trẻ
− công thức 4M:
Máu - Công thức máu (Công thức máu toàn phần
[CTM] với công thức bạch cầu [BC] và số lượng tiểu cầu)
Máu - Cấy máu
●● Sử dụng kỹ thuật vô trùng khi lấy máu nuôi cấy và
cho máu vào ống nuôi cấy
●● Nếu có thể, lấy tối thiểu 1 ml máu cho một ống
nuôi cấy1,19,20
●● Lưu ý: lượng máu 2-3 ml trong ống nuôi cấy vi
khuẩn ái khí giúp tăng khả năng xác định vi khuẩn
khi có ít khuẩn lạc
●● Lấy máu nuôi cấy trước khi cho kháng sinh
Máu - Glucose máu
●● Kiểm tra sớm và theo dõi sát theo chỉ định dựa vào
các yếu tố nguy cơ
Máu - Khí máu
●● Đây là xét nghiệm đặc biệt quan trọng nếu trẻ có
suy hô hấp hoặc bệnh sử sốc. Tuy nhiên, đối với
bất kỳ trẻ sơ sinh nào nghi có nhiễm khuẩn, định
lượng pH và kiềm thiếu đều có giá trị.](https://image.slidesharecdn.com/6-180422034902/75/6-p-229-to-278-lab-work-module-vietnamese-7-2048.jpg)






























![270
Chương trình S.T.A.B.L.E - Sách hướng dẫn học viên
Phần thực hành: Xét nghiệm
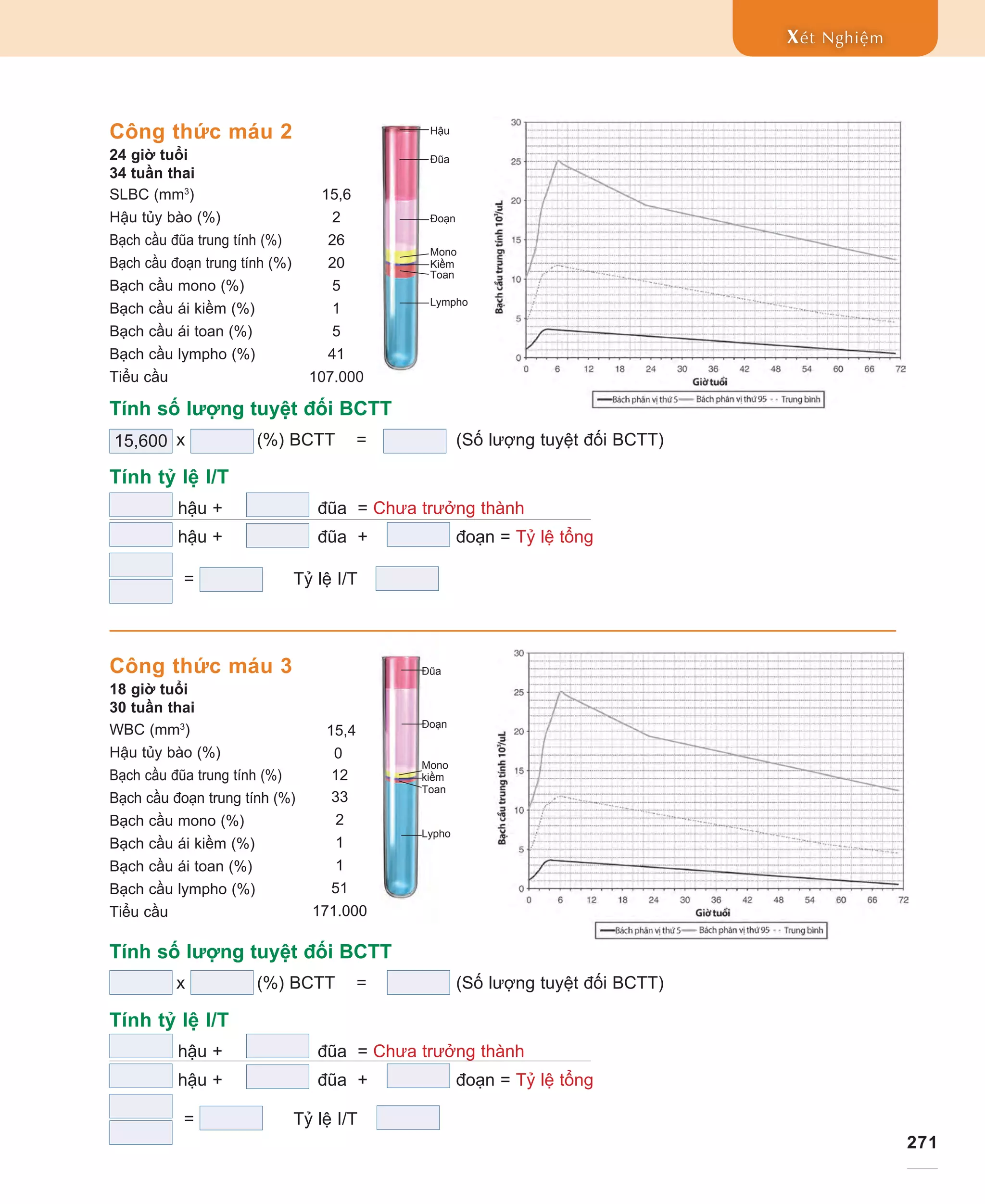
1. Với kết quả CTM sau, tính số lượng tuyệt đối BCTT và tỷ lệ I/T.
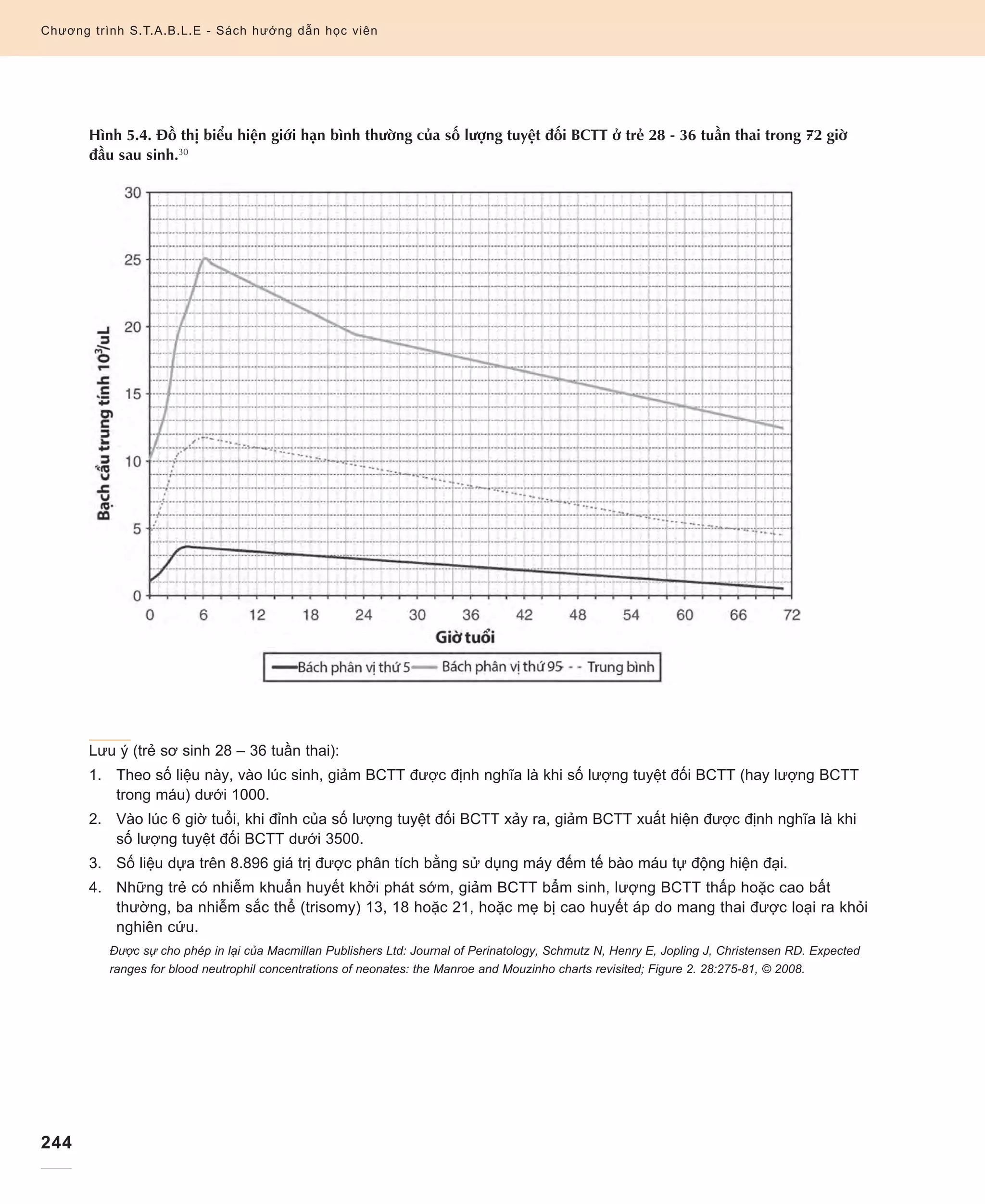
2. Chấm số lượng tuyệt đối BCTT lên biểu đồ Schmutz cho mỗi mẫu CTM.
3. Với mỗi CTM, số lượng tiểu cầu là thấp, bình thường, hay cao?
Tính số lượng tuyệt đối BCTT
SLBC (có thể ghi là SLBC x 103
/µl) nhân với [(%) (đoạn + đũa + hậu tủy bào)]
Tính tỷ lệ bạch cầu chưa trưởng thành trên tỷ lệ tổng (I/T)
(%) hậu tủy bào + đũa (chưa trưởng thành-I) chia cho (%) hậu tủy bào + đũa + đoạn (tỷ lệ tổng)
Công thức máu 1
8 giờ tuổi
39 tuần thai
SLBC (mm3
) 10,4
Hậu tủy bào (%) 0
Bạch cầu đũa trung tính (%) 14
Bạch cầu đoạn trung tính (%) 5
Bạch cầu mono (%) 6
Bạch cầu ái kiềm (%) 2
Bạch cầu ái toan (%) 3
Bạch cầu lympho (%) 70
Tiểu cầu 141.000
Tính số lượng tuyệt đối BCTT
Số lượng tuyệt đối BCTT là 1976 (Chấm lên biểu đồ phù hợp với tuổi thai và tuổi bệnh nhân)
x =
Tính tỷ lệ I/T
= 0,74 Tỷ lệ I/T là 0,74
Để tính I/T và giá trị tuyệt đối BCTT, không tính tỷ lệ bạch cầu lympho, bạch cầu mono, bạch cầu ái toan và bạch cầu
ái kiềm nhưng phải tính tất cả hậu bào và tủy bào là những tế bào chưa trưởng thành có trong báo cáo CTM.
Đũa
Đoạn
Mono
Ái kiềm
Ái toan
Lympho
14
19
10.400 197619% hoặc .19
140 hậu + đũa = Chưa trưởng thành
5140 hậu + đũa + đoạn = Tỷ lệ tổng](https://image.slidesharecdn.com/6-180422034902/75/6-p-229-to-278-lab-work-module-vietnamese-42-2048.jpg)