Recommended
PDF
เอกสารประกอบการเรียน เรื่อง อัตราการเกิดปฏิกิริยาเคมี
DOC
อัตราการเกิดปฎิกิริยาเคมี
PPT
PPT
PPTX
6-ปฏิกิริฟหดฟหกดฟหกดฟหกดฟหกดฟหกดยาเคมี-นร.pptx
PDF
แบบฝึกหัดอัตราการเกิดปฏิกิริยาเคมี
DOC
PDF
PDF
อัตราการเกิดปฏิกิริยา๘ มหิดล
PDF
PPT
อัตราการเกิดปฏิกิริยาเคมี (Rate of reaction
DOC
PDF
PDF
PPT
อัตราการเกิดปฏิกิริยาเคมี
PPT
2 กฎอัตราและอันดับของปฏิกิริยา
PDF
PDF
PPT
ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยา
DOC
PPT
PDF
บทที่ 6 อัตราการเกิดปฏิกิริยา
PDF
การเกิดปฏิกิริยาเคมี เล่ม1
PDF
DOC
DOC
PDF
ชุดกิจกรรมวิทยาศาสตร์ เรื่อง ปฏิกิริยาเคมี รายวิชาเคมีพื้นฐาน กลุ่มสาระก...
PDF
ชุดกิจกรรมวิทยาศาสตร์ เรื่อง ปฏิกิริยาเคมี รายวิชาเคมีพื้นฐาน ชั้นมัธยมศึก...
More Related Content
PDF
เอกสารประกอบการเรียน เรื่อง อัตราการเกิดปฏิกิริยาเคมี
DOC
อัตราการเกิดปฎิกิริยาเคมี
PPT
PPT
PPTX
6-ปฏิกิริฟหดฟหกดฟหกดฟหกดฟหกดฟหกดยาเคมี-นร.pptx
PDF
แบบฝึกหัดอัตราการเกิดปฏิกิริยาเคมี
DOC
PDF
Similar to 16442806.ppt
PDF
อัตราการเกิดปฏิกิริยา๘ มหิดล
PDF
PPT
อัตราการเกิดปฏิกิริยาเคมี (Rate of reaction
DOC
PDF
PDF
PPT
อัตราการเกิดปฏิกิริยาเคมี
PPT
2 กฎอัตราและอันดับของปฏิกิริยา
PDF
PDF
PPT
ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยา
DOC
PPT
PDF
บทที่ 6 อัตราการเกิดปฏิกิริยา
PDF
การเกิดปฏิกิริยาเคมี เล่ม1
PDF
DOC
DOC
PDF
ชุดกิจกรรมวิทยาศาสตร์ เรื่อง ปฏิกิริยาเคมี รายวิชาเคมีพื้นฐาน กลุ่มสาระก...
PDF
ชุดกิจกรรมวิทยาศาสตร์ เรื่อง ปฏิกิริยาเคมี รายวิชาเคมีพื้นฐาน ชั้นมัธยมศึก...
16442806.ppt 1. 2. 3. 4. คาอธิบาย: ข ถูกต้อง เพราะผลิตภัณฑ์เป็ นสารใหม่ที่เกิดขึ้นจากการทาปฏิกิริยา
ของสารเริ่มต้น
4
เลือกคาตอบที่ถูกต้องที่สุดเพียง
คาตอบเดียว
1. เราเรียกสารใหม่ที่เกิดจากการ
ทาปฏิกิริยาว่าอะไร
ก สารเริ่มต้น
ข ผลิตภัณฑ์
ค สารเร่งปฏิกิริยา
ง สารร่วมปฏิกิริยา
5. คาอธิบาย: ก ถูกต้อง เพราะจากข้อความแสดงว่า กามะถัน (S) และแก๊ส
ออกซิเจน (O2) เป็ นสารเริ่มต้น และเมื่อกามะถันและแก๊สออกซิเจนทาปฏิกิริยากัน
จะได้แก๊สซัลเฟอร ์ไดออกไซด์(SO2) เป็ นผลิตภัณฑ์ดังนั้น สมการเคมีที่เขียนได้
จึงเป็ น S + O SO
5
2. ขณะกลั่นน้ ามันดิบ กามะถันจะทา
ปฏิกิริยากับแก๊สออกซิเจน ปฏิกิริยาเคมีที่
เกิดขึ้นสามารถเขียนสมการเคมีได้ดัง
สมการเคมีใด
ก S + O2 SO2
ข SO2 + O2 SO4
ค 2SO2 + O2 2SO3
ง SO2 + H2O H2SO4
6. คาอธิบาย: ง ถูกต้อง เพราะในการเกิดปฏิกิริยาเคมี สารเริ่มต้นจะเปลี่ยนไปเป็ น
ผลิตภัณฑ์ซึ่งสารเริ่มต้นและผลิตภัณฑ์เป็ นสารต่างชนิดที่มีการสร ้างพันธะเคมี
ของอะตอมต่างกัน แต่อะตอมทั้งหมดที่เกิดเป็ นผลิตภัณฑ์นั้นได้มาจากสารเริ่มต้น
ทั้งหมดโดยไม่มีอะตอมชนิดใหม่เกิดขึ้น ดังนั้นในการดุลสมการเคมีจึงต้องทาให้
อะตอมของธาตุเดียวกันในสารเริ่มต้นเท่ากับในผลิตภัณฑ์
6
3. หลักการสาคัญในการดุลสมการเคมีคือ
อะไร
ก ทาให้จานวนสารเริ่มต้นเท่ากับผลิตภัณฑ์
ข ทาให้พลังงานของสารเริ่มต้นเท่ากับ
ผลิตภัณฑ์
ค ทาให้จานวนโมเลกุลของสารเริ่มต้นเท่ากับ
ผลิตภัณฑ์
ง ทาให้อะตอมของธาตุเดียวกันในสารเริ่มต้น
เท่ากับในผลิตภัณฑ์
7. คาอธิบาย: ง ถูกต้อง เพราะการลดอุณหภูมิทาให้อัตราการเกิดปฏิกิริยาเคมี
ลดลง และการลดความเข้มข้นของสารก็ทาให้อัตราการเกิดปฏิกิริยาเคมีลดลง
ด้วยเช่นกัน
7
4. การกระทาใดทาให้อัตราการเกิดปฏิกิริยา
เคมีมีแนวโน้มเดียวกัน
ก เพิ่มตัวเร่งปฏิกิริยา เพิ่มขนาด
ข เพิ่มอุณหภูมิ เพิ่มตัวหน่วงปฏิกิริยา
ค ลดขนาด ลดความเข้มข้นของสาร
ง ลดอุณหภูมิ ลดความเข้มข้นของสาร
8. คาอธิบาย: ก ถูกต้อง เพราะการเคี้ยวอาหารเป็ นการทาให้อาหารมีขนาดเล็กลง
ซึ่งเป็ นการเพิ่มพื้นที่ผิวให้กับอาหาร เนื่องจากสารที่มีมวลเท่ากัน สารขนาดเล็กจะ
มีพื้นที่ผิวมากกว่าสารขนาดใหญ่ เมื่ออาหารมีพื้นที่ผิว
มากขึ้น เอนไซม์จึงสัมผัสกับอาหารมากขึ้น อาหารจึงถูกย่อยได้เร็วขึ้น 8
5. การเคี้ยวอาหารให้ละเอียดขึ้นช่วยให้
ปฏิกิริยาการย่อยอาหาร
เกิดเร็วขึ้นเพราะอะไร
ก เพิ่มพื้นที่ผิวของอาหาร
ข เพิ่มอุณหภูมิของอาหาร
ค เพิ่มความเข้มข้นของอาหาร
ง เพิ่มตัวเร่งปฏิกิริยาในการย่อยอาหาร
9. คาอธิบาย: ค ถูกต้อง เพราะ HCl เป็ นสารเริ่มต้น ซึ่งการเพิ่มความเข้มข้นของ
สารเริ่มต้นทาให้โอกาสในการทาปฏิกิริยากันของสารเริ่มต้นสูงขึ้น อัตราการ
เกิดปฏิกิริยาเคมีจึงเพิ่มขึ้น
9
6. Mg(s) + 2HCl(aq) MgCl2(aq) +
H2(g)
วิธีใดที่ทาให้อัตราการเกิดปฏิกิริยาของ
สมการเคมีนี้เพิ่มขึ้น
ก เพิ่มขนาดของ Mg
ข เพิ่มปริมาตรของ H2
ค เพิ่มความเข้มข้นของ HCl
ง เพิ่มความเข้มข้นของ MgCl2
10. คาอธิบาย: ค ถูกต้อง เพราะเมื่อให้ความเข้มข้นของสารอื่นคงที่และปรับความ
เข้มข้นเฉพาะสารที่ต้องการศึกษาทาให้ผลการทดลองเปลี่ยนแปลงไปตามการ
เปลี่ยนแปลงความเข้มข้นของสารที่ต้องการศึกษาเท่านั้น ดังนั้นเราจึงสามารถ
สังเกตได้ว่าสารที่ต้องการศึกษามีผลต่ออัตราการเกิดปฏิกิริยาเคมีหรือไม่
1
0
7. ถ้านักเรียนต้องการศึกษาว่าความเข้มข้นของ
สารเริ่มต้นชนิดใดมีผลต่อ
อัตราการเกิดปฏิกิริยาเคมี นักเรียนจะออกแบบ
การทดลองอย่างไร
ก กาหนดความเข้มข้นของสารทั้งหมดให้เท่ากัน
ข กาหนดความเข้มข้นของสารทั้งหมดให้ไม่เท่ากัน
ค ปรับความเข้มข้นของสารที่ต้องการศึกษาโดยให้
สารอื่นมีความเข้มข้น
คงที่
ง ให้ความเข้มข้นของสารที่ต้องการศึกษาคงที่และ
ปรับความเข้มข้นของ
่
11. คาอธิบาย: ข ถูกต้อง เพราะการต้มน้าเป็ นการทาให้น้าเดือด ซึ่งเป็ นเพียงการ
เปลี่ยนสถานะจากของเหลวเป็ นแก๊สหรือไอน้า ไม่ใช่การเกิดปฏิกิริยาเคมี
1
1
8. กิจกรรมใดต่อไปนี้ไม่เกี่ยวข้องกับการ
ประยุกต์ใช้ความรู ้ในเรื่อง
อัตราการเกิดปฏิกิริยาเคมี
ก การปรุงอาหารที่อุณหภูมิต่า
ข การเพิ่มอุณหภูมิในการต้มน้าให้เดือด
ค การเก็บอาหารหรือยาบางชนิดในตู้เย็น
ง การใช้แท่งแก้วคนสารตลอดเวลาระหว่างการ
เกิดปฏิกิริยาเคมี
12. คาอธิบาย: ข ถูกต้อง เพราะการสุกของผลไม้เป็ นการเกิดปฏิกิริยาเคมีชนิดหนึ่ง
การปิดฝาภาชนะทาให้อากาศในภาชนะไม่เกิดการถ่ายเทและอุณหภูมิสูงขึ้น
อัตราการเกิดปฏิกิริยาเคมีจึงเพิ่มขึ้น ผลไม้จึงสุกเร็วขึ้น 1
2
9. ถ้านักเรียนต้องการให้ผลไม้ที่เก็บมา
สุกเร็วขึ้นควรเก็บผลไม้ไว้ในลักษณะ
ใด
ก ในตู้เย็น
ข ในภาชนะที่มีฝาปิด
ค ในที่ที่ไม่มีแสงสว่าง
ง ในที่ที่มีอากาศถ่ายเทสะดวก
13. คาอธิบาย: ง ถูกต้อง เพราะการควบคุมอัตราการเกิดปฏิกิริยาเคมีได้ ไม่ได้แสดง
ว่าทาให้ปฏิกิริยาเคมีทุกชนิดมีประโยชน์ต่อมนุษย์และสิ่งมีชีวิตอื่น เช่น การควบคุม
อัตราปฏิกิริยาการเกิดการเน่าเสียของอาหารเป็ นเพียงการชะลอการเน่าเสียของ
อาหาร ไม่ได้ทาให้ปฏิกิริยาการเน่าเสียของอาหารเกิดประโยชน์ต่อมนุษย์และ
1
3
10. ข้อความใดต่อไปนี้กล่าวไม่ถูกต้อง
ก ปฏิกิริยาเคมีบางชนิดก่อให้เกิดมลพิษต่อ
สภาพแวดล้อม
ข ปฏิกิริยาเคมีที่เกิดขึ้นมีทั้งที่เกิดขึ้นอย่าง
รวดเร็วหรือนานเป็นเดือน
ค แบตเตอรี่ชนิดต่าง ๆ มีสารที่เป็นอันตรายต่อ
มนุษย์ถ้าการใช้และ
การจัดเก็บไม่ถูกวิธี
ง ปฏิกิริยาเคมีทุกชนิดมีประโยชน์ต่อมนุษย์และ
สิ่งมีชีวิตอื่น ๆ
ถ้ารู้จักควบคุมอัตราการเกิดปฏิกิริยา
14. 15. 16. 17. 18. 1. สมการเคมีคืออะไร
สมการเคมี คือ การเขียนแสดงความสัมพันธ์
ระหว่างสารเริ่มต้นกับผลิตภัณฑ์ที่มีส่วนเกี่ยวข้อง
กับปฏิกิริยาเคมีที่เกิดขึ้น
ลูกศร โดยลูกศรจะชี้ไปทางผลิตภัณฑ์เสมอ
ตอบคาถาม
ต่อไปนี้
2. สัญลักษณ์ใดทาให้เราทราบว่าสารใดเป็น
ผลิตภัณฑ์ในสมการเคมี ลักษณะใด
1
8
1. สมการและการ
เกิดปฏิกิริยาเคมี
19. 20. 21. 22. 23. 24. ของแข็ง
l (liquid) แทน
ของเหลว
g (gas) แทน
แก๊ส
aq (aqueous)
แทน
สารละลายที่มีน้า
เป็ นตัว
ทาละลาย
แทน ปฏิกิริยา
เคมีเกิด
ทิศทางเดียว
แทน ปฏิกิริยา
2
4
สมการเคมี
(chemical
equation)
ความสัมพันธ์ระหว่างสาร
เริ่มต้นกับผลิตภัณฑ์ในการ
เกิดปฏิกิริยาเคมี
เขียน
แสดง
ตัวอักษร
ภาษาอังกฤษ
ในวงเล็บเพื่อแสดง
สถานะของสาร
เขียนกากับ
ด้วย
1.1 ความหมายและการเขียนสมการเคมี
1. สมการและการ
เกิดปฏิกิริยาเคมี
25. 26. 27. 28. 29. 30. 31. 32. 3
2
ค้นหา
คาตอบ
3. การเปลี่ยนแปลงของสารที่เกิดขึ้นเป็ นการเปลี่ยนแปลงทางเคมี
หรือไม่ เพราะอะไร
เป็ นการเปลี่ยนแปลงทางเคมี เพราะได้สารผลิตภัณฑ์ที่มี
สมบัติแตกต่างจากสารเริ่มต้น คือ สารที่ละลายในน้าและ
สารที่มีสถานะเป็ นแก๊ส
1. เมื่อใส่แผ่นสังกะสีลงในสารละลายกรดไฮโดรคลอริก ผลที่
เกิดขึ้นคืออะไร
แผ่นสังกะสีมีขนาดเล็กลงและเกิดฟองแก๊ส
2. สารที่เกิดขึ้นมีสมบัติเหมือนสารเริ่มต้นหรือไม่ เพราะอะไร
ไม่เหมือน สารที่เกิดขึ้นจะเป็ นสารประกอบของเกลือ และสารที่
อยู่ในสถานะแก๊ส
1.1 ความหมายและการเขียนสมการเคมี
1. สมการและการ
เกิดปฏิกิริยาเคมี
33. 3
3
4. สารเริ่มต้นและผลิตภัณฑ์ที่ได้จากปฏิกิริยานี้คือ
สารใด
สารเริ่มต้น คือ โลหะสังกะสี (Zn) กับสารละลายกรดไฮโดร
คลอริก (HCl) ส่วนผลิตภัณฑ์ ที่เกิดขึ้น คือ
สารประกอบเกลือของซิงก์(II) คลอไรด์(ZnCl2) กับแก๊ส
ไฮโดรเจน (H2)
5. ปฏิกิริยาเคมีระหว่างสังกะสีกับสารละลายกรดไฮโดรคลอริก
เขียนสมการเคมีได้ในลักษณะใด
Zn(s) + 2HCl(aq) ZnCl2
(aq)+ H2(g)
ค้นหา
คาตอบ
1.1 ความหมายและการเขียนสมการเคมี
1. สมการและการ
เกิดปฏิกิริยาเคมี
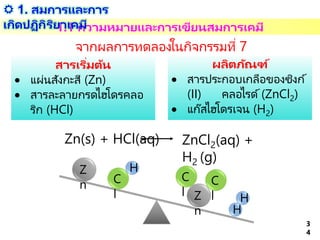
34. 3
4
สารเริ่มต้น
แผ่นสังกะสี (Zn)
สารละลายกรดไฮโดรคลอ
ริก (HCl)
ผลิตภัณฑ์
สารประกอบเกลือของซิงก์
(II) คลอไรด์(ZnCl2)
แก๊สไฮโดรเจน (H2)
Zn(s) + HCl(aq) ZnCl2(aq) +
H2 (g)
Z
n C
l
H
Z
n
C
l
C
l H
H
1.1 ความหมายและการเขียนสมการเคมี
จากผลการทดลองในกิจกรรมที่ 7
1. สมการและการ
เกิดปฏิกิริยาเคมี
35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 2.ใส่น้ากลั่นจานวน 50 ลูกบาศก์เซนติเมตร ลงในบีกเกอร ์ขนาด
100 ลูกบาศก์เซนติเมตร
3.ใส่สารละลายกรดไฮโดรคลอริกเข้มข้น 0.2 โมลต่อลิตร ลงใน
กระบอกตวงจนเต็มแล้ว
ปิดปากกระบอกตวงด้วยจุกคอร ์ก คว่ากระบอกตวงลงในบีกเกอร ์
โดยให้ปากกระบอกตวง
4
6
น้า
กลั่น
สารละลายกรดไฮโดร
คลอริก
2. อัตราการ
เกิดปฏิกิริยาเคมี
47. 48. 49. 50. 51. 52. 53. 54. 55. 56. 57. 58. Editor's Notes #2 ครูอธิบายเนื้อหาในหน่วยการเรียนรู้ที่ 2 ปฏิกิริยาเคมี ตามผังมโนทัศน์สาระการเรียนรู้ ดังนี้
หน่วยการเรียนรู้ที่ 2 ปฏิกิริยาเคมี
แบ่งเป็น 4 เรื่อง (ครูคลิกเพื่อแสดงทีละเรื่อง) ดังนี้
1. สมการและการเกิดปฏิกิริยาเคมี (แผนที่ 6)
2. อัตราการเกิดปฏิกิริยาเคมี (แผนที่ 6)
3. ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยาเคมี (แผนที่ 7–9)
4. ปฏิกิริยาเคมีที่มีผลต่อสิ่งมีชีวิตและสิ่งแวดล้อม (แผนที่ 10)
แบ่งเป็น 5 แผนการจัดการเรียนรู้ 7 ชั่วโมง
แผนการจัดการเรียนรู้ที่ 6 สมการเคมีและอัตราการเกิดปฏิกิริยาเคมี 2 ชั่วโมง
แผนการจัดการเรียนรู้ที่ 7 ความเข้มข้นและพื้นที่ผิวของสารเริ่มต้น
ที่มีผลต่ออัตราการเกิดปฏิกิริยาเคมี 2 ชั่วโมง
แผนการจัดการเรียนรู้ที่ 8 อุณหภูมิที่มีผลต่ออัตราการเกิดปฏิกิริยาเคมี 1 ชั่วโมง
แผนการจัดการเรียนรู้ที่ 9 ตัวเร่งปฏิกิริยาและธรรมชาติของสาร
ที่มีผลต่ออัตราการเกิดปฏิกิริยาเคมี 1 ชั่วโมง
แผนการจัดการเรียนรู้ที่ 10 ปฏิกิริยาเคมีที่มีผลต่อสิ่งมีชีวิตและสิ่งแวดล้อม 1 ชั่วโมง
#3 แผนการจัดการเรียนรู้ที่ 6 ชั่วโมงที่ 9–10 สมการเคมีและอัตราการเกิดปฏิกิริยาเคมี
#4 ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด (การทำแบบทดสอบใน PowerPoint อาจใช้เวลามาก ครูควร print ให้นักเรียนทำแล้วจึงใช้ PowerPoint ตรวจคำตอบ)
#5 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 1
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 1
เฉลย
ก ไม่ถูกต้อง เพราะสารเริ่มต้นเป็นสารที่ทำปฏิกิริยากันจนเกิดเป็นสารใหม่หรือผลิตภัณฑ์
ข ถูกต้อง เพราะผลิตภัณฑ์เป็นสารใหม่ที่เกิดขึ้นจากการทำปฏิกิริยาของสารเริ่มต้น
ค ไม่ถูกต้อง เพราะสารเร่งปฏิกิริยาเป็นสารที่ช่วยให้สารเริ่มต้นเปลี่ยนเป็นผลิตภัณฑ์ได้เร็วขึ้น
ง ไม่ถูกต้อง เพราะสารร่วมปฏิกิริยาเป็นสารทั้งหมดที่เข้าร่วมในปฏิกิริยาเคมีแล้วได้สารใหม่
หรือผลิตภัณฑ์
#6 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 2
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 2
เฉลย
ก ถูกต้อง เพราะจากข้อความแสดงว่า กำมะถัน (S) และแก๊สออกซิเจน (O2) เป็นสารเริ่มต้น
และเมื่อกำมะถันและแก๊สออกซิเจนทำปฏิกิริยากันจะได้แก๊สซัลเฟอร์ไดออกไซด์ (SO2)
เป็นผลิตภัณฑ์ ดังนั้น สมการเคมีที่เขียนได้จึงเป็น S + O2 SO2
ข ไม่ถูกต้อง เพราะ SO2 คือ แก๊สซัลเฟอร์ไดออกไซด์ ซึ่งไม่ใช่สารเริ่มต้นในปฏิกิริยาเคมีนี้
ค ไม่ถูกต้อง เพราะ SO2 คือ แก๊สซัลเฟอร์ไดออกไซด์ ซึ่งไม่ใช่สารเริ่มต้นในปฏิกิริยาเคมีนี้
ง ไม่ถูกต้อง เพราะ SO2 คือ แก๊สซัลเฟอร์ไดออกไซด์ และ H2O คือ น้ำ ซึ่งสารทั้ง 2 ชนิด
ไม่ใช่สารเริ่มต้นในปฏิกิริยาเคมีนี้
#7 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 3
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 3
เฉลย
ก ไม่ถูกต้อง เพราะในการเกิดปฏิกิริยาเคมี สารเริ่มต้นและผลิตภัณฑ์อาจมีจำนวนไม่เท่ากัน
แต่จำนวนอะตอมของธาตุเดียวกันในสารเริ่มต้นต้องเท่ากับในผลิตภัณฑ์
ข ไม่ถูกต้อง เพราะในการเกิดปฏิกิริยาเคมี สารเริ่มต้นและผลิตภัณฑ์ไม่จำเป็นต้องมีพลังงาน เท่ากัน
ค ไม่ถูกต้อง เพราะผลิตภัณฑ์ที่เกิดขึ้นไม่จำเป็นต้องมีจำนวนโมเลกุลเท่ากับสารเริ่มต้น
แต่จำนวนอะตอมของธาตุชนิดเดียวกันในสารเริ่มต้นต้องเท่ากับในผลิตภัณฑ์
ง ถูกต้อง เพราะในการเกิดปฏิกิริยาเคมี สารเริ่มต้นจะเปลี่ยนไปเป็นผลิตภัณฑ์ซึ่งสารเริ่มต้นและ
ผลิตภัณฑ์เป็นสารต่างชนิดที่มีการสร้างพันธะเคมีของอะตอมต่างกัน แต่อะตอมทั้งหมดที่เกิด เป็นผลิตภัณฑ์นั้นได้มาจากสารเริ่มต้นทั้งหมดโดยไม่มีอะตอมชนิดใหม่เกิดขึ้น ดังนั้นในการ
ดุลสมการเคมีจึงต้องทำให้อะตอมของธาตุเดียวกันในสารเริ่มต้นเท่ากับในผลิตภัณฑ์
#8 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 4
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 4
เฉลย
ก ไม่ถูกต้อง เพราะการเพิ่มตัวเร่งปฏิกิริยาทำให้อัตราการเกิดปฏิกิริยาเคมีเพิ่มขึ้น
แต่การเพิ่มขนาดเป็นการลดพื้นที่ผิวทำให้อัตราการเกิดปฏิกิริยาเคมีลดลง
ข ไม่ถูกต้อง เพราะการเพิ่มอุณหภูมิทำให้อัตราการเกิดปฏิกิริยาเคมีเพิ่มขึ้น
แต่การเพิ่มตัวหน่วงปฏิกิริยาทำให้อัตราการเกิดปฏิกิริยาเคมีลดลง
ค ไม่ถูกต้อง เพราะการลดขนาดเป็นการเพิ่มพื้นที่ผิวทำให้อัตราการเกิดปฏิกิริยาเคมีเพิ่มขึ้น
แต่การลดความเข้มข้นของสารทำให้อัตราการเกิดปฏิกิริยาเคมีลดลง
ง ถูกต้อง เพราะการลดอุณหภูมิทำให้อัตราการเกิดปฏิกิริยาเคมีลดลง และการลดความเข้มข้น
ของสารก็ทำให้อัตราการเกิดปฏิกิริยาเคมีลดลงด้วยเช่นกัน
#9 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 5
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 5
เฉลย
ก ถูกต้อง เพราะการเคี้ยวอาหารเป็นการทำให้อาหารมีขนาดเล็กลง ซึ่งเป็นการเพิ่มพื้นที่ผิว
ให้กับอาหาร เนื่องจากสารที่มีมวลเท่ากัน สารขนาดเล็กจะมีพื้นที่ผิวมากกว่าสารขนาดใหญ่
เมื่ออาหารมีพื้นที่ผิวมากขึ้น เอนไซม์จึงสัมผัสกับอาหารมากขึ้น อาหารจึงถูกย่อยได้เร็วขึ้น
ข ไม่ถูกต้อง เพราะการเคี้ยวอาหารให้ละเอียดไม่ได้ทำให้อุณหภูมิของอาหารเพิ่มขึ้น
ค ไม่ถูกต้อง เพราะการเคี้ยวอาหารให้ละเอียดไม่ได้ทำให้ความเข้มข้นของอาหารเพิ่มขึ้น
ง ไม่ถูกต้อง เพราะการเคี้ยวอาหารให้ละเอียดไม่ได้ทำให้ตัวเร่งปฏิกิริยาในการย่อยอาหารเพิ่มขึ้น
#10 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 6
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 6
เฉลย
ก ไม่ถูกต้อง เพราะการเพิ่มขนาดของ Mg เป็นการลดพื้นที่ผิวของสารเริ่มต้นทำให้โอกาส
ในการทำปฏิกิริยากันของสารเริ่มต้นลดลง อัตราการเกิดปฏิกิริยาเคมีจึงลดลง
ข ไม่ถูกต้อง เพราะ H2 เป็นผลิตภัณฑ์ การเพิ่มปริมาตรของ H2 จึงไม่มีผลต่ออัตรา
การเกิดปฏิกิริยาเคมี
ค ถูกต้อง เพราะ HCl เป็นสารเริ่มต้น ซึ่งการเพิ่มความเข้มข้นของสารเริ่มต้นทำให้โอกาส
ในการทำปฏิกิริยากันของสารเริ่มต้นสูงขึ้น อัตราการเกิดปฏิกิริยาเคมีจึงเพิ่มขึ้น
ง ไม่ถูกต้อง เพราะ MgCl2 เป็นผลิตภัณฑ์ การเพิ่มความเข้มข้นของ MgCl2 จึงไม่มีผลต่ออัตรา
การเกิดปฏิกิริยาเคมี
#11 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 7
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 7
เฉลย
ก ไม่ถูกต้อง เพราะถ้าสารทั้งหมดมีความเข้มข้นเท่ากันจะไม่สามารถเปรียบเทียบได้ว่าสารใด
มีผลต่ออัตราการเกิดปฏิกิริยาเคมี
ข ไม่ถูกต้อง เพราะการกำหนดความเข้มข้นของสารทั้งหมดให้ไม่เท่ากัน เมื่ออัตราการเกิด
ปฏิกิริยาเปลี่ยนไปจะทำให้ไม่สามารถบอกได้ว่าสารใดเป็นตัวที่มีผลต่ออัตราการเกิด
ปฏิกิริยาเคมี
ค ถูกต้อง เพราะเมื่อให้ความเข้มข้นของสารอื่นคงที่และปรับความเข้มข้นเฉพาะสารที่ต้องการ
ศึกษา ทำให้ผลการทดลองเปลี่ยนแปลงไปตามการเปลี่ยนแปลงความเข้มข้นของสาร
ที่ต้องการศึกษาเท่านั้น ดังนั้นเราจึงสามารถสังเกตได้ว่าสารที่ต้องการศึกษามีผลต่ออัตรา
การเกิดปฏิกิริยาเคมีหรือไม่
ง ไม่ถูกต้อง เพราะเมื่อความเข้มข้นของสารที่เราต้องการศึกษาคงที่ ในการทำการทดลองทุกครั้ง
ผลของสารที่ต้องการศึกษาต่ออัตราการเกิดปฏิกิริยาจะเหมือนเดิม เราจึงสังเกตไม่ได้ว่าสาร
ที่ต้องการศึกษามีผลต่ออัตราการเกิดปฏิกิริยาเคมีหรือไม่
#12 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 8
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 8
เฉลย
ก ไม่ถูกต้อง เพราะการสุกของอาหารทำให้โครงสร้างของอาหารเปลี่ยนไป การใช้อุณหภูมิต่ำ
ในการปรุงอาหารเป็นการลดอัตราการเกิดปฏิกิริยาเคมี ทำให้อาหารสุกช้าและสุกอย่างทั่วถึง
จึงเป็นการประยุกต์ใช้ความรู้ในเรื่องอัตราการเกิดปฏิกิริยาเคมี
ข ถูกต้อง เพราะการต้มน้ำเป็นการทำให้น้ำเดือดซึ่งเป็นเพียงการเปลี่ยนสถานะจากของเหลว
เป็นแก๊สหรือไอน้ำ ไม่ใช่การเกิดปฏิกิริยาเคมี
ค ไม่ถูกต้อง เพราะอาหารเมื่อวางไว้ในที่อุณหภูมิสูงอาจทำให้อาหารบูด หรือยาบางชนิดเมื่อเก็บ
ที่อุณหภูมิสูง ยาจะเกิดปฏิกิริยาเคมีกลายเป็นสารอีกชนิดหนึ่ง ทำให้ยาเสื่อมคุณภาพ
ดังนั้นการเก็บอาหารหรือยาบางชนิดในตู้เย็นจึงเป็นการลดอัตราการเกิดปฏิกิริยาเคมี
จึงเป็นการประยุกต์ใช้ความรู้ในเรื่องอัตราการเกิดปฏิกิริยาเคมี
ง ไม่ถูกต้อง เพราะการใช้แท่งแก้วคนสารเป็นการช่วยให้สารเคลื่อนที่มากขึ้น สารจึงมีโอกาส
เข้าทำปฏิกิริยากันมากขึ้นเป็นการเพิ่มอัตราการเกิดปฏิกิริยาเคมี จึงเป็นการประยุกต์ใช้
ความรู้ในเรื่องอัตราการเกิดปฏิกิริยาเคมี
#13 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 9
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 9
เฉลย
ก ไม่ถูกต้อง เพราะความเย็นจะทำให้อัตราการเกิดปฏิกิริยาเคมีลดลง ซึ่งเป็นการทำให้ผลไม้
สุกช้า
ข ถูกต้อง เพราะการสุกของผลไม้เป็นการเกิดปฏิกิริยาเคมีชนิดหนึ่ง การปิดฝาภาชนะทำให้
อากาศในภาชนะไม่เกิดการถ่ายเทและอุณหภูมิสูงขึ้น อัตราการเกิดปฏิกิริยาเคมีจึงเพิ่มขึ้น
ผลไม้จึงสุกเร็ว
ค ไม่ถูกต้อง เพราะการที่ไม่มีแสงสว่าง อุณหภูมิของสิ่งแวดล้อมจะไม่สูง ทำให้อัตราการเกิด
ปฏิกิริยาเคมีไม่เพิ่มขึ้น ผลไม้จึงสุกช้า
ง ไม่ถูกต้อง เพราะการที่อากาศถ่ายเทสะดวก อุณหภูมิของสิ่งแวดล้อมจะไม่สูง ทำให้อัตรา
การเกิดปฏิกิริยาเคมีไม่เพิ่มขึ้น ผลไม้จึงสุกช้า
#14 1) ครูให้นักเรียนทำแบบทดสอบก่อนเรียน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ข้อ 10
2) ครูคลิกเพื่อเฉลยคำตอบข้อ 10
เฉลย
ก ไม่ถูกต้อง เพราะปฏิกิริยาเคมีบางชนิดก่อให้เกิดมลพิษต่อสภาพแวดล้อม เช่น การเผาไหม้
เชื้อเพลิงที่ไม่สมบูรณ์เกิดแก๊สคาร์บอนมอนอกไซด์ที่เป็นแก๊สพิษต่อร่างกาย
ข ไม่ถูกต้อง เพราะปฏิกิริยาเคมีบางชนิดเกิดขึ้นอย่างรวดเร็ว เช่น การเผาไหม้กระดาษ
ส่วนปฏิกิริยาเคมีบางชนิดเกิดนานเป็นเดือน เช่น ปฏิกิริยาการเกิดสนิม
ค ไม่ถูกต้อง เพราะแบตเตอรี่มีโลหะหนักเป็นส่วนประกอบซึ่งเป็นอันตรายต่อมนุษย์ ซึ่งถ้าใช้
และจัดเก็บไม่ถูกวิธี โลหะหนักอาจเกิดการรั่วไหลและเป็นพิษต่อสิ่งแวดล้อมได้
ง ถูกต้อง เพราะการควบคุมอัตราการเกิดปฏิกิริยาเคมีได้ ไม่ได้แสดงว่าทำให้ปฏิกิริยาเคมี
ทุกชนิดมีประโยชน์ต่อมนุษย์และสิ่งมีชีวิตอื่น เช่น การควบคุมอัตราปฏิกิริยาการเกิดการ
เน่าเสียของอาหารเป็นเพียงการชะลอการเน่าเสียของอาหาร ไม่ได้ทำให้ปฏิกิริยาการเน่าเสีย
ของอาหารเกิดประโยชน์ต่อมนุษย์และสิ่งมีชีวิตอื่น ๆ
#15 แผนการจัดการเรียนรู้ที่ 6 สมการเคมีและอัตราการเกิดปฏิกิริยาเคมี 2 ชั่วโมง
สาระการเรียนรู้
1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
2. อัตราการเกิดปฏิกิริยาเคมี
จากหนังสือเรียน รายวิชาพื้นฐาน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
#16 1) ครูกระตุ้นเกี่ยวกับประสบการณ์เดิมของนักเรียน โดยให้นักเรียนดูรูปแล้วถามคำถามว่า
นักเรียนสามารถระบุได้หรือไม่ว่า สารในรูปใดเกิดการเปลี่ยนแปลงทางกายภาพและสาร
ในรูปใดเกิดการเปลี่ยนแปลงทางเคมี เพราะอะไร
2) ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม เพื่อเชื่อมโยงความรู้ใหม่จากบทเรียนกับ
ประสบการณ์เดิมของนักเรียน เมื่อนักเรียนอภิปรายคำถามเสร็จแล้ว ครูสรุปแนวคำตอบ
ร่วมกันกับนักเรียน (แนวคำตอบ รูปที่ 1 เกิดการเปลี่ยนแปลงทางกายภาพ เพราะน้ำแข็งเกิด
การหลอมเหลวซึ่งเป็นการเปลี่ยนแปลงสถานะเท่านั้น รูปที่ 2 เกิดการเปลี่ยนแปลงทางเคมี
เพราะกระดาษเกิดการเผาไหม้กลายเป็นขี้เถ้าซึ่งเกิดการเปลี่ยนแปลงโครงสร้างทางเคมี)
ครูใช้เวลาในการนำเข้าสู่บทเรียนประมาณ 5 นาที (หรือให้ครูใช้เวลาตามความเหมาะสม)
#17 1. สมการและการเกิดปฏิกิริยาเคมี
1) ครูตรวจสอบว่านักเรียนปฏิบัติตามภาระงานก่อนเรียนที่ได้รับมอบหมายไปหรือไม่ โดยครู
ถามคำถามกับนักเรียนว่า การอ่านและค้นคว้าล่วงหน้าเกี่ยวกับสมการและการเกิดปฏิกิริยาเคมี
นักเรียนได้อะไรบ้าง
2) ครูและนักเรียนร่วมกันตอบคำถามและแสดงความคิดเห็น
ครูใช้เวลาในการจัดกิจกรรมการเรียนรู้ประมาณ 55 นาที (หรือให้ครูใช้เวลาตามความเหมาะสม)
#18 1. สมการและการเกิดปฏิกิริยาเคมี
1) ครูแบ่งกลุ่มนักเรียนแล้วเปิดโอกาสให้นักเรียนในกลุ่มนำเสนอข้อมูลเกี่ยวกับสมการและ
การเกิดปฏิกิริยาเคมี ที่ครูมอบหมายให้ไปเรียนรู้ล่วงหน้าให้เพื่อน ๆ ในกลุ่มฟัง โดยครูให้
นักเรียนร่วมกันอภิปรายซักถามจนคาดว่าสมาชิกทุกคนในกลุ่มมีความรู้ความเข้าใจที่ตรงกัน
2) ครูคลิกแสดงข้อความเพื่อให้แต่ละกลุ่มส่งตัวแทนมานำเสนอข้อมูลหน้าห้องเรียน
#19 1. สมการและการเกิดปฏิกิริยาเคมี
ครูคลิกเพื่อแสดงคำถามเกี่ยวกับภาระงานก่อนเรียนแล้วให้นักเรียนช่วยกันตอบ (ครูคลิก
คำถามและเฉลยทีละข้อ)
#20 1. สมการและการเกิดปฏิกิริยาเคมี
1) ครูถามคำถามนักเรียนว่า นักเรียนตั้งคำถามที่สงสัยไว้ว่าอย่างไร เพื่อเปิดโอกาสให้นักเรียน
ตั้งประเด็นคำถามที่สงสัยจากการทำภาระงานก่อนเรียน ซึ่งครูให้นักเรียนเตรียมมาล่วงหน้า
และให้นักเรียนช่วยกันตอบคำถามและแสดงความคิดเห็น
2) เมื่อนักเรียนตอบคำถามและแสดงความคิดเห็นเสร็จแล้ว ครูคลิกเพื่อสรุปภาระงานก่อนเรียน
โดยถามนักเรียนว่า นักเรียนได้เรียนรู้อะไรบ้าง
3) ครูและนักเรียนร่วมกันสรุปเกี่ยวกับภาระงานก่อนเรียนเพื่อให้ได้ข้อสรุปว่า สมการเคมีใช้
แสดงความสัมพันธ์ระหว่างสารเริ่มต้นกับผลิตภัณฑ์ที่มีส่วนเกี่ยวข้องกับปฏิกิริยาเคมี
4) ครูคลิกเพื่อแสดงข้อสรุปของภาระงานก่อนเรียน #21 1. สมการและการเกิดปฏิกิริยาเคมี
1 ครูให้นักเรียนดูรูปแล้วคลิกตามลำดับ จากนั้นถามคำถามกับนักเรียนว่า
– ฟันเฟืองในรูปทำจากวัสดุชนิดใด
– ฟันเฟืองในรูปเกิดการเปลี่ยนแปลงในลักษณะใด
– ฟันเฟืองในรูปเกิดการเปลี่ยนแปลงเพราะอะไร
2) ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม ซึ่งคำตอบอาจมีได้หลากหลายคำตอบ
โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง และให้นักเรียนร่วมกันหาคำตอบจากบทเรียนเรื่อง สมการ
และการเกิดปฏิกิริยาเคมีในเฟรมถัดไป
#22 1. สมการและการเกิดปฏิกิริยาเคมี
ครูคลิกตามลำดับ เพื่อตอบคำถามจากเฟรมที่ผ่านมา ดังนี้
– ฟันเฟืองในรูปทำจากวัสดุชนิดใด (คำตอบ ฟันเฟืองทำจากเหล็ก)
– ฟันเฟืองในรูปเกิดการเปลี่ยนแปลงในลักษณะใด (คำตอบ ฟันเฟืองเกิดสนิมขึ้นที่ผิว)
– ฟันเฟืองในรูปเกิดการเปลี่ยนแปลงเพราะอะไร (คำตอบ ฟันเฟืองเกิดสนิม เพราะเหล็ก
ทำปฏิกิริยากับความชื้นในอากาศ) #23 1. สมการและการเกิดปฏิกิริยาเคมี
1) ครูคลิกตามลำดับ เพื่ออธิบายความหมายของปฏิกิริยาเคมี สารเริ่มต้นหรือ
ตัวทำปฏิกิริยา (reactant) และผลิตภัณฑ์ (product) จากการเกิดสนิมของฟันเฟือง
2) ครูอธิบายเกี่ยวกับสารเริ่มต้นและผลิตภัณฑ์เพิ่มเติม ในหนังสือเรียน รายวิชาพื้นฐาน
วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
#24 1. สมการและการเกิดปฏิกิริยาเคมี
1) ครูคลิกเพื่อแสดงว่า นักวิทยาศาสตร์ใช้สัญลักษณ์ของธาตุจากตารางธาตุเขียนเป็น
สูตรเคมีเพื่อให้นักวิทยาศาสตร์ทุกคนเข้าใจตรงกันว่ากำลังกล่าวถึงสารชนิดใด
2) ครูคลิกแล้วถามคำถามกับนักเรียนว่า นักเรียนคิดว่า นักวิทยาศาสตร์ใช้สิ่งใดเพื่อบอก
การเกิดปฏิกิริยาเคมีให้เข้าใจตรงกันได้
3) ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม ซึ่งคำตอบอาจมีได้หลากหลายคำตอบ
โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง และให้นักเรียนร่วมกันหาคำตอบจากบทเรียนเรื่อง
ความหมายและการเขียนสมการเคมีในเฟรมถัดไป
#25 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
ครูคลิกตามลำดับเพื่ออธิบายความหมายของสมการเคมี (chemical equation) ในหนังสือเรียน รายวิชาพื้นฐาน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
#26 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
ครูคลิกตามลำดับเพื่ออธิบายการเขียนสมการเคมีของการเกิดสนิมของฟันเฟืองที่ทำจากเหล็ก
โดยครูยังไม่ดุลสมการเคมีให้นักเรียนดู ซึ่งครูจะนำสมการเคมีนี้ไปดุลสมการเคมีเมื่อทราบหลัก
ในการเขียนสมการเคมีแล้ว #27 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูคลิกตามลำดับแล้วถามนักเรียนว่า เมื่อมีปฏิกิริยาเคมีเกิดขึ้น นักเรียนจะเขียนสมการเคมี
เพื่อแสดงการเกิดปฏิกิริยาเคมีนั้นได้อย่างไร ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับ
คำถาม ซึ่งคำตอบอาจมีได้หลากหลายคำตอบ โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง จากนั้น
ครูให้นักเรียนแบ่งกลุ่มแล้วร่วมกันค้นหาคำตอบ เพื่อเชื่อมโยงเข้าสู่การปฏิบัติกิจกรรม
2) นักเรียนปฏิบัติกิจกรรมที่ 7 สังเกตการเกิดปฏิกิริยาเคมี ในแบบฝึกทักษะ รายวิชาพื้นฐาน
วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด #28 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูให้นักเรียนร่วมกันตั้งคำถามเพื่อกำหนดปัญหาก่อนปฏิบัติกิจกรรม โดยครูช่วยสรุป
การตั้งคำถามของนักเรียน แล้วร่วมกันกำหนดเป็นปัญหาที่สอดคล้องกับการปฏิบัติกิจกรรม
2) ครูคลิกเพื่อแสดงปัญหาของกิจกรรม
3) ครูคลิกเพื่อแสดงอุปกรณ์ที่ใช้ในการปฏิบัติกิจกรรม #29 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูคลิกเพื่อแสดงขั้นตอนในการปฏิบัติกิจกรรม
2) ครูอธิบายวิธีการเตรียมสารก่อนการปฏิบัติกิจกรรม คือ สารละลายกรดไฮโดรคลอริก
(ครูดูวิธีการเตรียมสารจากหมายเหตุ ในแบบฝึกทักษะ รายวิชาพื้นฐาน วิทยาศาสตร์
สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด)
3) ครูแนะนำให้นักเรียนใช้กระดาษทรายขัดแผ่นสังกะสีก่อนปฏิบัติกิจกรรม
4) ครูเตือนให้นักเรียนระวังการใช้สารละลายกรดไฮโดรคลอริก เนื่องจากกรดสามารถทำลาย
เนื้อเยื่อผิวหนังได้
#30 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูคลิกเพื่อแสดงขั้นตอนในการปฏิบัติกิจกรรม
2) ครูแนะนำให้นักเรียนจุ่มปากหลอดทดลองให้อยู่ใต้ผิวน้ำในบีกเกอร์
3) ครูคอยแนะนำช่วยเหลือนักเรียนขณะปฏิบัติกิจกรรม โดยครูเดินดูรอบ ๆ ห้องเรียนและเปิด
โอกาสให้นักเรียนทุกคนซักถามเมื่อมีปัญหา
#31 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) เมื่อปฏิบัติกิจกรรมเสร็จ ครูให้นักเรียนแต่ละกลุ่มนำเสนอผลการปฏิบัติกิจกรรมหน้าชั้นเรียน
2) ครูคลิกเพื่อแสดงตารางบันทึกผล
3) ครูคลิกเพื่อแสดงแนวคำตอบของการปฏิบัติกิจกรรม
#32 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) นักเรียนและครูร่วมกันสรุปผลจากการปฏิบัติกิจกรรม
2) ครูคลิกเพื่อแสดงสรุปผลของกิจกรรม #33 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูและนักเรียนร่วมกันอภิปรายซักถามและแสดงความคิดเห็นผลจากการปฏิบัติกิจกรรม
โดยใช้แนวคำถามจากกรอบค้นหาคำตอบท้ายกิจกรรม ในหนังสือเรียน รายวิชาพื้นฐาน
วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
2) ครูคลิกเพื่อแสดงคำถามให้นักเรียนช่วยกันตอบ (ครูคลิกคำถามและเฉลยทีละข้อ)
#34 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
ครูคลิกเพื่อแสดงคำถามให้นักเรียนช่วยกันตอบ (ครูคลิกคำถามและเฉลยทีละข้อ)
#35 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูคลิกตามลำดับ เพื่อแสดงสารเริ่มต้นและผลิตภัณฑ์จากกิจกรรมที่ 7
2) ครูคลิกเพื่อแสดงสมการเคมีที่เขียนได้จากปฏิกิริยาเคมีในกิจกรรมที่ 7
3) ครูคลิกเพื่อแสดงว่า ถ้านำสูตรเคมีของสารเริ่มต้นและผลิตภัณฑ์มาเขียนสมการเคมี
จำนวนธาตุแต่ละชนิดของสารเริ่มต้นและผลิตภัณฑ์นั้นจะไม่สมดุลกัน #36 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูถามคำถามนักเรียนว่า นักเรียนจะทำให้จำนวนธาตุแต่ละชนิดของสารเริ่มต้นและผลิตภัณฑ์
ในสมการเคมีสมดุลกันได้ด้วยวิธีใด
2) ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม ซึ่งคำตอบอาจมีได้หลากหลายคำตอบ
โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง
3) ครูคลิกแสดงรูปและอธิบายว่า ถ้าเพิ่มจำนวนกรดไฮโดรคลอริกของสารเริ่มต้น 1 โมเลกุล
จะทำให้จำนวนธาตุแต่ละชนิดของสารเริ่มต้นและผลิตภัณฑ์ในสมการเคมีสมดุลกัน
4) ครูคลิกแสดงสมการเคมีที่ดุลสมการเคมีแล้ว โดยการเติมตัวเลข 2 ลงหน้าสูตรเคมีของ HCl
#37 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
ครูคลิกตามลำดับเพื่อแสดงหลักในการเขียนสมการเคมี ในหนังสือเรียน รายวิชาพื้นฐาน
วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
#38 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูอธิบายการเขียนสมการเคมีและการดุลสมการเคมีของปฏิกิริยาเคมี “เมื่อเหล็กทำปฏิกิริยา
กับความชื้นในอากาศ จะเกิดสนิมและแก๊สไฮโดรเจน”
2) ครูคลิกแสดงสูตรเคมีของสารที่เกี่ยวข้องในปฏิกิริยาเคมี และการเขียนสมการเคมี โดยเขียน
สารเริ่มต้นด้านซ้าย ผลิตภัณฑ์ด้านขวา และมีลูกศรคั่นกลาง ตามลำดับ
3) ครูคลิกเพื่อแสดงรูปแล้วอธิบายว่า จำนวนอะตอมของธาตุในสารเริ่มต้นและผลิตภัณฑ์
ไม่สมดุลกัน
4) ครูคลิกแสดงการดุลสมการเคมี ตามลำดับ โดยดุลสมการเคมีตามหลักในการเขียนสมการเคมี
คือ ดุลจำนวนอะตอมของธาตุที่มีจำนวนมากก่อน แล้วจึงดุลโมเลกุลของน้ำและธาตุอิสระ
ทีหลัง ดังนั้นสมการเคมีนี้จึงต้องทำจำนวนอะตอมของ Fe ให้เท่ากันก่อน โดยเพิ่มอะตอม
ของ Fe อีก 2 อะตอมทางด้านสารเริ่มต้นให้เป็น 3 อะตอมเท่ากับอะตอมของ Fe ในผลิตภัณฑ์
5) ครูคลิกแสดงการเพิ่มเลข 3 หน้า Fe ในสมการเคมี
#39 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูคลิกแสดงการดุลสมการเคมีตามลำดับ โดยการทำจำนวนอะตอมของ O ในสารเริ่มต้นให้
เท่ากับผลิตภัณฑ์ โดยเพิ่มโมเลกุลของ H2O อีก 3 โมเลกุลเพื่อทำให้สารเริ่มต้นและผลิตภัณฑ์
มีอะตอมของ O เท่ากัน คือ 4 อะตอม
2) ครูแสดงการเพิ่มเลข 4 หน้า H2O ในสมการเคมี #40 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูคลิกแสดงการดุลสมการเคมีตามลำดับ โดยการทำจำนวนอะตอมของ H ในสารเริ่มต้นให้
เท่ากับผลิตภัณฑ์ โดยเพิ่มโมเลกุลของ H2 ในผลิตภัณฑ์อีก 3 โมเลกุล เพื่อทำให้สารเริ่มต้น
และผลิตภัณฑ์มีอะตอมของ H เท่ากัน คือ 8 อะตอม
2) ครูแสดงการเพิ่มเลข 4 หน้า H2 ในสมการเคมี
3) ครูสรุปว่าเมื่อทำการดุลสมการเคมีแล้ว จำนวนอะตอมของธาตุชนิดเดียวกันในสารเริ่มต้นและ
ผลิตภัณฑ์ต้องเท่ากันเสมอ
#41 1. สมการและการเกิดปฏิกิริยาเคมี
1.1 ความหมายและการเขียนสมการเคมี
1) ครูแบ่งกลุ่มนักเรียนเป็น 4 กลุ่ม เพื่อเล่นเกม โดยให้แต่ละกลุ่มแข่งกันดุลสมการเคมีต่อไปนี้
ให้ถูกต้อง กลุ่มใดตอบได้ถูกต้องมากกว่าเป็นฝ่ายชนะ
2) ครูคลิกเฉลยทีละข้อ
(1) 3H2(g) + N2(aq) 2NH3(g)
(2) 2Na(s) + 2H2O(l) 2NaOH(aq) + H2(g)
(3) CaC2(s) +2H2O(l) Ca(OH)2(s) + C2H2(g)
#42 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูกระตุ้นนักเรียนโดยถามคำถามกับนักเรียนว่า เมื่อมีปฏิกิริยาเคมีเกิดขึ้น นักเรียนจะทราบได้
อย่างไรว่า ปฏิกิริยาเคมีที่เกิดขึ้นนั้นเกิดช้าหรือเร็ว
2) ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม ซึ่งคำตอบอาจมีได้หลากหลายคำตอบ
โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง และให้นักเรียนร่วมกันหาคำตอบจากบทเรียนเรื่องอัตรา
การเกิดปฏิกิริยาเคมีในเฟรมถัดไป
#43 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูคลิกแสดงกราฟตามลำดับเพื่ออธิบายความสัมพันธ์ระหว่างปริมาณสารเริ่มต้นและผลิตภัณฑ์
กับเวลาเมื่อเกิดปฏิกิริยาเคมี
2) ครูคลิกเพื่อสรุปว่าการที่ปริมาตรของสารเริ่มต้นและผลิตภัณฑ์มีความสัมพันธ์กับเวลา
จึงนำมาใช้บอกได้ว่าปฏิกิริยาเคมีที่เกิดขึ้นนั้นเกิดช้าหรือเร็วได้
#44 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูคลิกแสดงความสัมพันธ์ของอัตราการเกิดปฏิกิริยาเคมี (rate of reaction) ตามลำดับ
พร้อมกับอธิบายอัตราการเกิดปฏิกิริยาเคมีในหนังสือเรียน รายวิชาพื้นฐาน วิทยาศาสตร์
สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
2) ครูคลิกถามนักเรียนว่าการหาอัตราการเกิดปฏิกิริยาเคมีของสารในปฏิกิริยาเคมีทำได้
อย่างไร ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม ซึ่งคำตอบอาจมีได้หลากหลาย
คำตอบ โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง จากนั้นครูให้นักเรียนแบ่งกลุ่มแล้วร่วมกันค้นหา
คำตอบ เพื่อเชื่อมโยงเข้าสู่การปฏิบัติกิจกรรม
3) นักเรียนปฏิบัติกิจกรรมที่ 8 สังเกตอัตราการเกิดปฏิกิริยาเคมีของลวดแมกนีเซียมกับกรด
ไฮโดรคลอริกในแบบฝึกทักษะ รายวิชาพื้นฐาน วิทยาศาสตร์ สารและสมบัติของสาร ชั้น
ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
#45 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูให้นักเรียนร่วมกันตั้งคำถามเพื่อกำหนดปัญหาก่อนปฏิบัติกิจกรรม โดยครูช่วยสรุป
การตั้งคำถามของนักเรียน แล้วร่วมกันกำหนดเป็นปัญหาที่สอดคล้องกับการปฏิบัติกิจกรรม
2) ครูคลิกเพื่อแสดงปัญหาของกิจกรรม
3) ครูคลิกเพื่อแสดงอุปกรณ์ที่ใช้ในการปฏิบัติกิจกรรม #46 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูคลิกเพื่อแสดงขั้นตอนในการปฏิบัติกิจกรรม
2) ครูอธิบายวิธีการเตรียมสารก่อนการปฏิบัติกิจกรรม ซึ่งประกอบด้วยสารต่าง ๆ ดังนี้
– ลวดแมกนีเซียม
– สารละลายกรดไฮโดรคลอริก
(ครูดูวิธีการเตรียมสารจากหมายเหตุ ในแบบฝึกทักษะ รายวิชาพื้นฐาน วิทยาศาสตร์
สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด)
3) ครูแนะนำให้นักเรียนบากด้านข้างของจุกคอร์กให้ไม่เล็กหรือกว้างเกินไป เพื่อให้ของเหลว
ไหลออกมาได้ในอัตราเร็วที่พอเหมาะ
#47 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูคลิกเพื่อแสดงขั้นตอนในการปฏิบัติกิจกรรม
2) ครูเตือนให้นักเรียนระวังการใช้สารละลายกรดไฮโดรคลอริก เนื่องจากกรดสามารถทำลาย
เนื้อเยื่อผิวหนังได้
3) ครูคอยแนะนำช่วยเหลือนักเรียนขณะปฏิบัติกิจกรรม โดยครูเดินดูรอบ ๆ ห้องเรียนและเปิด
โอกาสให้นักเรียนทุกคนซักถามเมื่อมีปัญหา
#48 2. อัตราการเกิดปฏิกิริยาเคมี
1) เมื่อปฏิบัติกิจกรรมเสร็จ ครูให้นักเรียนแต่ละกลุ่มนำเสนอผลการปฏิบัติกิจกรรมหน้าชั้นเรียน
2) ครูคลิกเพื่อแสดงตารางบันทึกผล
3) ครูคลิกเพื่อแสดงแนวคำตอบของการปฏิบัติกิจกรรม
#49 2. อัตราการเกิดปฏิกิริยาเคมี
1) นักเรียนและครูร่วมกันสรุปผลจากการปฏิบัติกิจกรรม
2) ครูคลิกเพื่อแสดงสรุปผลของกิจกรรม #50 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูและนักเรียนร่วมกันอภิปรายซักถามและแสดงความคิดเห็นผลจากการปฏิบัติกิจกรรม
โดยใช้แนวคำถามจากกรอบค้นหาคำตอบท้ายกิจกรรม ในหนังสือเรียน รายวิชาพื้นฐาน
วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
2) ครูคลิกเพื่อแสดงคำถามให้นักเรียนช่วยกันตอบ (ครูคลิกคำถามและเฉลยทีละข้อ)
#51 2. อัตราการเกิดปฏิกิริยาเคมี
ครูคลิกเพื่อแสดงคำถามให้นักเรียนช่วยกันตอบ (ครูคลิกคำถามและเฉลยทีละข้อ)
#52 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูคลิกตามลำดับ เพื่อแสดงความสัมพันธ์ระหว่าง ปริมาตรของแก๊สไฮโดรเจนที่เกิดขึ้น
กับเวลาที่ใช้ ในการปฏิบัติกิจกรรมที่ 8 พร้อมกับอธิบายการเปลี่ยนแปลงของสารที่เกิดขึ้น
ในปฏิกิริยาเคมี ในหนังสือเรียน รายวิชาพื้นฐาน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6
ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
2) ครูคลิกแสดงสมการอัตราการเกิดปฏิกิริยาเคมีจากการปฏิบัติกิจกรรมที่ 8 #53 2. อัตราการเกิดปฏิกิริยาเคมี
1) ครูขยายความรู้เกี่ยวกับอัตราการเกิดปฏิกิริยาเคมี โดยคลิกตามลำดับ แล้วถามคำถามกับ
นักเรียนว่า
– เพราะเหตุใดจึงเลือกบันทึกปริมาตรของแก๊สไฮโดรเจนที่เพิ่มขึ้น
– ปริมาตรแก๊สที่เพิ่มขึ้นบอกอัตราการเกิดปฏิกิริยาเคมีได้เพราะอะไร
– อัตราการเกิดปฏิกิริยาเคมีไม่คงที่เพราะอะไร
2) ครูให้นักเรียนร่วมกันอภิปรายคำตอบเกี่ยวกับคำถาม ซึ่งคำตอบอาจมีได้หลากหลายคำตอบ
โดยครูยังไม่เฉลยคำตอบที่ถูกต้อง และให้นักเรียนร่วมกันหาคำตอบในเฟรมถัดไป
#54 2. อัตราการเกิดปฏิกิริยาเคมี
ครูคลิกตามลำดับเพื่อสรุป ดังนี้
– การเลือกสารที่เหมาะสม เพื่อนำมาบอกอัตราการเกิดปฏิกิริยาเคมีจะต้องเลือกสารที่สามารถ
วัดการเปลี่ยนแปลงปริมาณได้อย่างต่อเนื่อง
– การบอกอัตราการเกิดปฏิกิริยาเคมี ต้องบอกโดยใช้สารที่เกี่ยวข้องกับการเกิดปฏิกิริยาเคมี
เท่านั้น
– อัตราการเกิดปฏิกิริยาเคมี มักมีค่าสูงเมื่อเริ่มต้นปฏิกิริยาเคมีและมีค่าลดลงในช่วงท้าย
ปฏิกิริยาเคมี #55 1) ครูถามนักเรียนว่าในหัวข้อนี้มีจุดใดบ้างที่ยังไม่เข้าใจ ถ้ามีครูช่วยอธิบายเพิ่มเติม
2) ครูทดสอบความเข้าใจของนักเรียนโดยการให้ตอบคำถาม
3) ครูคลิกเพื่อแสดงคำถาม ให้นักเรียนช่วยกันตอบ (ครูคลิกคำถามและคำตอบทีละข้อ) #56 1) ครูทดสอบความเข้าใจของนักเรียนโดยการให้ตอบคำถามจากกิจกรรมประจำหน่วย ใน
หนังสือเรียน รายวิชาพื้นฐาน วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท
สำนักพิมพ์วัฒนาพานิช จำกัด
2) ครูคลิกเพื่อแสดงคำถามในหัวข้อทบทวนคำศัพท์และหลักการทางวิทยาศาสตร์ แล้วให้
นักเรียนช่วยกันตอบ (ครูคลิกคำถามและเฉลยทีละข้อ)
#57 ครูคลิกเพื่อแสดงคำถามในหัวข้อทบทวนคำศัพท์และหลักการทางวิทยาศาสตร์ แล้วให้
นักเรียนช่วยกันตอบ (ครูคลิกคำถามและเฉลยตามลำดับ)
#58 ครูคลิกเพื่อแสดงคำถามในหัวข้อทักษะสร้างเสริมความเข้าใจที่คงทนแล้วให้นักเรียน
ช่วยกันตอบ (ครูคลิกคำถามและเฉลยทีละข้อ) #59 1) ครูและนักเรียนร่วมกันสรุปเกี่ยวกับสมการเคมีและอัตราการเกิดปฏิกิริยาเคมีโดยครูให้นักเรียน
แต่ละคนเขียนสรุปเป็นแผนที่ความคิดหรือผังมโนทัศน์
2) ครูคลิกเพื่อแสดงตัวอย่างแผนที่ความคิดหรือผังมโนทัศน์ทีละขั้น พร้อมสรุปทีละประเด็น
3) ครูอาจให้นักเรียนปฏิบัติกิจกรรมเสนอแนะเพิ่มเติม โดยดูจากคู่มือครู แผนการจัดการเรียนรู้
วิทยาศาสตร์ สารและสมบัติของสาร ม. 4–6 ของบริษัท สำนักพิมพ์วัฒนาพานิช จำกัด
ครูใช้เวลาในการสรุปประมาณ 5 นาที (หรือให้ครูใช้เวลาตามความเหมาะสม)