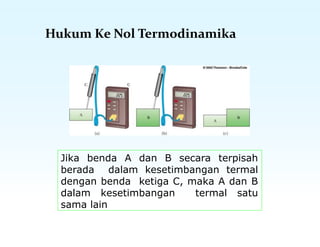
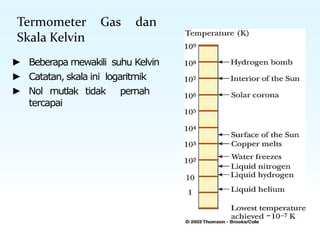
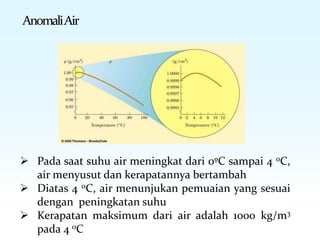
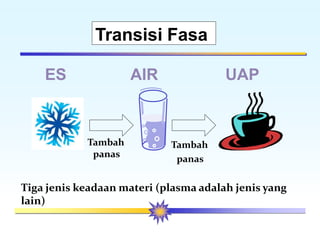
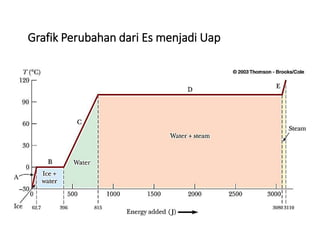
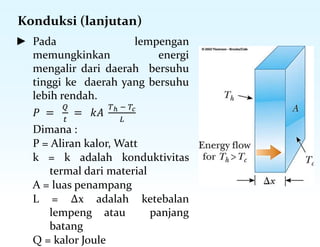
Dokumen ini membahas tentang konsep suhu, skala temperatur, pemuaian termal, dan kalor dalam termodinamika. Terdapat penjelasan tentang berbagai skala suhu seperti Celsius, Kelvin, dan Fahrenheit, serta fenomena pemuaian zat. Selain itu, juga dijelaskan tentang mekanisme transfer panas melalui konduksi, konveksi, dan radiasi, serta kalor jenis dan kalor laten pada perubahan fase zat.