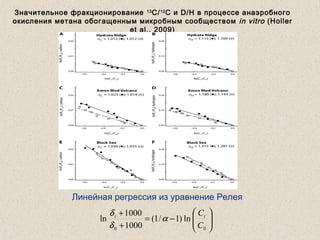
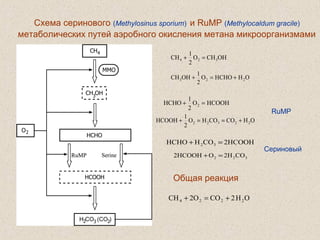
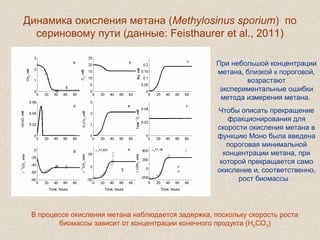
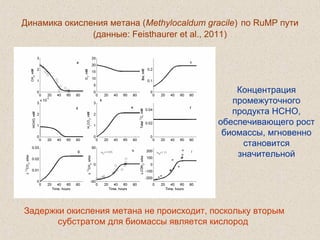
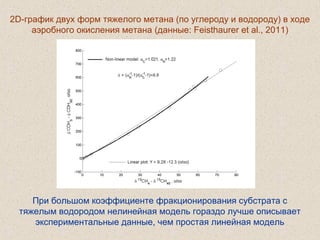
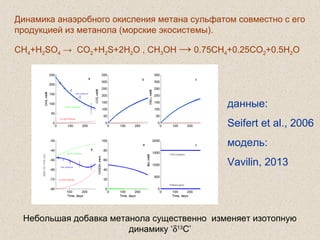
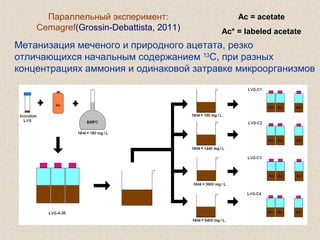
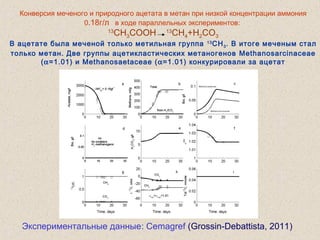
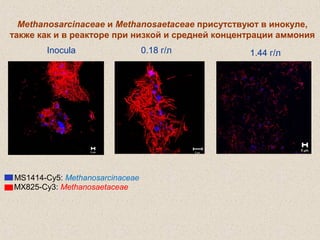
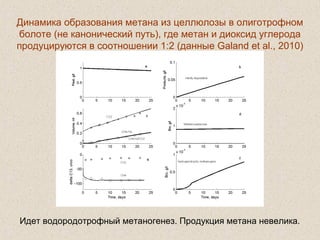
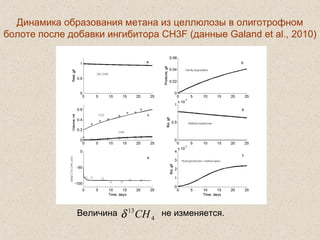
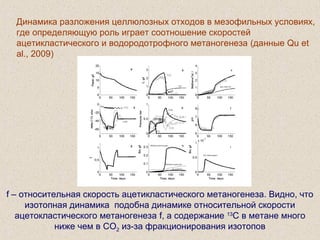
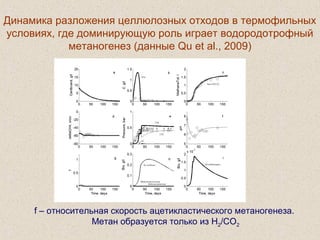
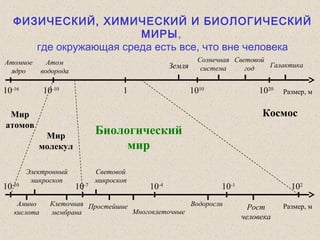
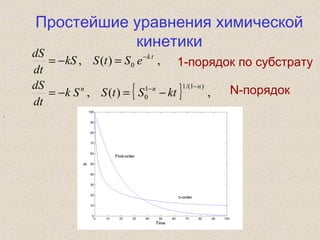
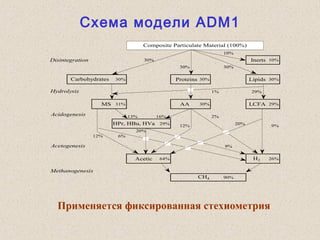
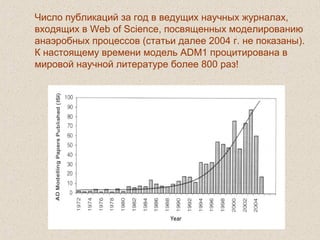
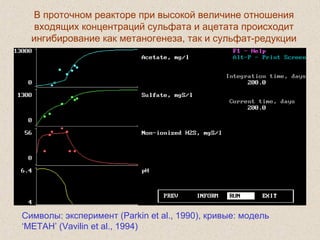
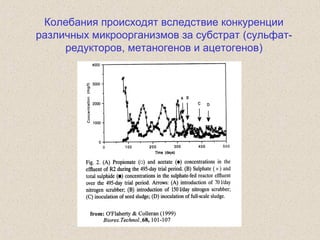
Документ обсуждает применение математического моделирования и стабильных изотопов в экологии, акцентируя внимание на анаэробных процессах и микробиологических системах. Основное внимание уделяется моделям, таким как ADM1, и их значимости для анализа экологических систем и изучения динамики роста микроорганизмов. Документ также описывает исторический контекст и развитие моделей, включая колебательные реакции и их влияние на современные исследования.




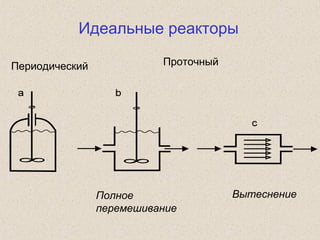


![Реактор-вытеснитель: уравнение материального баланса с
элементарным объемом V , S(x) и S(x+ x) в качестве
входящей и выходящей концентрации
V S(x) = q[S(x) - S(x+ x)] t - V (S(x)) t∆ ∆∆ ∆ ∆∆ ρ
При t и x , стремящихся к 0, получим
S
t
u
S
x
S x ( ( )) u = q/A, V=A x
∆ ∆
∆ ∆
A, площадь
поперечного сечения](https://image.slidesharecdn.com/oedmppwsls8xhtqudqe7-signature-d9d562bdf95fb945082786fb4742c84adea7e7982c98933a2587ca13b3c3893d-poli-150414063510-conversion-gate01/85/slide-10-320.jpg)


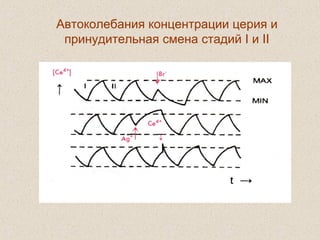






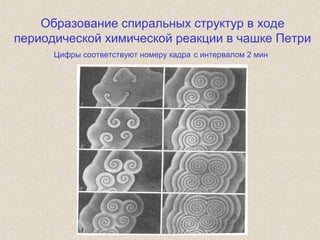


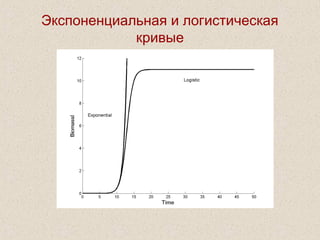
![Простейшие уравнения
биологической динамики
,)(, t
0 eNtNN
dt
dN µ
µ ==
)/1( KNN
dt
dN
−= µ
,
,
][
)( t
00
0
eNKN
NK
tN µ
−+
=
,)/1(2
2
KNN
x
N
D
t
N
−+
∂
∂
=
∂
∂
µ
Malthus, 1798
Verhulst, 1838
Fisher, 1937
Kolmogoroff et al., 1937](https://image.slidesharecdn.com/oedmppwsls8xhtqudqe7-signature-d9d562bdf95fb945082786fb4742c84adea7e7982c98933a2587ca13b3c3893d-poli-150414063510-conversion-gate01/85/slide-23-320.jpg)





















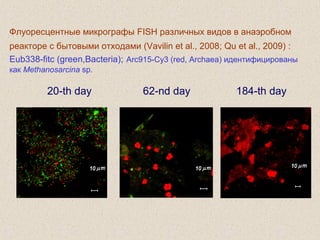




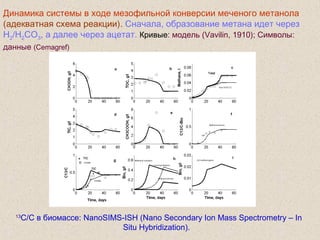
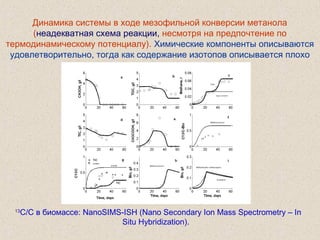

![В природе величина отношения стабильных
изотопов углерода 13
С/12
С составляет
небольшую величину, порядка 0,01, и в этом
случае она традиционно определяется при
помощи величин “приращения ”, которые
выражаются в промилях (тысячных долях)
разницы от стандарта Pee Dee Belemnite (PDB)
carbonate в моллюске, который отличается
высоким содержанием С13
1000]1
)/(
)/(
[)/( 1213
1213
13
×−=
PDB
обр
CC
CC
oooCδ](https://image.slidesharecdn.com/oedmppwsls8xhtqudqe7-signature-d9d562bdf95fb945082786fb4742c84adea7e7982c98933a2587ca13b3c3893d-poli-150414063510-conversion-gate01/85/slide-63-320.jpg)