Recommended
PDF
การเคลื่อนที่ของสัตว์มีกระดูกสันหลัง
PDF
PPT
PDF
PDF
PDF
Isomers [compatibility mode]
PDF
Isomers [compatibility mode]
PPT
PDF
PDF
PPT
PPT
PDF
สารอินทรีย์ และหมู่ฟังก์ชัน : Organic Compounds and Functional Groups
DOC
PDF
More Related Content
PDF
การเคลื่อนที่ของสัตว์มีกระดูกสันหลัง
PDF
PPT
PDF
PDF
PDF
Isomers [compatibility mode]
PDF
Isomers [compatibility mode]
PPT
Similar to Hydrocarbon
PDF
PDF
PPT
PPT
PDF
สารอินทรีย์ และหมู่ฟังก์ชัน : Organic Compounds and Functional Groups
DOC
PDF
Hydrocarbon 1. 2. การเรียกชือสารอินทรีย์
การเรียกชือสารอินทรียแบ่งเป็ น 2 ระบบ
์
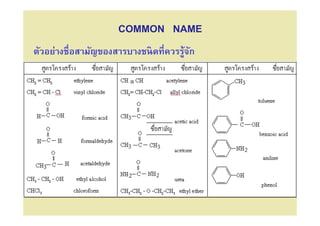
1. ชือสามัญ (common name)
ไม่มกฎเกณฑ์ทแน่นอน อาจจะเรียกชือตามสิงทีพบหรือตามสถานทีพบ
ี ี
2. ระบบ IUPAC (International Union of Pure and Applied Chemistry)
สัมพันธ์กบชนิดและสูตรโครงสร้างของสารจึงทําให้งายแก่การจดจํา ซึงยังคงใช้กน
ั ่ ั
่ ั ั
อยูในปจจุบนนี/
3. 4. IUPAC NAME
การเรียกชือตามระบบ IUPAC
หลักเกณฑ์ทวไป คือ ให้แบ่งการเรียกชือสารอินทรียออกเป็ น 3 ส่วน คือ
ั ์
ส่วนที 1 เป็ นชือโครงสร้างหลัก (basic unit หรือ parent name)
ส่วนที 2 เป็ นคําลงท้าย (suffix)
ส่วนที 3 เป็ นคํานําหน้า (prefix)
prefix + basic unit (parent name) + suffix
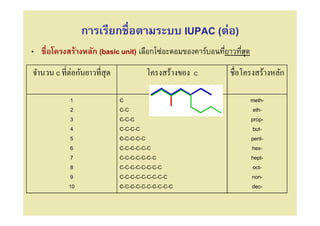
5. การเรียกชือตามระบบ IUPAC (ต่อ)
• ชือโครงสร้างหลัก (basic unit) เลือกโซ่อะตอมของคาร์บอนทียาวทีสุด
จํานวน C ทีต่อกันยาวทีสุ ด โครงสร้างของ C ชือโครงสร้างหลัก
1 C meth-
2 C-C eth-
3 C-C-C prop-
4 C-C-C-C but-
5 C-C-C-C-C pent-
6 C-C-C-C-C-C hex-
7 C-C-C-C-C-C-C hept-
8 C-C-C-C-C-C-C-C oct-
9 C-C-C-C-C-C-C-C-C non-
10 C-C-C-C-C-C-C-C-C-C dec-
6. Mnemonic for First Four Prefixes
First four prefixes
• Meth- Monkeys
• Eth- Eat
• Prop- Peeled
• But- Bananas
7. Other Prefixes
• Pent-
Decade
• Oct-
Decimal • Dec-
Decathalon • Hex-, Hept-, Non-
8. ่ ั ั
คําลงท้าย (suffix) บอกให้ทราบถึงชนิดของหมูฟงก์ชนในโมเลกุล เป็ นสารประกอบ
ประเภทใด เป็ นสารประกอบประเภทอิมตัวหรือไม่อมตัว
ิ
อ่านชือสารประเภทอืนๆ (ยกเว้น แอลคีน และแอลไคน์) เหมือนแอลเคน โดยตัด –e ตัว
ท้ายออก แล้วเติม คําลงท้ายของสารประเภทนัน (เช่น –ol, -one) แทน
/
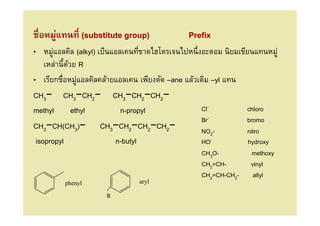
9. ชือหมู่แทนที (substitute group) Prefix
• หมูแอลคิล (alkyl) เป็ นแอลเคนทีขาดไฮโดรเจนไปหนึงอะตอม นิยมเขียนแทนหมู่
่
เหล่านี/ดวย R
้
• เรียกชือหมูแอลคิลคล้ายแอลเคน เพียงตัด –ane แล้วเติม –yl แทน
่
CH3− CH3−CH2− CH3−CH2−CH2−
methyl ethyl n-propyl Cl- chloro
Br- bromo
CH3−CH(CH3)− CH3−CH2−CH2−CH2− NO2- nitro
isopropyl n-butyl HO- hydroxy
CH3O- methoxy
CH2=CH- vinyl
CH2=CH-CH2- allyl
phenyl aryl
R
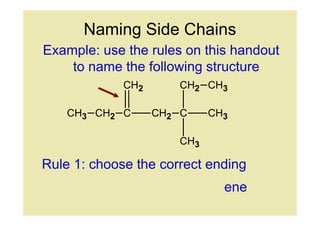
10. Naming Side Chains
Example: use the rules on this handout
to name the following structure
CH2 CH2 CH3
CH3 CH2 C CH2 C CH3
CH3
Rule 1: choose the correct ending
ene
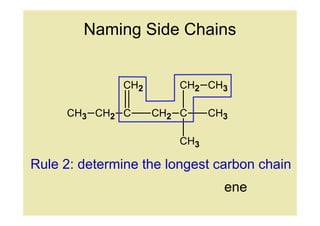
11. Naming Side Chains
CH2 CH2 CH3
CH3 CH2 C CH2 C CH3
CH3
Rule 2: determine the longest carbon chain
ene
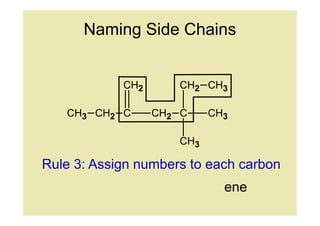
12. Naming Side Chains
CH2 CH2 CH3
CH3 CH2 C CH2 C CH3
CH3
Rule 3: Assign numbers to each carbon
ene
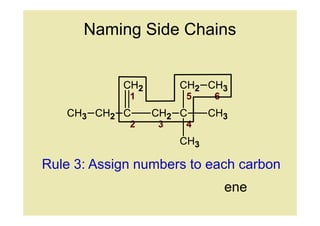
13. Naming Side Chains
CH2 CH2 CH3
1 5 6
CH3 CH2 C CH2 C CH3
2 3 4
CH3
Rule 3: Assign numbers to each carbon
ene
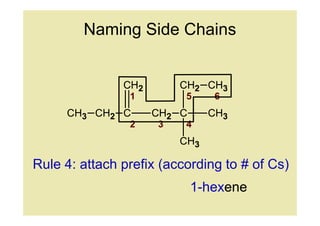
14. Naming Side Chains
CH2 CH2 CH3
1 5 6
CH3 CH2 C CH2 C CH3
2 3 4
CH3
Rule 4: attach prefix (according to # of Cs)
1-hexene
ene
15. Naming Side Chains
CH2 CH2 CH3
ethyl 1 5 6
CH3 CH2 C CH2 C CH3
2 3 4 methyl
CH3
methyl
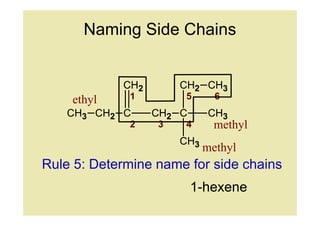
Rule 5: Determine name for side chains
1-hexene
16. Naming Side Chains
CH2 CH2 CH3
ethyl 1 5 6
CH3 CH2 C CH2 C CH3
2 3 4 methyl
CH3
methyl
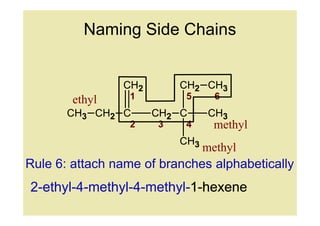
Rule 6: attach name of branches alphabetically
2-ethyl-4-methyl-4-methyl-1-hexene
1-hexene
17. Naming Side Chains
CH2 CH2 CH3
ethyl 1 5 6
CH3 CH2 C CH2 C CH3
2 3 4 methyl
CH3
methyl
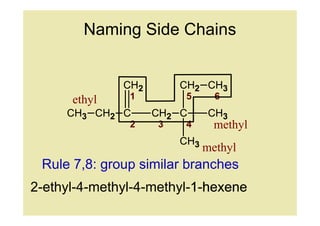
Rule 7,8: group similar branches
2-ethyl-4-methyl-4-methyl-1-hexene
1-hexene
18. Naming Side Chains
CH2 CH2 CH3
ethyl 1 5 6
CH3 CH2 C CH2 C CH3
2 3 4 methyl
CH3
methyl
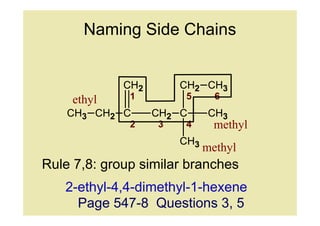
Rule 7,8: group similar branches
2-ethyl-4,4-dimethyl-1-hexene
Page 547-8 Questions 3, 5
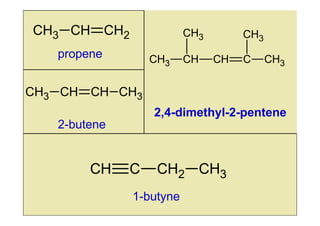
19. CH3 CH CH2 CH3 CH3
propene CH3 CH CH C CH3
CH3 CH CH CH3
2,4-dimethyl-2-pentene
2-butene
CH C CH2 CH3
1-butyne
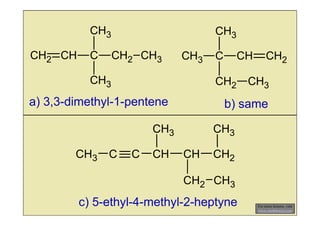
20. CH3 CH3
CH2 CH C CH2 CH3 CH3 C CH CH2
CH3 CH2 CH3
a) 3,3-dimethyl-1-pentene b) same
CH3 CH3
CH3 C C CH CH CH2
CH2 CH3
c) 5-ethyl-4-methyl-2-heptyne For more lessons, visit
www.chalkbored.com
21. ่ ั ั
1. ตําแหน่งของ C ทีหมูฟงก์ชนเกาะอยู่ ต้องนับให้อยูในตําแหน่งทีน้อยทีสุด
่
OH OH
H3C CH2 CH2 CH CH3 H3C CH2 CH2 CH CH3
1 2 3 4 5 5 4 3 2 1
2. ถ้าในโครงสร้างหลักมีพนธะคูอยูดวย จะต้องระบุตาแหน่งพันธะคูหรือพันธะสามด้วย
ั ่ ่ ้ ํ ่
โดยกําหนดให้เป็ นเลขน้อยทีสุดเพียงค่าเดียว
H3C CH2 CH CH CH3 H3C CH2 CH CH CH3
1 2 3 4 5 5 4 3 2 1
ตําแหน่งของพันธะคู่ คือ 2 ไม่ใช่ 3 หรื อ 4
22. 5.2 การเรียกชือตามระบบ IUPAC (ต่อ)
3. ถ้าในโครงสร้างหลักมีกลุมอะตอมซํ/า ๆ กันมาเกาะให้บอกจํานวนโดยใช้ภาษากรีก
่
เช่น di = 2 กลุม, tri = 3 กลุม, tetra = 4 กลุม, penta = 5 กลุม
่ ่ ่ ่
4. ถ้าในโครงสร้างหลักมีกลุมอะตอมหลายชนิดมาเกาะ ให้เรียกชือเรียงลําดับตามอักษร
่
ภาษาอังกฤษ
CH2 CH3
CH3 CH2 CH2 CH CH CH3
ตัวอย่าง CH3
6 5 4 3 2 1
1 2 3 4 5 6
• 3-ethyl-2-methylhexane หมายถึง มี ethyl มาต่อที C ตําแหน่ง 3 และ methyl
group มาต่อที C ตําแหน่ง 2 ในโครงสร้างหลักของ hexane
23. 24. ไอโซเมอริซึมของสารประกอบอินทรีย์
• ไอโซเมอริซึม (isomerism) หมายถึง ปรากฏการณ์ทสารอินทรียมสตรโมเลกุล
ี ์ ีู
เหมือนกัน แต่มสตรโครงสร้างต่างกัน ซึงอาจจะเป็ นสารประเภทเดียวหรือต่างชนิด
ีู
กันก็ได้
• ไอโซเมอร์ (isomer) หมายถึง สารอินทรียทมีสตรโมเลกุลเหมือนกัน แต่สามารถ
์ ี ู
เขียนสูตรโครงได้หลายแบบ แต่ละไอโซเมอร์มสมบัตต่างกัน
ี ิ
• C2H6O มี 2 ไอโซเมอร์
CH3–CH2–OH และ CH3–O–CH3
• C3H6O มี 2 ไอโซเมอร์
O O
H3C C CH3 H3C CH2 C H
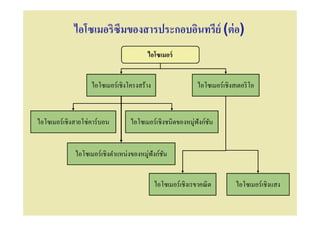
25. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
ไอโซเมอร์
ไอโซเมอร์เชิงโครงสร้าง ไอโซเมอร์เชิงสเตอริ โอ
ไอโซเมอร์เชิงสายโซ่คาร์บอน ไอโซเมอร์เชิงชนิดของหมู่ฟังก์ชน
ั
ไอโซเมอร์เชิงตําแหน่งของหมู่ฟังก์ชน
ั
ไอโซเมอร์เชิงเรขาคณิ ต ไอโซเมอร์เชิงแสง
26. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
1. ไอโซเมอร์เชิงโครงสร้าง (Structural isomer) สารอินทรียทมีสตรโมเลกุล
์ ี ู
เหมือนกันแต่มสตรโครงสร้างต่างกัน แบ่งได้เป็ น
ีู
1.1 ไอโซเมอร์เชิงสายโซ่คาร์บอน (skeleton isomer)
่ ั ั
1.2 ไอโซเมอร์เชิงตําแหน่งของหมูฟงก์ชน (positional isomer)
่ ั ั
1.3 ไอโซเมอร์เชิงชนิดของหมูฟงก์ชน (functional isomer)
2. ไอโซเมอร์เชิงสเตอริ (Stereo isomer) เป็ นไอโซเมอร์ทมีโครงแบบ
ี
(configuration) ต่างกันคือมีการจัดเรียงอะตอมในทีว่างต่างกัน (การจัด
ตําแหน่งของอะตอมใน 3 มิตแตกต่างกัน) แบ่งได้เป็ น 2 ชนิด คือ
ิ
2.1 ไอโซเมอร์เชิงเรขาคณิต (geometrical isomer)
2.2 ไอโซเมอร์เชิงแสง (optical isomer)
27. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
1. ไอโซเมอร์เชิงโครงสร้าง (Structural isomer)
1.1 ไอโซเมอร์เชิงสายโซ่คาร์บอน (skeleton isomer)
• ไอโซเมอร์ทมีการจัดเรียงตัวของคาร์บอนในโครงสร้างหลักต่างกัน
ี
• คาร์บอนอะตอมอาจต่อกันเป็ นเส้นตรงหรือเป็ นแบบกิงสาขา
• จํานวนไอโซเมอร์จะเพิมขึนเมือจํานวนคาร์บอนเพิมขึน เช่น
/ /
– C5H12 มี 3 ไอโซเมอร์ C6H14 มี 5 ไอโซเมอร์
– C7H16 มี 9 ไอโซเมอร์ C8H18 มี 18 ไอโซเมอร์
– C9H20 มี 35 ไอโซเมอร์ C10H22 มี 75 ไอโซเมอร์
• สารทีเป็ นไอโซเมอร์เชิงโครงสร้างกันจะมีสมบัตทางกายภาพและทางเคมี
ิ
ต่างกัน
28. 29. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
1.2 ไอโซเมอร์เชิงตําแหน่ งของหมู่ฟังก์ชน (positional isomer)
ั
่ ั ั
• ไอโซเมอร์ทเกิดจากหมูฟงก์ชนนัลมาเกาะกับอะตอมของคาร์บอนใน
ี
โครงสร้างหลักทีตําแหน่งต่างกัน
• เช่น C4H10O มี positional isomer ทีเป็ นแอลกอโอล์ 2 ไอโซเมอร์
30. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
1.3 ไอโซเมอร์เชิงชนิดของหมู่ฟังก์ชน (functional isomer)
ั
ี ่ ั ั
• ไอโซเมอร์ทมีหมูฟงก์ชนนัลต่างกัน เป็ นสารอินทรียต่างชนิดกันทีมีสตรโมเลกุล
์ ู
เหมือนกันแต่สตรโครงสร้างต่างกัน
ู
• ตัวอย่าง เช่น แอลกอฮอล์ กับ อีเทอร์ ทีมีสตรโมเลกุล C2H6O เป็ น functional
ู
isomer กัน
• แอลดีไฮด์ กับ คีโตน ทีมีสตรโมเลกุล C3H6O เป็ น functional isomer กัน
ู
O O
H C CH2 CH3 H3C C CH3
propanal propanone
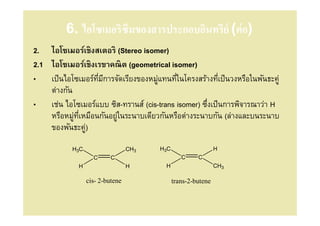
31. 6. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
2. ไอโซเมอร์เชิงสเตอริ (Stereo isomer)
2.1 ไอโซเมอร์เชิงเรขาคณิต (geometrical isomer)
• เป็ นไอโซเมอร์ทมีการจัดเรียงของหมูแทนทีในโครงสร้างทีเป็ นวงหรือในพันธะคู่
ี ่
ต่างกัน
• เช่น ไอโซเมอร์แบบ ซิส-ทรานส์ (cis-trans isomer) ซึงเป็ นการพิจารณาว่า H
หรือหมูทเหมือนกันอยูในระนาบเดียวกันหรือต่างระนาบกัน (ล่างและบนระนาบ
่ ี ่
ของพันธะคู) ่
H3C CH3 H3C H
C C C C
H H H CH3
cis- 2-butene trans-2-butene
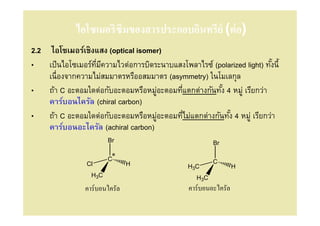
32. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
2.2 ไอโซเมอร์เชิงแสง (optical isomer)
• เป็ นไอโซเมอร์ทมีความไวต่อการบิดระนาบแสงโพลาไรซ์ (polarized light) ทังนี/
ี /
เนืองจากความไม่สมมาตรหรืออสมมาตร (asymmetry) ในโมเลกุล
• ถ้า C อะตอมใดต่อกับอะตอมหรือหมูอะตอมทีแตกต่างกันทัง 4 หมู่ เรียกว่า
่ /
คาร์บอนไครัล (chiral carbon)
• ถ้า C อะตอมใดต่อกับอะตอมหรือหมูอะตอมทีไม่แตกต่างกันทัง 4 หมู่ เรียกว่า
่ /
คาร์บอนอะไครัล (achiral carbon)
Br Br
C* C
Cl H H3C H
H3C H3C
คาร์บอนไครัล คาร์บอนอะไครัล
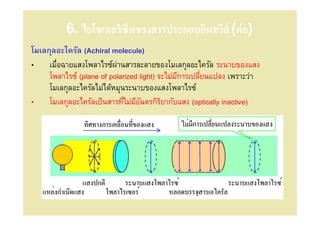
33. 6. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
โมเลกุลอะไครัล (Achiral molecule)
• เมือฉายแสงโพลาไรซ์ผานสารละลายของโมเลกุลอะไครัล ระนาบของแสง
่
โพลาไรซ์ (plane of polarized light) จะไม่มการเปลียนแปลง เพราะว่า
ี
โมเลกุลอะไครัลไม่ได้หมุนระนาบของแสงโพลาไรซ์
• โมเลกุลอะไครัลเป็ นสารทีไม่มอนตรกิรยากับแสง (optically inactive)
ีั ิ
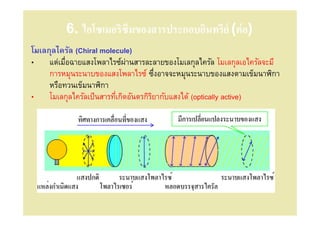
34. 6. ไอโซเมอริซึมของสารประกอบอินทรีย์ (ต่ อ)
โมเลกุลไครัล (Chiral molecule)
• แต่เมือฉายแสงโพลาไรซ์ผานสารละลายของโมเลกุลไครัล โมเลกุลเอไครัลจะมี
่
การหมุนระนาบของแสงโพลาไรซ์ ซึงอาจจะหมุนระนาบของแสงตามเข็มนาฬิกา
หรือทวนเข็มนาฬิกา
• โมเลกุลไครัลเป็ นสารทีเกิดอันตรกิรยากับแสงได้ (optically active)
ิ