CHUẨN ĐỘ BÀI 4.pdf
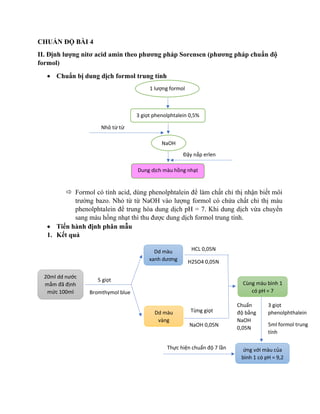
- 1. CHUẨN ĐỘ BÀI 4 II. Định lượng nitơ acid amin theo phương pháp Sorensen (phương pháp chuẩn độ formol) • Chuẩn bị dung dịch formol trung tính Formol có tính acid, dùng phenolphtalein để làm chất chỉ thị nhận biết môi trường bazo. Nhỏ từ từ NaOH vào lượng formol có chứa chất chỉ thị màu phenolphtalein để trung hòa dung dịch pH = 7. Khi dung dịch vừa chuyển sang màu hồng nhạt thì thu được dung dịch formol trung tính. • Tiến hành định phân mẫu 1. Kết quả Đậy nắp erlen 1 lượng formol 3 giọt phenolphtalein 0,5% NaOH Nhỏ từ từ Dung dịch màu hồng nhạt Thực hiện chuẩn độ 7 lần NaOH 0,05N Cùng màu bình 1 có pH = 7 3 giọt phenolphthalein 5ml formol trung tính Chuẩn độ bằng NaOH 0,05N ứng với màu của bình 1 có pH = 9,2 20ml dd nước mắm đã định mức 100ml 5 giọt Bromthymol blue Dd màu xanh dương Dd màu vàng HCL 0,05N H2SO4 0,05N Từng giọt
- 2. - Chuẩn độ dung dịch mẫu (nước mắm) Dung dịch có màu vàng khi thêm 5 giọt Bromthymol blue Thêm NaOH 0,05N dung dịch mẫu có màu ứng với màu của bình pH 7
- 3. - Chuẩn độ thí nghiệm kiểm chứng, tương tự thay dung dịch mẫu bằng nước cất. Dung dịch mẫu sau khi chuẩn độ với NaOH 0,05N ứng với màu của bình pH 9,2 lần 1 Dung dịch mẫu Dung dịch có pH 9.2 Dung dịch mẫu sau khi chuẩn độ với NaOH 0,05N ứng với màu của bình pH 9,2 lần 2 Dung dịch mẫu Dung dịch có pH 9.2 Dung dịch có màu xanh dương khi thêm 5 giọt Bromthymol blue
- 4. 2. Biện luận - Trong acid amin có cả nhóm –COOH (tính acid) và -NH2 (tính bazo), do đó ta cho tác dụng với formol HCHO để nhóm –NH2 tạo thành nhóm –N=CH2 làm mất tính base. Từ đó ta có thể chuẩn độ trung hòa bằng NaOH và chất chỉ thị. Phản ứng xảy ra giữa acid amin và formol. - Các axit amin trong dung dịch nước thì trung tính, khi gặp formol, các axit amin bị mất tính kiềm, tính axit của nhóm COOH trội lên. Do đó có thể định lượng nhóm COOH bằng một dung dịch kiềm chuẩn. - Khi thêm 5 giọt Bromthymol Blue. Có 3 trường hợp: + Mẫu có màu xanh lục nhạt giống bình mẫu pH 7 → môi trường trung tính. Thêm H2SO4 0,05N dung dịch mẫu có màu ứng với màu của bình pH 7 Dung dịch mẫu sau khi chuẩn độ với NaOH 0,05N ứng với màu của bình pH 9,2 Dung dịch có pH 9,2 Dung dịch mẫu
- 5. + Mẫu có màu xanh dương → môi trường base → thêm acid cho đến khi dung dịch có màu như bình 1 (pH 7). + Mẫu có màu vàng → môi trường acid → thêm NaOH cho đến khi dung dịch có màu như bình 1 (pH 7). - Ranh giới chuyển màu trước và sau điểm tương đương rất rõ ràng nên kết quả ổn định. Thời gian phân tích nhanh, điều kiện đơn giản, ít tốn hóa chất. - Acid amin là thành phần cấu tạo nên protein có vai trò quan trọng trong hình thành sự sống. Các acid amin kết hợp với nhau theo tỉ lệ nhất định sẽ tạo nên các loại protein khác nhau và có vai trò khác nhau. Việc phân tích đạm formol giúp xác định giá trị dinh dưỡng của thực phẩm. 3. Tính toán kết quả - Dung dịch mẫu: Lần 1 2 3 4 5 6 7 VNước mắm (ml) 20,00 VNaOH (ml) 3,20 3,15 3,20 3,20 3,15 3,15 3,15 - Dung dịch kiểm chứng: Lần 1 2 3 4 5 6 7 VNước cất (ml) 20,00 VNaOH (ml) 1,25 1,30 1,30 1,25 1,25 1,25 1,25 Ta có, công thức số gam Nito acid amin có trong 1 lít nước mắm: 𝑿 = (𝒂 − 𝒃) 𝒙 𝑻 𝒙 𝟎, 𝟎𝟎𝟎𝟕 𝒙 𝑽𝑫𝑴 𝒙 𝟏𝟎𝟎𝟎 𝟐𝟎 𝒙 𝑽 (𝟏) Trong đó: X: Lượng gam nitơ acid amin có trong 1L nước mắm. a: Số mL NaOH 0.1N dùng để chuẩn dung dịch thí nghiệm (lấy trung bình). b: Số mL NaOH 0.1N dùng để chuẩn dung dịch kiểm chứng. T: Hệ số hiệu chỉnh nồng độ của dung dịch NaOH đem dùng so với nồng độ chuẩn (T=1). VDM: Thể tích bình định mức. V: Số mL nước mắm cho vào bình định mức. 0.0014: Số gam nitơ ứng với 1mL NaOH 0.1N • Từ (1), ta tính lần 1:
- 6. = (3,20 − 1,25) 𝑥 1 𝑥 0,0007 𝑥 100,00 𝑥 1000 20,00 𝑥 1 = 6,825 - Tương tự, ta tính được số gam Nito acid amin từ lần 2 -> 7 theo thứ tự: 6,475; 6,65; 6,825; 6,65; 6,65; 6,65. Mặt khác: n = 7, f = n -1 = 6 và tại P = 0,95 => tp,f = 2,48 X ̅ = 6,675 Sx = 0,1207614729 𝜀 = 𝑡𝑝,𝑓 𝑥 𝑆𝑥 √𝑛 = 2,48 𝑥 0,1207614729 √7 = 0,1131960009 = 0,11 Vậy, số gam Nito acid amin có trong 1 lít nước mắm là X = 6,675 ± 0,11