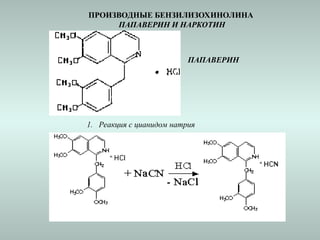
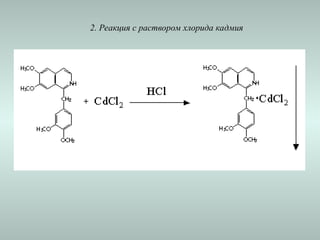
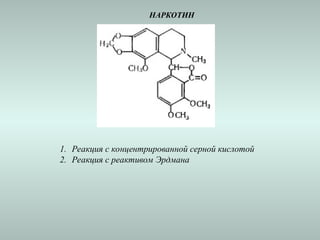
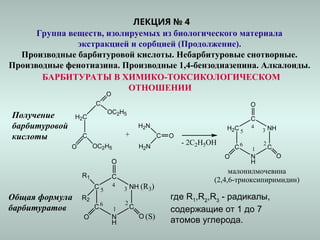
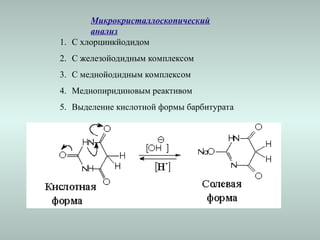
Документ посвящён изучению и классификации барбитуратов и алкалоидов, их свойствам и методам анализа. Рассматриваются пути получения, токсикологические исследования и метаболизм различных производных барбитуровой кислоты и алкалоидов, а также их влияние на организм. Упоминаются методы идентификации, количественного анализа и токсикокинетические особенности этих веществ.














![Общеалкалоидные осадительные реактивы:
1. Реактивы, дающие с алкалоидами простые соли:
- раствор таннина, пикриновая, пикролоновая и некоторые другие
органические кислоты.
2. Реактивы, дающие с алкалоидами комплексные соединения.
а) реактивы, содержащие в своем составе металлоиды:
1) I2
/KI - реактив Бушарда-Вагнера
2)H3
PO4
I2MoO3
- фосфорномолибденовая кислота (реактив
Зонненшейна)
3)Н3
РО4
12WO3
2Н2
О- фосфорновольфрамовая кислота (реактив
Шейблера)
б) реактивы, содержащие в своем составе металлы:
1)ВiI3
/KI - реактив Драгендорфа (К[ВiI4
])
2)CdI2
/KI - реактив Марме (K2
[CdI4
])
3)HgI2
/KI- реактив Майера (K2
[HgI4
])
4)H2
[PtCl6
] - платинохлористоводородная кислота
5)Н[АuСl4
] - золотохлористоводородная кислота](https://image.slidesharecdn.com/lekc42-241014185635-88d5f843/85/l-18-320.jpg)





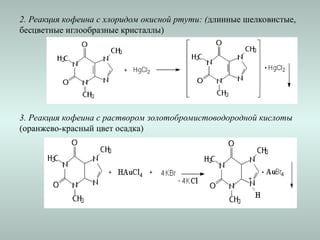


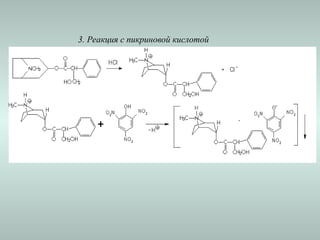
![3. Реакция образования пикрата ареколина и никотина
4. Реакция образования рейнеката никотина и анабазина
N
+
CH3
COOCH3
H
O
NO2
NO2
O2
N
N
CH3
COOCH3
+
OH
NO2
NO2
O2
N
*
N
N
H
+ HCL N
+
N
H H
+ CL
-
N
+
N
H H
+ NH4
[Cr(NH3
)2
(CNS)4
] NH4 +
+
N
+
N
H H
[Cr(NH3
)2
(CNS)4
]
*](https://image.slidesharecdn.com/lekc42-241014185635-88d5f843/85/l-27-320.jpg)

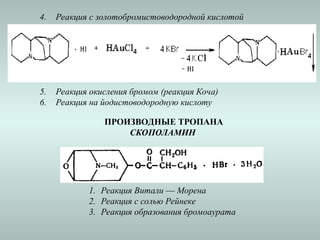





![1. Реакция образования таллейохина
N
O
O
R
+ NH
H
H
+
N
R
OH
HO
HO N
R O
N
N
OH
HO
R
талейохин
1. Реакция получения эритрохинина
N
H3CO
R
Br2
K3[Fe(CN)6]
/OH
N
O
O
H3CO
R
N
H3CO
H R
H2
_
N
O
H3CO
R
O
N
R
OCH3
1. Реакция с раствором роданида аммония](https://image.slidesharecdn.com/lekc42-241014185635-88d5f843/85/l-36-320.jpg)