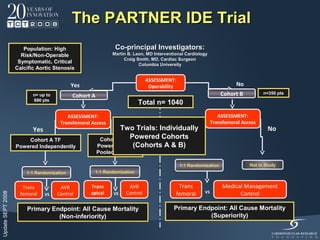
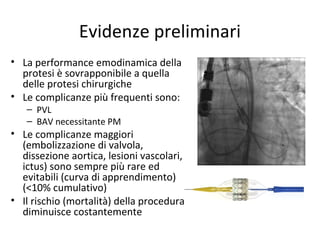
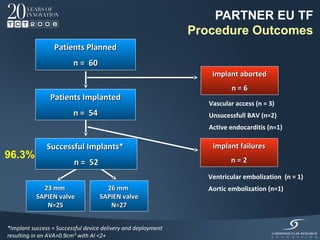
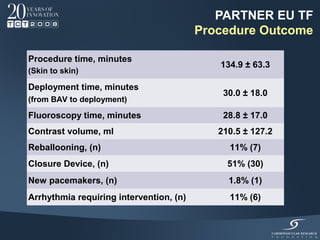
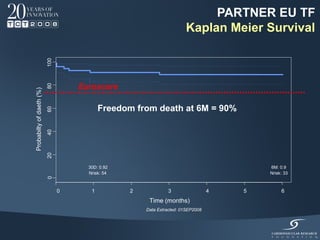
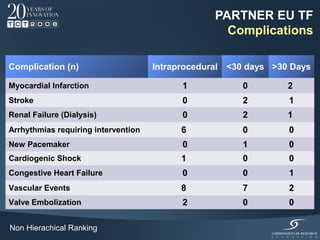
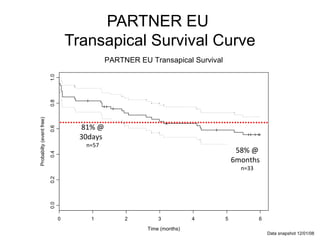
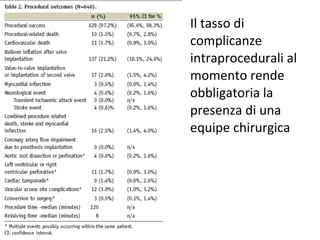
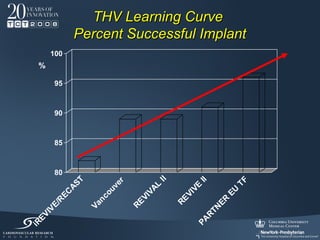
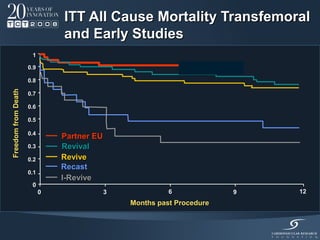
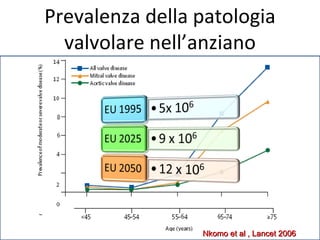
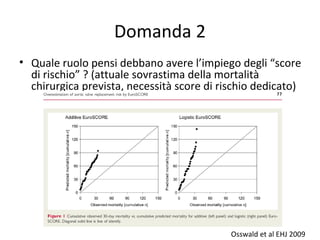
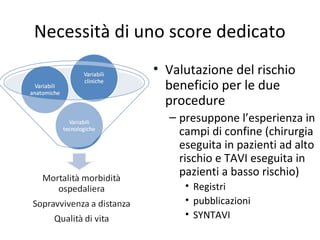
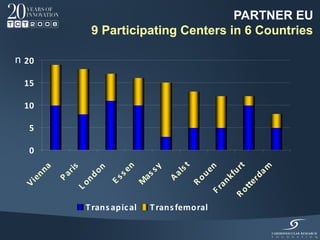
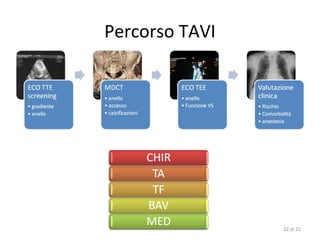
Il documento discute l'uso delle endoprotesi valvolate per il trattamento della stenosi aortica, evidenziando l'importanza di identificare pazienti idonei e il ruolo degli score di rischio. Sono analizzati risultati clinici, complicanze e l'evoluzione della procedura, suggerendo che l'approccio transcatetere diventerà la prima scelta per i pazienti a basso rischio. Infine, si sottolinea la necessità di centri di eccellenza e team multidisciplinari per una gestione efficace dei pazienti.