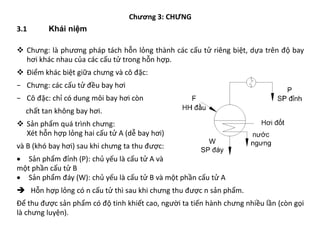
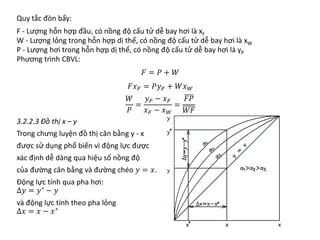
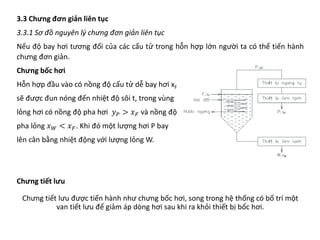
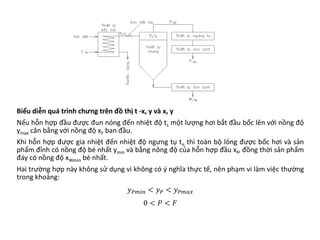
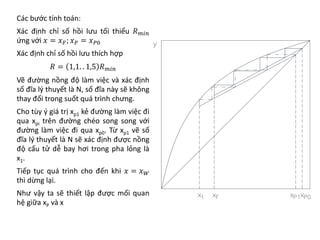
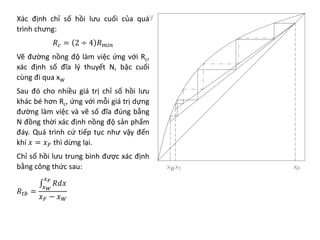
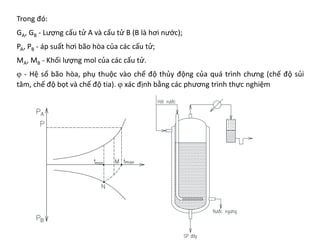
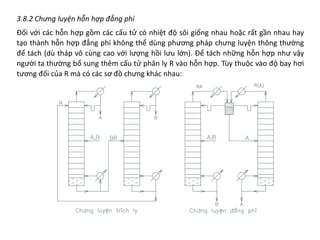
Chương 3 trình bày về quá trình chưng, phương pháp tách hỗn lỏng dựa trên độ bay hơi khác nhau của các cấu tử, cùng với các ứng dụng và cân bằng pha của hỗn hợp hai cấu tử. Các khái niệm như hỗn hợp lý tưởng và thực, cũng như các phương pháp chưng đơn giản và chưng luyện liên tục được đề cập. Cuối cùng, các phương trình cân bằng vật liệu và nhiệt lượng trong quá trình chưng luyện cũng được mô tả chi tiết.