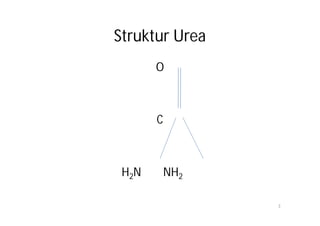
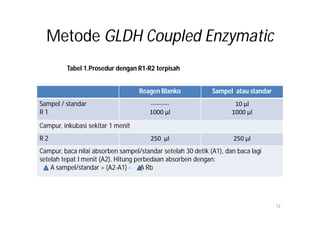
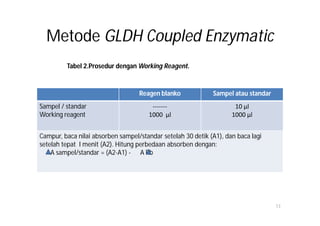
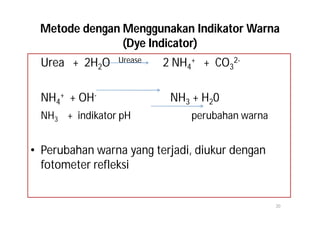
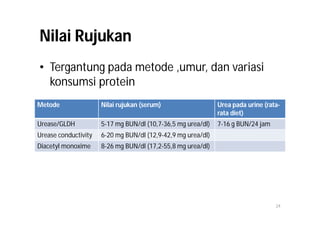
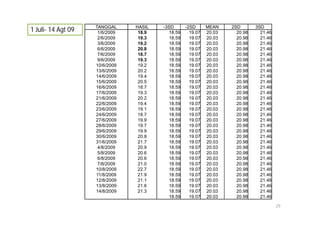
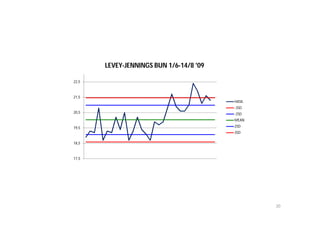
Dokumen ini membahas tentang pemeriksaan kadar urea dalam darah, termasuk metabolisme, metabolisme, dan berbagai metode pengukurannya. Kadar urea berfungsi sebagai indikator kesehatan renal, dengan pengukuran yang bergantung pada berbagai faktor seperti diet dan fungsi ginjal. Terdapat beberapa metode pengukuran urea, seperti metode enzimatik, kimia, dan konduktimetri, dengan nilai rujukan yang bervariasi tergantung metoda dan kondisi individu.