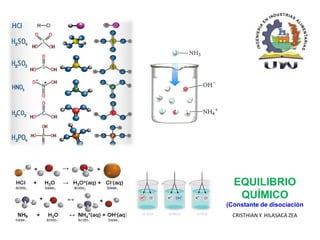
Constante de disociacion
- 1. EQUILIBRIO QUÍMICO (Constante de disociación CRISTHIAN Y. HILASACA ZEA
- 2. El agua es un electrolito débil y es capaz de disociarse en una proporción muy escasa y originar tanto H+ como OH- (Figura izquierda de la tabla). Se comporta, por tanto, como ácido y como base. Por este motivo se dice que el agua es una sustancia anfótera o anfolito. Disociación en química y bioquímica es un proceso general en el cual complejos, moléculas o sales se separan en moléculas más pequeñas, iones o radicales, usualmente de manera reversible. Disociación es lo opuesto de la asociación y de la recombinación. La disociación de los ácidos en una solución significa la liberación de un protón H+, éste es un proceso de equilibrio, esto quiere decir que disociación y la recombinación ocurren al mismo tiempo con la misma velocidad. La constante de disociación de los ácidos Ka indica qué tan fuerte es un ácido, los ácidos fuertes poseen una Ka de mayor valor (por lo tanto menor pKa). El estudio de estos equilibrios se llama Equilibrio ácido-base. INTRODUCCIÓN
- 3. EQUILIBRIO ÁCIDO - BASE
- 4. CONSTANTES DE DISOCIACIÓN PARA ÁCIDOS Y BASES DÉBILES Ácido débil; base débil (HA + A-) Efecto del ion común 𝐻𝑁𝑂2 + 𝐻2𝑂 ⇌ 𝐻3𝑂+ + 𝑁𝑂2 − (sistema en equilibrio) 0,2 x x ácido débil iones comunes: 𝐻3𝑂+ ; 𝑁𝑂2 − Si se adiciona NaNO2 𝑁𝑎𝑁𝑂2 → 𝑁𝑎+ + 𝑁𝑂2 − 0,1 0,1 (ion común (perturba el equilibrio 𝐾𝑎 = 𝐻3𝑂+ 𝑁𝑂2 − 𝐻𝑁𝑂2 𝐻3𝑂+ = 𝐾𝑎. 𝐻𝑁𝑂2 𝑁𝑂2 − A medida que aumenta el PH, la 𝐻3𝑂+ disminuye El NO2 − del NaNO2, disminuye la disociación del ácido (HNO2) * Por lo tanto al disminuir la disociación del HNO2, el equilibrio se ve perturbado por el efecto del ion común (𝑁𝑂2 − ); el equilibrio se rompe, la reacción se desplaza hacia la izquierda, incrementándose la 𝐻𝑁𝑂2 El ion común disminuye la disociación del ácido: La 𝐻3𝑂+ que aporta el ácido es menor, entonces el pH será menor.
- 5. EJEMPLO 01: Hallar el pH de una solución de HNO2 0,2 M Solución: 𝐻𝑁𝑂2 ⇌ 𝐻+ + 𝑁𝑂2 − 𝐾𝑎 = 4,5 × 10−4 𝐻3𝑂+ = 𝐾𝑎. 𝐶𝑎 𝐻3𝑂+ = (4,5 × 10−4)(0,2) 𝐻3𝑂+ = 9,48 × 10−3 𝑝𝐻 = −𝑙𝑜𝑔 𝐻3𝑂+ 𝑝𝐻 = −𝑙𝑜𝑔 (9,48 × 10−3) 𝑝𝐻 = 2,02
- 6. EJEMPLO 02: Hallar el pH de una solución de HNO2 0,2 M, si se le agrega una solución de NaNO2 0,3 M Solución: 𝐻𝑁𝑂2 + 𝐻2𝑂 ⇌ 𝐻3𝑂+ + 𝑁𝑂2 − (sistema en equilibrio) 0,2 x x 𝑁𝑎𝑁𝑂2 → 𝑁𝑎+ + 𝑁𝑂2 − disminuye la disociación de HNO2 ion no común ion común 0,3 0,3 𝐾𝑎 = 4,5 × 10−4 2𝐻2𝑂 ⇌ 𝐻3𝑂+ + 𝑂𝐻− 𝐾𝑎 = 𝐻3𝑂+ 𝑁𝑂2 − 𝐻𝑁𝑂2 𝐻3𝑂+ = 𝐾𝑎. 𝐻𝑁𝑂2 𝑁𝑂2 − 𝐻3𝑂+ = 4,5 × 10−4 . 0,2 0,3 𝐻3𝑂+ = 3 × 10−4 𝑝𝐻 = −𝑙𝑜𝑔(3 × 10−4) 𝑝𝐻 = −𝑙𝑜𝑔 𝐻3𝑂+ 𝑝𝐻 = 3,52 𝑁𝑂2 − = 0,2 − 𝑥 (lo que se disocia) 𝑁𝑂2 − = 0,3 − 𝑥 (lo que se forma) “x” es insignificante; por lo tanto se desprecia
- 7. TRATAMIENTO GENERAL 𝐾𝑎 = 𝐻3𝑂+ 𝐴− 𝐻𝐴 𝐻3𝑂+ = 𝐾𝑎. 𝐻𝐴 𝐴− 𝐵𝑀 → 𝐴− + 𝐻𝐴 = 𝐶𝑏 + 𝐶𝑎 𝐵𝐶 → 𝑁𝑎+ + 𝐻3𝑂+ = 𝐴− + 𝑂𝐻− 𝐶𝑏 + 𝐻3𝑂+ = 𝐴− + 𝑂𝐻− 𝐴− = 𝐶𝑏 + 𝐻3𝑂+ − 𝑂𝐻− Reemplazando en BM: 𝐵𝑀 → 𝐶𝑏 + 𝐻3𝑂+ − 𝑂𝐻− + 𝐻𝐴 = 𝐶𝑏 + 𝐶𝑎 𝐻3𝑂+ − 𝑂𝐻− + 𝐻𝐴 = 𝐶𝑎 𝐻𝐴 = 𝐶𝑎 − 𝐻3𝑂+ + 𝑂𝐻− Reemplazando 𝐻3𝑂+ : 𝐻𝐴 = 𝐶𝑎 + 𝐾𝑎. 𝐻𝐴 𝐴− + 𝑂𝐻− 𝐶𝑎 + 𝑂𝐻− = 𝐻𝐴 + 𝐾𝑎. 𝐻𝐴 𝐴− 𝐻𝐴 = 𝐶𝑎 𝐴− + 𝑂𝐻− 𝐴− 𝐴− + 𝐾𝑎 ………… (1) ………… (2)
- 8. Reemplazando 1 y 2 en Ka 𝐾𝑎 = 𝐻3𝑂+ . 𝐶𝑏 + 𝐻3𝑂+ − 𝑂𝐻− 𝐶𝑎. 𝐻3𝑂+ + 𝑂𝐻− Cuando se considera la disociación del ácido y la hidrólisis de la base: 𝐻3𝑂+ = 𝐾𝑎.(𝐶𝑎 − 𝐻3𝑂+ + 𝑂𝐻− ) 𝐶𝑏 + 𝐻3𝑂+ − 𝑂𝐻− ECUACIÓN GENERAL Considerar en todos los equilibrios 𝐻𝑁𝑂2 ⇌ 𝐻3𝑂+ + 𝑁𝑂2 − 0,2 x x 𝑁𝑎𝑁𝑂2 → 𝑁𝑎+ + 𝑁𝑂2 − + 𝐻2𝑂 ⇌ 𝐻𝑁𝑂2 + 𝑂𝐻− 𝑁𝑂2 − 𝑇 = 𝐶𝑏 + 𝐻3𝑂+ − 𝑂𝐻− 𝐻𝑁𝑂2 𝑇 = 𝐶𝑎 − 𝐻3𝑂+ + 𝑂𝐻− Como: Ka = 4,5x10-4 𝐾𝑏 = 𝐾𝑤 𝐾𝑎 𝐾𝑏 = 2,22 × 10−11 Como es tan pequeño, no se considera.
- 9. INDICADORES Es una sustancia que puede ser de carácter ácido o básico débil, que posee la propiedad de presentar coloraciones diferentes dependiendo del pH de la disolución en la que dicha sustancia se encuentre diluida. 𝐻 − 𝐼𝑛𝑑𝑖𝑐𝑎𝑑𝑜𝑟 𝐾𝑎 = 𝐻3𝑂+ 𝐼𝑛𝑑− 𝐻 − 𝐼𝑛𝑑 Que es un indicador ácido – base? 𝐻2𝑂 + 𝐻3𝑂+ + 𝐼𝑛𝑑𝑖𝑐𝑎𝑑𝑜𝑟− 𝐼𝑛𝑑𝑖𝑐𝑎𝑑𝑜𝑟− 𝐻2𝑂 + 𝑂𝐻− + 𝐻 − 𝐼𝑛𝑑𝑖𝑐𝑎𝑑𝑜𝑟 (ácido) (base) Ka Kb 𝐻3𝑂+ = 𝐾𝑎. 𝐻 − 𝐼𝑛𝑑 𝐼𝑛𝑑− ; solución ácida solución básica rojo amarillo Anaranjado de metilo 𝐻3𝑂+ = 𝐾𝑎. 10 1 ; 10 1 ; 10 1 rojo amarillo naranja ⇌ ⇌
- 10. − 𝑙𝑜𝑔 𝐻3𝑂+ = −𝑙𝑜𝑔. 𝑘𝑎. 10 1 𝑝𝐻 = 𝑝𝑘𝑎. 𝐻 − 𝐼𝑛𝑑 𝐼𝑛𝑑− ; 𝑝𝐻 = 𝑝𝑘𝑎 − 1 − 𝑙𝑜𝑔 𝐻3𝑂+ = −𝑙𝑜𝑔. 𝑘𝑎. 1 10 𝑝𝐻 = 𝑝𝑘𝑎 + 1 𝑝𝐻 = 𝑝𝑘𝑎 + 1 Sirve para elegir un indicador ácido - base cuando: 10 10 𝑝𝐻 = 𝑝𝑘𝑎 𝑝𝐻 = 𝑝𝑘𝑎 5 = 5 𝑝𝐻 = 5 𝑘𝑎 = 1 × 10−5 𝑘𝑎 = 1 × 10−4 ; 1 × 10−5 ; 1 × 10−6 * si se considera para: 10 1 ; 1 10
- 12. EJERCICIO 01: Formular la disociación iónica de las siguientes sustancias: a) Ácido sulfúrico, ácido sulfuroso b) Ácido fosfórico, ácido fosforoso c) Ácido carbónico, ácido carbonoso d) Ácido acético, ácido metanoico, ácido propanoico e) Ácido cianhídrico, ácido clórico f) Hidróxido de sodio, hidróxido de potasio g) Hidróxido de estroncio, hidróxido de aluminio EJERCICIO 02: Determinar los ácidos y las bases conjugadas del ácido sulfúrico y del ácido carbónico; indicando las reacciones para cada caso. EJERCICIO 03: Indicar los respectivos pares conjugados del HPO4 2− y del HCO3 − frente a un ácido y a una base. EJERCICIO 04: Clasifica a las siguientes sustancias como ácido o bases, según la teoría de Bronsted-Lowry. a) CO3 2− b) NH3 c) H3O+
- 13. EJERCICIO 05: Indicar las respectivas bases y ácidos conjugados de las siguientes especies. a) H2CO3 b) NH3 c) HCl EJERCICIO 06: Determinar el pH, pOH y la [OH-] de una solución coloreada cuya concentración de iones hidronio es igual a 10-9. EJERCICIO 07: Si el pH de una disolución es 4,2. ¿Cuál es la concentración de iones hidronio e iones hidroxilo? EJERCICIO 08: Determinar el pH y el pOH de una solución 0,2 M de hidróxido de sodio. EJERCICIO 09: Determinar el pH de una solución, cuando se disuelven 2 gramos de ácido nítrico en 600 mL de disolución EJERCICIO 10: Calcular el pH de una solución cuando se mezclan 10 mL de una solución del ácido perclórico 0,3 M con 25 mL de una disolución de ácido clorhídrico 0,35 M.
