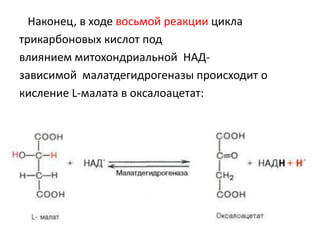
Цикл Кребса, впервые описанный английским биохимиком Г. Кребсом, является центральным процессом метаболизма, в котором происходит полное окисление ацетил-коа,Derived from катаболизма углеводов, жирных кислот и аминокислот. Цикл состоит из восьми последовательных реакций, проходящих в митохондриальном матриксе, и включает в себя преобразования лимонной кислоты, изолимонной кислоты, сукцината и других соединений, производя углекислый газ и воду. Кроме энергетической функции, цикл также участвует в анаболических и катаболических процессах, обеспечивая синтез органических веществ и транспортировку водорода.