Cinetica chimica
- 1. CINETICA CHIMICA
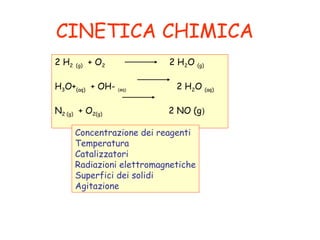
2 H2 (g) + O2 2 H 2O (g)
H3O+(aq) + OH- (aq) 2 H2O (aq)
N2 (g) + O2(g) 2 NO (g)
Concentrazione dei reagenti
Temperatura
Catalizzatori
Radiazioni elettromagnetiche
Superfici dei solidi
Agitazione
- 2. A prodotti d[A]
V=-
A prodotti dt
- 8. Cinetiche di 1° ordine
aA prodotti
1 d[A]
- = k [A]
a dt
[A]
t
d[A] d[A]
= - k’ dt = - k’ dt
[A] [A]o
[A]
to
ln [A] = - K(t – to)
[A]o
ln [A] = - kt +ln [Ao]
- 11. Cinetiche di 2° ordine
aA prodotti
1 d[A]
- = k [A]2
a dt
[A]
t
d[A] d[A]
- = k dt =- k dt
[A]2 [A]o
[A]2
to
1 1
- = - K(t – to)
[A] [A]o
- 16. Effetto della temperatura
k=Ae –Ea/RT
ln k = ln A – Ea/RT
K = K’T½ poiché
1 3
2 mv = 2 KT
2
KT √T
= =2
K300 √ 300
T =22 · 300 = 1200 K
- 27. Meccanismi di reazione
H2 + I 2 2HI
d[H2]
- = k [H2] [I2]
dt
2NO2 + F2 2NO2F
d[F2]
- = k [NO2] [F2]
dt
k’
NO2 + F2 NO2F + F stadio lento
k’’
F + NO2 NO2F
- 28. Meccanismi di reazione
H2 + Br2 2HBr
d[H2]
- = k [H ] [Br ]½
dt 2 2
Br2 2 Br [Br] = (Keq [Br ])½
2
{
Br + H2 HBr + H stadio lento
Reazioni a catena
H + Br2 HBr + Br