урок № 1
- 2. Ступінь окиснення – це умовний цілочисельний заряд з припущення, що всі полярні зв'язки є йонними. атомів хімічного елемента в сполуках, який обчислюють О
- 3. 1Н 8О
- 4. 1Н 8О
- 5. 1Н 8О
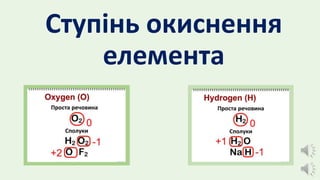
- 7. Н 𝟐 +𝟏 О− 𝟐 1Н 8Оδ1 − δ2 + δ2 + −2 +1 +1
- 8. Н 𝟐 +𝟏 О−𝟐 на себе спільні електронні пари. Електронегативність – це здатність атомів відтягувати
- 9. Шкала електронегативності хімічних елементів за Полінгом
- 10. Електронегативність залежить від радіусу атомів
- 11. Сума ступенів окиснення всіх атомів у речовині дорівнює нулю. Правила визначення ступенів окиснення елементів
- 12. Ступінь окиснення елементів у простих речовинах дорівнює 0. O2 H2 S8 000 Правила визначення ступенів окиснення елементів
- 13. Металічні елементи в сполуках проявляють позитивний ступінь окисненння. Правила визначення ступенів окиснення елементів
- 14. +2 +1 +3
- 15. Н0 + ē = Н LiH CaH2 Гідроген у сполуках має ступінь окиснення з неметалічними елементами +1 з металічними елементами -1 H2S HCl NH3 +1+1+1 SiH4 −1 ―1―1 Правила визначення ступенів окиснення елементів Н0 − ē = Н+1 −1 1Н
- 16. Флуор в сполуках завжди має ступінь окиснення -1. OF2 +2 −1 Правила визначення ступенів окиснення елементів + − 1∙2 = − 20−(− 2) = +20
- 17. H2O2 Na2O2 CuO Mg(OH)2 HNO3 Оксиген найчастіше має ступінь окиснення -2. −2 У пероксидах ступінь окиснення Оксигену -1. + + Правила визначення ступенів окиснення елементів −1 −1
- 18. Mn2O7 CrO3 V2O5 ↑↓ ↑↓ ↑↓ ↑ Максимально можливий ступінь окиснення елемента найчастіше збігається з номером групи періодичної системи, в якій розміщено елемент. Правила визначення ступенів окиснення елементів Cl*** ↑ ↑ ↑ ↑ ↑ ↑ ↑ Cl2O7 +7 +7 +6 +5
- 19. 8−7=1 Мінімальний (негативний) ступінь окиснення неметалічних елементів можна обчислити за формулою: 8 - № групи періодичної системи, в якій розміщено елемент. CH4 −4 8−4=4 Правила визначення ступенів окиснення елементів HBr −1
- 20. P2S3 −+ 8−6 = 2 2 3∙(−2) = −6 66/2 = 3 3
- 21. Н2SО3 −2 3∙(−2) = −6 +1 2∙(+1) = +2 = 0+2 + х +(−6) +4
- 22. K2Cr2О7 −2 7∙(−2) = −14 +1 2∙(+1) = +2 = 0+2 + 2х +(−14) +6
- 23. Ступінь окиснення – це умовний цілочисельний заряд атомів в речовині. Ступінь окиснення можна визначити, використовуючи правило електронейтральності речовин.