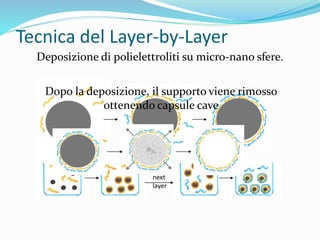
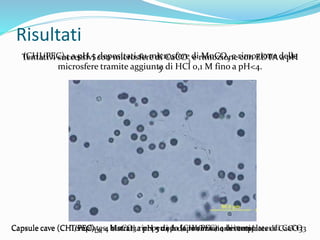
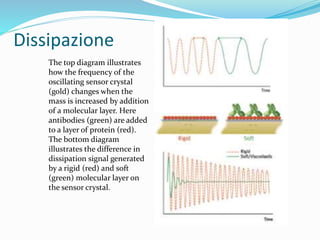
Il documento descrive un progetto di ricerca volto alla creazione di idrogeli contenenti nanocapsule polimeriche (NPCs) di pectina e chitosano, esplorando la loro interazione e applicazione nel controllo del rilascio di farmaci bioattivi. Si evidenziano i metodi di sintesi e deposizione delle NPCs tramite la tecnica layer-by-layer, i risultati relativi all'efficacia delle pectine a diverso grado di metilazione, e le potenti potenzialità future nel campo del drug delivery. L'obiettivo finale è quello di sviluppare un sistema biocompatibile stabile, in grado di rilasciare farmaci in modo controllato e specifico presso il sito della malattia.