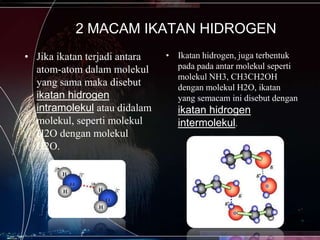
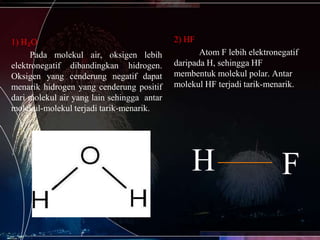
Dokumen ini membahas tentang ikatan hidrogen, yaitu gaya tarik antarmolekul yang terjadi antara dua muatan listrik parsial dengan polaritas berlawanan. Ikatan hidrogen terjadi ketika atom F, O, atau N memiliki pasangan elektron bebas yang berinteraksi dengan hidrogen molekul lain. Kekuatan ikatan dipengaruhi oleh perbedaan elektronegativitas atom-atom. Ikatan hidrogen mempengaruhi titik didih senyawa, semakin besar ikatan hidrogenny