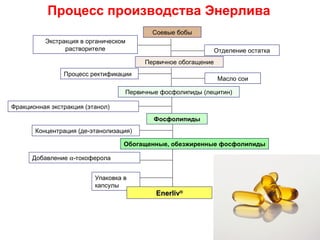
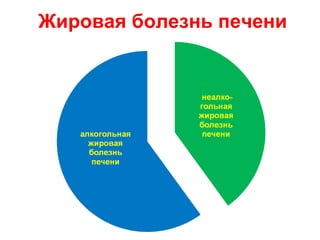
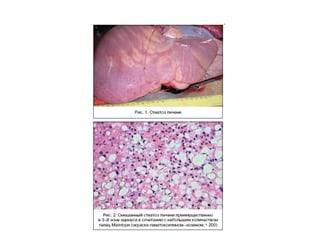
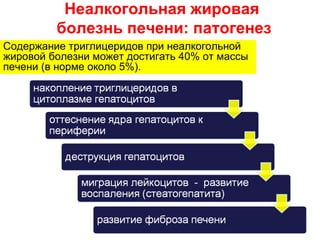
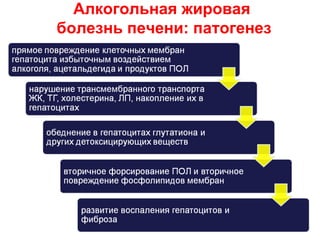
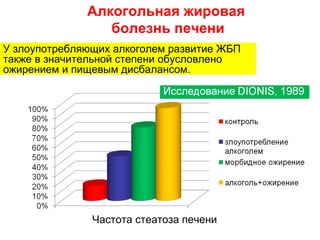
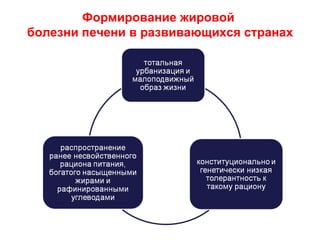
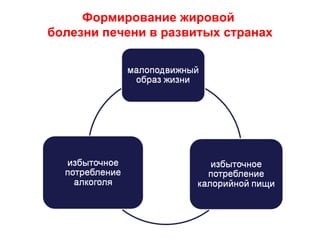
Документ посвящен жировой болезни печени, ее причинам, эпидемиологии и патогенезу, а также современным методам лечения. Отмечается, что неалкогольная жировая болезнь печени затрагивает 20–35% взрослого населения в индустриальных странах и имеет серьезные последствия, такие как цирроз и метаболический синдром. В качестве терапевтических средств рассматриваются различные фармакологические препараты и гепатопротекторы, особенно обогащенные соевые фосфолипиды.















![Гепатопротекторные эффекты ФЛ
Алкогольные гепатиты и стеатозы
Положительное действие у пациентов с алкогольным стеатозом:
Восстановление печеночных проб после 12 недельного курса терапии
[U/l] n = 40 [U/l] [U/l]
* *
AST ALT *p ≤ 0.05 γ-GT *p ≤ 0.05
ALT = alanine aminotransferase
AST = aspartate aminotransferase
γ-GT = gamma-glutamyltransferase
1)
Dosage of EPL: 3 g/day
[Adapted from Schüller-Pérez FG and González San Martin F, 1985]](https://image.slidesharecdn.com/02-120413040412-phpapp01/85/02-23-320.jpg)
![Гепатопротекторные эффекты ФЛ
Хронический активный вирусный гепатит
Выраженный положительный эффект у пациентов с вирусным
гепатитом:
ЭФЛ в сочетании с базовым назначением интерферонотерапии улучшали
параметры печени у пациентов с вирусным гепатитом С.
n = 176 IFN = interferon
Patients [%]
* *
71 71
56 51 51
43 42 44
36
*p ≤ 0.05
[Adapted from Niederau Cet al., 1998]](https://image.slidesharecdn.com/02-120413040412-phpapp01/85/02-24-320.jpg)
![Гепатопротекторные эффекты ФЛ
Лекарственное повреждение печени
Уменьшение побочных эффектов со стороны печени у пациентов,
получающих туберкулостатическую терапию:
TBS + placebo TBS + EPL n = 101
AST>35 U/l, and ALT>47 U/l)
25
Number of patients with
20
20
15 *
13
10 *
5 8
4 * p < 0.05 vs.
0 placebo
Patients with drug-induced Patients with drug-induced
AST increase ALT increase
ALT = alanine aminotransferase
AST = aspartate aminotransferase
TBS: tuberculostatic therapy
[Adapted from Marpaung B et al., 1988]](https://image.slidesharecdn.com/02-120413040412-phpapp01/85/02-25-320.jpg)

![Снижение уровня липидов
Улучшение липидных параметров у пациентов с
гиперлипидемией:
Лечение ЭФЛ на протяжении 6 недель привело к снижению изначально
повышенного уровня липидов крови.
[mg/dl] n = 28 [mg/dl] [mg/dl]
Total cholesterol LDL-C Triglycerides
[Modified from Horsch AK et al., 1986]](https://image.slidesharecdn.com/02-120413040412-phpapp01/85/02-27-320.jpg)
![Снижение уровня липидов
Положительный эффект на липидный профиль у пациентов с
сахарным диабетом и вторичной гиперлипидемией.
[mg/dl] n = 30 mg / dl
[mg/dl] Placebo EPL
220
200 204.3
203
303 197
292 289.9 * 285 290 180 291 291
254.5 *
160
158.4
140
120
100
До лечения После 8 недель Через 4 недели
лечения после отмены
*p < 0.05 vs.
Total cholesterol placebo
LDL-C *p < 0.05 vs.
placebo
1)
Dosage of EPL: 2.7 g/day
[Adapted from Kirsten R et al., 1994]](https://image.slidesharecdn.com/02-120413040412-phpapp01/85/02-28-320.jpg)

![Состав фосфолипидов в Энерливе
Фосфатидилхолин : 73-79% (в среднем: 76 %)
Фосфатидилетаноламин: 0-7 %
Фосфатидилиностинол: 0-0.5 %
[Berlin-Chemie AG / Menarini Group; data on file]](https://image.slidesharecdn.com/02-120413040412-phpapp01/85/02-30-320.jpg)