Report
Share
Recommended
Recommended
More Related Content
Featured
Featured (20)
Product Design Trends in 2024 | Teenage Engineerings

Product Design Trends in 2024 | Teenage Engineerings
How Race, Age and Gender Shape Attitudes Towards Mental Health

How Race, Age and Gender Shape Attitudes Towards Mental Health
AI Trends in Creative Operations 2024 by Artwork Flow.pdf

AI Trends in Creative Operations 2024 by Artwork Flow.pdf
Content Methodology: A Best Practices Report (Webinar)

Content Methodology: A Best Practices Report (Webinar)
How to Prepare For a Successful Job Search for 2024

How to Prepare For a Successful Job Search for 2024
Social Media Marketing Trends 2024 // The Global Indie Insights

Social Media Marketing Trends 2024 // The Global Indie Insights
Trends In Paid Search: Navigating The Digital Landscape In 2024

Trends In Paid Search: Navigating The Digital Landscape In 2024
5 Public speaking tips from TED - Visualized summary

5 Public speaking tips from TED - Visualized summary
Google's Just Not That Into You: Understanding Core Updates & Search Intent

Google's Just Not That Into You: Understanding Core Updates & Search Intent
The six step guide to practical project management

The six step guide to practical project management
Beginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...

Beginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...
Yamasaki
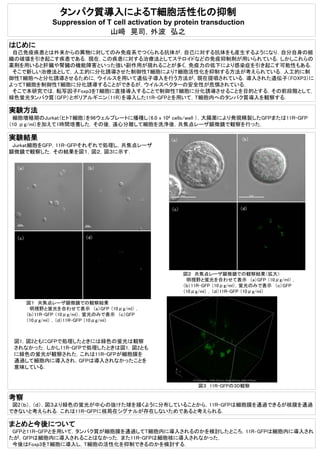
- 1. タンパク質導入によるT細胞活性化の抑制 Suppression of T cell activation by protein transduction 山﨑 晃司,外波 弘之 はじめに 自己免疫疾患とは外来からの異物に対してのみ免疫系でつくられる抗体が,自己に対する抗体をも産生するようになり,自分自身の組 織の破壊を引き起こす疾患である.現在,この疾患に対する治療法としてステロイドなどの免疫抑制剤が用いられている.しかしこれらの 薬剤を用いると肝臓や腎臓の機能障害といった強い副作用が現れることが多く,免疫力の低下により感染症を引き起こす可能性もある. そこで新しい治療法として,人工的に分化誘導させた制御性T細胞によりT細胞活性化を抑制する方法が考えられている.人工的に制 御性T細胞へと分化誘導させるために,ウイルスを用いて遺伝子導入を行う方法が,現在提唱されている.導入された遺伝子(FOXP3)に よってT細胞を制御性T細胞に分化誘導することができるが,ウイルスベクターの安全性が危惧されている. そこで本研究では,転写因子Foxp3をT細胞に直接導入することで制御性T細胞に分化誘導させることを目的とする.その前段階として, 緑色蛍光タンパク質(GFP)とポリアルギニン(11R)を導入した11R-GFPとを用いて,T細胞内へのタンパク質導入を観察する. 実験方法 細胞増殖期のJurkat(ヒトT細胞)を96ウェルプレートに播種し(6.0 x 104 cells/well ),大腸菌により発現精製したGFPまたは11R-GFP (10 μg/ml)を加えて1時間培養した.その後,遠心分離して細胞を洗浄後,共焦点レーザ顕微鏡で観察を行った. 実験結果 Jurkat細胞をGFP,11R-GFPそれぞれで処理し,共焦点レーザ 顕微鏡で観察した.その結果を図1,図2,図3に示す. (a) (b) 図1 共焦点レーザ顕微鏡での観察結果 明視野と蛍光を合わせて表示 (a)GFP (10μg/ml) , (b)11R-GFP (10μg/ml),蛍光のみで表示 (c)GFP (10μg/ml) ,(d)11R-GFP (10μg/ml) (c) (d) 図2 共焦点レーザ顕微鏡での観察結果(拡大) 明視野と蛍光を合わせて表示 (a)GFP (10μg/ml) , (b)11R-GFP (10μg/ml),蛍光のみで表示 (c)GFP (10μg/ml) ,(d)11R-GFP (10μg/ml) 考察 図2(b),(d),図3より緑色の蛍光が中心の抜けた球を描くように分布していることから,11R-GFPは細胞膜を通過できるが核膜を通過 できないと考えられる.これは11R-GFPに核局在シグナルが存在しないためであると考えられる. まとめと今後について GFPと11R-GFPとを用いて,タンパク質が細胞膜を通過してT細胞内に導入されるのかを検討したところ,11R‐GFPは細胞内に導入され たが,GFPは細胞内に導入されることはなかった.また11R-GFPは細胞核に導入されなかった. 今後はFoxp3をT細胞に導入し,T細胞の活性化を抑制できるのかを検討する. (a) 図3 11R-GFPの3D観察 図1,図2ともにGFPで処理したときには緑色の蛍光は観察 されなかった.しかし11R-GFPで処理したときは図1,図2とも に緑色の蛍光が観察された.これは11R-GFPが細胞膜を 通過して細胞内に導入され,GFPは導入されなかったことを 意味している. (b) (c) (d)