205938300 problemas-de-diseno-de-reactores
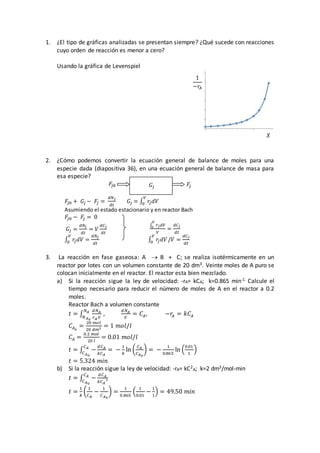
- 1. 1. ¿El tipo de gráficas analizadas se presentan siempre? ¿Qué sucede con reacciones cuyo orden de reacción es menor a cero? Usando la gráfica de Levenspiel 2. ¿Cómo podemos convertir la ecuación general de balance de moles para una especie dada (diapositiva 36), en una ecuación general de balance de masa para esa especie? 𝐹 𝑗0 + 𝐺𝑗 − 𝐹 𝑗 = 𝑑𝑁𝑗 𝑑𝑡 𝐺𝑗 = ∫ 𝑟 𝑗𝑑𝑉 𝑉 0 Asumiendo el estado estacionario y en reactor Bach 𝐹 𝑗0 − 𝐹 𝑗 = 0 ∫ 𝑟𝑗𝑑𝑉 𝑉 0 𝑉 = 𝑑𝐶𝑗 𝑑𝑡 𝐺𝑗 = 𝑑𝑁𝑗 𝑑𝑡 = 𝑉 𝑑𝐶𝑗 𝑑𝑡 ∫ 𝑟 𝑗𝑑𝑉 𝑉 0 = 𝑑𝑁𝑗 𝑑𝑡 ∫ 𝑟 𝑗𝑑𝑉 𝑉 0 /𝑉 = 𝑑𝐶𝑗 𝑑𝑡 3. La reacción en fase gaseosa: A B + C; se realiza isotérmicamente en un reactor por lotes con un volumen constante de 20 dm3. Veinte moles de A puro se colocan inicialmente en el reactor. El reactor esta bien mezclado. a) Si la reacción sigue la ley de velocidad: -rA= kCA; k=0.865 min-1. Calcule el tiempo necesario para reducir el número de moles de A en el reactor a 0.2 moles. Reactor Bach a volumen constante 𝑡 = ∫ 𝑑𝑁𝐴 𝑟𝐴 𝑉 𝑁𝐴 𝑁𝐴0 , 𝑑𝑁𝐴 𝑉 = 𝐶𝐴, −𝑟 𝐴 = 𝑘𝐶𝐴 𝐶𝐴0 = 20 𝑚𝑜𝑙 20 𝑑𝑚3 = 1 𝑚𝑜𝑙/𝑙 𝐶𝐴 = 0.2 𝑚𝑜𝑙 20 𝑙 = 0.01 𝑚𝑜𝑙/𝑙 𝑡 = ∫ − 𝑑𝐶𝐴 𝑘𝐶𝐴 𝐶𝐴 𝐶𝐴0 = − 1 𝑘 ln ( 𝐶𝐴 𝐶𝐴0 ) = − 1 0.865 ln ( 0.01 1 ) 𝑡 = 5.324 𝑚𝑖𝑛 b) Si la reacción sigue la ley de velocidad: -rA= kC2 A; k=2 dm3/mol-min 𝑡 = ∫ − 𝑑𝐶𝐴 𝑘𝐶𝐴 2 𝐶𝐴 𝐶𝐴0 𝑡 = 1 𝑘 ( 1 𝐶𝐴 − 1 𝐶𝐴0 ) = 1 0.865 ( 1 0.01 − 1 1 ) = 49.50 𝑚𝑖𝑛 1 −𝑟 𝐴 𝑋 𝐹 𝑗0 𝐹 𝑗 𝐺𝑗
- 2. c) Si la temperatura es de 127 C, calcule la presión total suponiendo que en la reacción se consume totalmente A. Ecuación general de los gases 𝑃 = 𝑁𝑡 𝑅𝑇 𝑉 Si se consume A totalmente 𝑁𝑡 = 𝑁𝐴 + 𝑁𝐵 + 𝑁𝐶 = 0 + 1 + 1 = 2 𝑚𝑜𝑙 𝑇 = 127 + 273 = 400 𝐾 0 𝑉 = 20 𝑙 𝑃 = (2 𝑚𝑜𝑙)(0.082 𝑙 − 𝑎𝑡𝑚 𝑚𝑜𝑙 − 𝐾 0 20 𝑙 = 3.28 𝑎𝑡𝑚 4. ¿Qué supuestos se hicieron al deducir la ecuación diseño para: a) el reactor por lotes, 𝐹 𝑗0 + 𝐺𝑗 − 𝐹 𝑗 = 𝑑𝑁𝑗 𝑑𝑡 , pero 𝐹 𝑗0 = 𝐹 𝑗 Mezcla Homogénea, volumen constante, no existe flujo de entrada y de salida. La velocidad de reacción es igual en todo el reactor 𝐺𝑗 = 𝑑𝑁𝑗 𝑑𝑡 , la conversión es función del tiempo b) el CSTR, 𝐹 𝑗0 + 𝐺𝑗 − 𝐹 𝑗 = 𝑑𝑁𝑗 𝑑𝑡 , 𝑑𝑁𝑗 𝑑𝑡 = 0 (Estado estacionario), 𝐺𝑗 = 𝑟 𝐴𝑉 𝐹 𝑗0 + 𝑟 𝐴 𝑉 − 𝐹 𝑗 = 0 Mezcla completa, instantánea y homogénea La velocidad de reacción es independiente del tiempo c) el reactor de flujo tapón (PFR) y 𝐹 𝑗0 + 𝐺𝑗 − 𝐹 𝑗 = 𝑑𝑁𝑗 𝑑𝑡 , 𝑑𝑁𝑗 𝑑𝑡 = 0 (Estado estacionario), 𝐹 𝑗0 + ∫ 𝑟 𝑗𝑑𝑉 𝑉 0 − 𝐹 𝑗 = 0 Concentración radial constante; existe variación axial a través del reactor La base de cálculo es el reactivo limitante Los reactantes se consumen a través de la trayectoria del reactor d) el de lecho empacado (PBR)? 𝐹 𝑗0 + 𝐺𝑗 − 𝐹 𝑗 = 𝑑𝑁𝑗 𝑑𝑡 , 𝑑𝑁𝑗 𝑑𝑡 = 0 (Estado estacionario), 𝐹 𝑗0 + ∫ 𝑟 𝐴𝑑𝑊 𝑊 0 − 𝐹 𝑗 = 0 Se expresa en peso; el lecho actúa como catalizador para la transferencia de masa, sistema no homogéneo 5. La reacción no elemental irreversible, en fase gaseosa: A+2B → C Se llevará a cabo isotérmicamente en un reactor por lotes a presión constante. La alimentación está a una temperatura de 227 ºC, una presión de 1013 kPa y su composición es 33.3% de A y 66.7% de B. Se obtuvieron los siguientes datos de laboratorio en condiciones idénticas. -rA (mol/dm3.s )x103 0.010 0.005 0.002 0.001 X 0.0 0.2 0.4 0.6 (1/--rA) 0.1 0.2 0.5 1.0 a. Estime el volumen del reactor de flujo tapón (PFR) requerido para alcanzar una conversión de 30% de A para una velocidad de flujo volumétrico de 2 m3/min. 𝑁𝐴 𝑉 = 𝑃 𝑅𝑇 𝐹𝐴0 = 1013𝑘𝑝𝑎 101 .3𝑘𝑝𝑎 𝑥 1𝑎𝑡𝑚 0.082 𝑙−𝑎𝑡𝑚 𝑚𝑜𝑙−º𝐾 𝑥 (227+273)º𝐾 𝑥 2 𝑚3 𝑠 𝑥 1000 𝑙 𝑚3 𝑥 60 𝑠 𝑚𝑖𝑛 = 3.38 𝑚𝑜𝑙/𝑚𝑖𝑛
- 3. X 0.0 0.2 0.4 0.6 (1/--rA) 0.1 0.2 0.5 1.0 𝑉 = 𝐹𝐴0 ∫ 𝑑𝑋 −𝑟𝐴 𝑋 0 ∫ 𝑑𝑋 −𝑟𝐴 𝑋 0 = ∆𝑋 3 ( 1 −𝑟𝐴 (𝑋=0) + 4 −𝑟𝐴 (𝑋1) + 2 −𝑟𝐴 (𝑋2) + 1 −𝑟𝐴(𝑋3) ) ∫ 𝑑𝑋 −𝑟𝐴 𝑋 0 = 0.2 3 (1 ∗ 0.1 + 4 ∗ 0.2 + 2 ∗ 0.5 + 1 ∗ 1) = 193x10-3 𝑉 = 𝐹𝐴0 ∫ 𝑑𝑋 −𝑟𝐴 𝑋 0 = 3.38 𝑚𝑜𝑙 𝑚𝑖𝑛 𝑥 193𝑥10−3 = 0.6523 dm3 b. Estime el volumen de un CSTR requerido para recibir el efluente de PFR anterior y alcanzar una conversión total de 50% (con base en la especie A alimentada al PFR) 𝑉𝑃𝐹𝑅 = 𝐹𝐴0 𝐴𝑟𝑒𝑎 = 3.38 𝑚𝑜𝑙 𝑚𝑖𝑛 𝑥 0.3 = 1.014 𝑑𝑚3 c. ¿Qué volumen total tienen los dos reactores? 𝑉𝑇𝑜𝑡𝑎𝑙 = 0.652 + 1.014 = 1.666 𝑑𝑚3 d. ¿Qué volumen tiene un solo PFR necesario para alcanzar una conversión de 60%? ¿De 80%? e. ¿Qué volumen tiene un solo CSTR necesario para alcanzar una conversión de 50%? f. ¿Qué volumen tendría que tener un segundo CSTR para elevar la conversión de 50% a 60%. g. Grafique la velocidad de reacción y la conversión en función del volumen de PFR
- 4. h. Analice críticamente las respuestas a este problema 6. Considerar la isomerización del cis-trans 2-buteno en fase líquida, la cual se puede escribir simbólicamente como AB. La reacción de primer orden (-rA=kCA) se lleva acabo en un reactor tubular con una velocidad de flujo volumétrico constante, v, ejemplo, v=v0. a) Grafique el perfil de la concentración. b) Derive una ecuación para el reactor que relacione el volumen del reactor, la concentración de A de entrada y salida, la constante de velocidad, k y la velocidad del flujo volumétrico v. c) Determinar el volumen del reactor necesario para reducir la concentración hasta el 10% de la concentración inicial cuando la velocidad de flujo volumétrico es 10 dm3/min y constante especifica de velocidad es 0.23 min-1. 7. La reacción AB cuyos resultados se muestran en la tabla se lleva a cabo en un reactor CSTR. Las especies A entran al reactor con una velocidad de flujo molar de 0.4 mol/s. a) Calcule el volumen necesario del reactor para obtener una conversión del 80% en un reactor CSTR. Datos del problema X 0.0 .01 0.2 0.3 0.4 0.6 0.8 −𝑟 𝐴 ( 𝑚𝑜𝑙 𝑚3 ∙ 𝑠 ) 0.45 0.37 0.30 0.195 0.113 0.079 0.05 (1 −𝑟 𝐴 ⁄ ) ( 𝑚3 ∙ 𝑠 𝑚𝑜𝑙 ) 2.22 2.70 3.33 5.13 8.85 12.7 20 8. Las mediciones de laboratorio que se dan en la tabla, muestran la velocidad de reacción en función de la conversión. La temperatura fue de 300 ºF (422.2 K), la presión total fue de 10 atm (1013 kPa) y la carga inicial fue una mezcla equimolar de A e inertes. El flujo de entrada es vo = 6 dm3/s X -rA (mol/dm3·s) 0.0 0.00530 0.1 0.00520 0.2 0.00500 0.3 0.00450 0.4 0.00400 0.5 0.00330 0.6 0.00250 0.7 0.00180 0.8 0.00125
- 5. 0.85 0.00100 a) Trazar una gráfica de la conversión y la velocidad de reacción. b) Calcule el volumen necesario para alcanzar una conversión de 80% en un CSTR. c) Sombree en la figura el área que, al multiplicarse por FA0, daría el volumen de un CSTR necesario para lograr una conversión de 80%. 9. La reacción descrita en la tabla anterior, se llevará a cabo en un PFR. La velocidad de flujo molar entrante es de 0.867 mol/s. a) Trazar una gráfica de la conversión, X, y la velocidad de reacción, -rA, a lo largo del volumen del reactor. b) Calcule el volumen de reactor necesario para lograr una conversión de 80% en un PFR. c) Sombrear el área que al multiplicarse por FA0 dará el volumen del PFR. 10. La reacción exotérmica: A B + C, se lleva a cabo adiabáticamente y se obtuvieron los siguientes datos: X 0 0.2 0.4 0.45 0.5 0.6 0.8 0.9 -rA, mol/dm3- min 1.0 1.67 5.0 5.0 5.0 5.0 1.25 0.91 a) La velocidad de flujo molar de alimentación fue de 300 mol/min. b) ¿Cuáles son los volúmenes necesarios de un PFR y un CSTR para obtener una conversión del 40% de conversión? c) ¿En qué rango de conversión los volúmenes del CSTR y PFR son iguales? d) ¿Cuál es la máxima conversión que se puede obtener en un CSTR de 10.5 dm3? e) ¿Cuál es la máxima conversión que se puede obtener en un PFR de 72 dm3 conectado en serie con un CSTR de 24 dm3? f) ¿Cuál es la máxima conversión que se puede obtener en un CSTR de 24 dm3 conectado en serie con un PFR de 72 dm3? g) Grafique la velocidad de reacción en función de la conversión de un reactor PFR de 100 dm3? 11. Para los datos mostrados abajo como podría arreglar los tanques de 4 litros CSTR y un litro PFR para maximizar la conversión? Sí, el FA0 = 1000 mol/día. Las unidades son mol/L-min. Determinar la conversión intermedia y la conversión final en cada caso.
- 6. X 1 −𝑟 𝐴 0.0 1.07 0.07 1.23 1.23 1.5 0.23 1.8 0.31 2.24 0.389 2.86 0.452 3.55 0.52 4.65 0.6 6.67 0.67 9.76 0.74 15.8 0.79 24.1 12. Diseñe el mínimo volumen del reactor para obtener un 80% de conversión, si la reacción en el reactor tiene la siguiente cinética: 𝑟 𝐴 = − 0.0005 1−0.3𝑋+0.55𝑥2 𝑚𝑜𝑙 𝐿−𝑠 𝐹𝑆0 = 1 𝑚𝑜𝑙 𝑠