Tema 4 Diagramas I 2024 Uvigo Ciencia Materiales
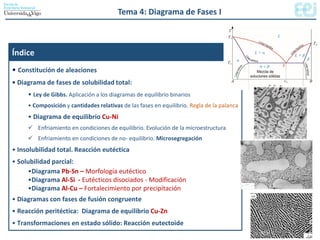
- 1. Tema 4: Diagrama de Fases I Índice • Constitución de aleaciones • Diagrama de fases de solubilidad total: • Ley de Gibbs. Aplicación a los diagramas de equilibrio binarios • Composición y cantidades relativas de las fases en equilibrio. Regla de la palanca • Diagrama de equilibrio Cu-Ni Enfriamiento en condiciones de equilibrio. Evolución de la microestructura Enfriamiento en condiciones de no- equilibrio. Microsegregación • Insolubilidad total. Reacción eutéctica • Solubilidad parcial: •Diagrama Pb-Sn – Morfología eutéctico •Diagrama Al-Si - Eutécticos disociados - Modificación •Diagrama Al-Cu – Fortalecimiento por precipitación • Diagramas con fases de fusión congruente • Reacción peritéctica: Diagrama de equilibrio Cu-Zn • Transformaciones en estado sólido: Reacción eutectoide
- 2. Constitución de aleaciones Conceptos básicos Aleación Metálica: Mezcla de un metal y otros elementos químicos metálicos y/o no metálicos (solutos). Puede ser una solución sólida o una mezcla de dos o más fases. Siempre tiene propiedades metálicas. Límite de solubilidad: En una solución sólida es la máxima concentración de átomos de soluto que puede disolverse. Superar el límite de solubilidad implica la formación de otra solución sólida o de un compuesto. 2 Un sistema de aleación contiene todas las aleaciones que se pueden formar combinando varios elementos en todas las proporciones posibles; dos: binario; tres: ternario... Compuesto: Se forma por afinidad química entre los elementos: proporciones definidas, red cristalina propia, enlace iónico o covalente. suelen presentar altos puntos de fusión, elevada dureza y resistencia, y pueden ser frágiles
- 3. Constitución de aleaciones Conceptos básicos Componentes de una aleación: Especies químicas que la forman: Elementos o compuestos Fase: Porción homogénea de un sistema que tiene características físicas y químicas uniformes. Fases posibles en estado sólido metálico: metal puro, compuesto y solución sólida 3 1 componente: H2O 3 pases: agua líquida, hielo y vapor 5 componentes: Fe, Ni, Cr, Mo, C 2 pases: amarilla (α) y blanca (γ) Constituyentes de una aleación: cada una de las fases o agregados de fases microscópicamente diferentes que tienen características propias, que forman la aleación
- 4. Ejemplo 1: postres Componentes: agua leche, azúcar, harina. Fases: flan, galleta, puding, caramelo Constituentes: Monofásicos: flan, galleta, puding, caramelo Bifásicos: tarta de la abuela (agregado) 4 Ejemplo 2: patrones Componentes: pintura blanca y pintura negra. Fases: blanco, negro Constituentes: Monofásicos: blanco y negro Bifásicos: cebra, dálmata, geométrico……
- 5. ALEACIONES METÁLICAS HOMOGÉNEAS Monofásicas De metales puros De soluciones sólidas HETEROGÉNEAS Polifásicas De metales puros De compuestos De soluciones sólidas Clasificación 5 Constitución de aleaciones
- 6. Diagrama de fases de equilibrio Representación gráfica de las fases que están presentes en equilibrio en un sistema binario en función de la temperatura y la composición. Solidificación en equilibrio Enfriamiento muy lento Se determinan a partir de datos experimentales de A en B de B en A 6 Conocer las fases presentes en función de la Temperatura y composición. Determinar la Temperatura de inicio y final de la solidificación. Determinar la Temperatura de comienzo de la fusión. Conocer la solubilidad de los componentes. Predecir la microestructura de la aleación a temperatura ambiente. Utilidades
- 7. PROPORCIÓN DEL SOLUTO TERMINAL Con límite de solubilidad Fases terminales INTERMEDIA Intervalo de solubilidad (mínimo –máximo) Fases intermedias A B α A B α δ de A en B de B en A SERIE CONTINUA Solubilidad total 1 Solución Sólida 7 Constitución de aleaciones INSOLUBILIDAD Afinidad eutéctica Agregado eutéctico
- 8. Cu TS Cu: 1085ºC Liq Liq + sol sol TSNi: 1453ºC Ni Liq Liq + sol sol Liq Liq + α α 60Cu- 40Ni tiempo Composición ( % peso Ni) Temperatura (ºC) Línea de líquidus Líquido, L Línea de sólidus Solución sólida, α Diagrama de equilibrio Cu-Ni Curvas de enfriamiento Línea sólidus T de servicio Línea líquidus procesado por moldeo L + α Diagrama de fases de solubilidad total 8 Cuanto menor sea el interval de solidificación⇒ Mejor capacidad de moldeo
- 9. Grados de libertad (L): Número de variables deben fijarse para que el sistema se encuentre en un estado unívocamente definido F + L= C + 2 Para un sistema en equilibrio puede establecerse la siguiente relación entre el número de fases (F), el número de componentes del sistema (C), y los grados de libertad (L): En particular, para un sistema en equilibrio a presión constante: F= 2 L=1 Equilibrio monovariante L=2 Equilibrio bivariante Para sistemas binarios, C=2 L = 3- F F + L = C + 1 Ley de Gibbs. Aplicación a los diagramas de equilibrio binarios 9 L (1 fase) α (1 fase)
- 10. Composición (% peso Ni) Temperatura (ºC) Línea de vínculo Líquido To Co Cantidades relativas de las fases en equilibrio Una aleación de composición: Co(%Ni) a Temperatura To El trazado de la línea de vínculo permite obtener la composición de las fases en equilibrio (CL y C α) Solución sólida α Líquido % L = 100 (Cα-Co) / (Cα-CL) % α = 100 - % L Composición y cantidades relativas de las fases en equilibrio Regla de la palanca 10 29% Ni 35% Ni 39,5% Ni
- 11. Temperatura (ºC) Composición (% peso Ni) Evolución de la microestructura de equilibrio de una aleación Cu-Ni del 35% de Ni Situación ideal: Velocidad de enfriamiento muy lenta para permitir la difusión del Cu y Ni En ocasiones se consigue con moldeo en arena Estructura a T ambiente: Granos de composición homogénea 35%Ni → microconstituyente monofásico Enfriamiento en condiciones de equilibrio. Evolución de la microestructura 11 b c d e
- 12. Difusión rápida en líquido ⇓ Difusión lenta en sólido ⇓ La composición del sólido depende de la velocidad de solidificación ⇓ Se establece un gradiente de concentraciones, siendo el centro de los granos rico en el componente de mayor Tm ⇓ MICROSEGREGACIÓN Composición no uniforme producida por la solidificación fuera del equilibrio Fotomicrografía de una aleación 85Cu-Ni (100x) Consecuencias: Si se produce recalentamiento, el borde de grano funde antes (rico en componente menor Tm) ⇒ fallo mecánico prematuro Enfriamiento fuera de las condiciones de equilibrio. Microsegregación 12 Enriquecida en el componente de menor Tm Micrografía de aleación Cu-4,5%P (100x) Enriquecido en compontente de mayor Tm Gradientes de composición a través de los granos ESTRUCTURA SEGREGADA
- 13. ELIMINACIÓN MICROSEGREGACIÓN: Recocido de homogenización Aleación (Cu-4% Sn) 75x Estructura bruta de solidificación Moldeo en arena Misma probeta tras ser sometida al Tratamiento térmico Enfriamiento fuera de las condiciones de equilibrio MACROSEGREGACIÓN Heterogeneidad en la composición entre las distintas partes del sólido ej. La superficie y su interior de una pieza SOLUCIÓN: Procesado en caliente 13 microrrechupes
- 14. Variación de la resistencia mecánica y la ductilidad en función de la composición en el sistema Cu-Ni a Tambiente Características de los cuproníqueles: Excelente resistencia a la corrosión “Antifouling” Fácil manufactura Cuproníqueles Alargamiento ∆L (%) Composición (% peso Ni) Composición (% peso Ni) Resistencia a la tracción, Rm (Mpa) Monel Aplicaciones: Intercambiadores de calor Bombas Válvulas Industria Química 14
- 15. Tema 4: Diagrama de Fases I Índice • Constitución de aleaciones • Diagrama de fases de solubilidad total: • Ley de Gibbs. Aplicación a los diagramas de equilibrio binarios • Composición y cantidades relativas de las fases en equilibrio. Regla de la palanca • Diagrama de equilibrio Cu-Ni Enfriamiento en condiciones de equilibrio. Evolución de la microestructura Enfriamiento en condiciones de no- equilibrio. Microsegregación • Insolubilidad total. Reacción eutéctica • Solubilidad parcial: •Diagrama Pb-Sn – Morfología eutéctico •Diagrama Al-Si - Eutécticos disociados - Modificación •Diagrama Al-Cu – Fortalecimiento por precipitación • Diagramas con fases de fusión congruente • Reacción peritéctica: Diagrama de equilibrio Cu-Zn • Transformaciones en estado sólido: Reacción eutectoide
- 16. Reacción eutéctica: L ( CE % B) A (0%B) + B (100%B) TE Insolubilidad total. Reacción eutéctica 16 Mezcla eutéctica
- 17. Temperatura (ºC) Composición (% peso Sn) Temperatura (ºF) Pb Sn Reacción eutéctica: L ( 61.9%Sn) α (18.3%Sn) + β (97.8%Sn) Mezcla eutéctica = agregado eutéctico Diagrama de equilibrio Pb-Sn Solubilidad parcial en estado sólido 17 Línea Sólidus Línea Líquidus Línea de solvus Línea de solvus
- 18. L ( 61.9%Sn) α (18.3%Sn) + β (97.8%Sn) Diagrama de equilibrio Pb-Sn Temperatura ( o C) Composición (% peso Sn) 18 Mezcla eutéctica = agregado eutéctico Solidificación incongruente
- 19. Espaciado interlaminar, λ λ↓ ⇒ Venfr ↑ ⇒ ts ↓ λ↓ ⇒ área interfase↑ ⇒ resistencia↑ Líquido Dirección de crecimiento Aumento de la resistencia de la aleación por formación del eutéctico Formación del agregado eutéctico por difusión de Pb y Sn λ Diagrama de equilibrio Pb-Sn 19 CONSTITUYENTE EUTÉCTICO A menor espaciado interlaminar mayor resistencia
- 20. Temperatura (ºC) Composición (% peso Sn) Solución sólida α Solución sólida β % α = 100 (Q+R) / (P+Q+R) % β = 100 P / (P+Q+R) Cantidades relativas de las fases en la mezcla eutéctica Cantidades relativas de fases a T=182 ºC % α (αproE + αE) 20
- 21. Diagrama de equilibrio Pb-Sn 21 Aleaciones hipoeutécticas Composición (% peso Sn) Temperatura (ºC)
- 22. % E = 100 P / (P+Q) % αp= 100 Q / (P+Q) Mezcla eutéctica. CONST MATRIZ Determina las propiedades del material Constituyente primario o proeutéctico CONST. DISPERSO Cálculo de los constituyentes relativos Temperatura (ºC) Composición (% peso Sn) Cantidades relativas de constituyentes a Tª 182 ºC Consideraremos la misma cantidad a Tª ambiente 22
- 23. 23 Microconstituyentes Para describir las microestructuras, es conveniente usar el término microconstituyente Fase ≠ microconstituyente Microconstituyentes: Elementos de la microestructura con una estructura característica e identificable. Los eutécticos se consideran un solo microconstituyente Eutéctico: agregado bifásico que normalmente presentan estructura laminar Microconstituyente Matriz: Microconstituyente continuo, determina en mayor medida las propiedades del material. Microconstituyente Disperso: Condiciona las propiedades. Fases 2 2 2 Microconstituyentes: 2 1 2 Ejemplo: Diagrama de equilibrio Pb-Sn Aleaciones Bifásicas Matriz eutéctica Presencia de Eutéctico Aleaciones hipoeutécticas Al. hipereutécticas Aleación eutéctica
- 24. 11-4 The Eutectic Phase Diagram- Askeland Efecto del % de agregado eutéctico en las propiedades mecánicas 24
- 25. Materiales empleados en soldadura blanda Componentes electrónicos: 62 Sn + 38 Pb (TS=183ºC) Fontanería (tubería de cobre): 50 Sn + 50 Pb (∆TS: 183-212ºC) Alta temperatura: 5 Sn + 1,5 Ag + 93,5 Pb (∆TS: 296-301ºC) Diagrama de equilibrio Pb-Sn. APLICACIONES Pb Sn Temperatura (ºC) Composición (% peso Sn) Temperatura (ºF) 25 Composición (% atómico Sn)
- 26. Composición (% peso Si) Si L L + Si L + α α + Si 577ºC 1414ºC E Un eutéctico se denomina “anormal” (disociado) cuando las fases que la forman difieren notablemente en sus temperaturas de fusión y en sus cantidades relativas TS Al: 660ºC TS Si: 1414ºC Temperaturas de fusión: % de fases en la mezcla eutéctica: % α: 88,9% % Si: 11,1% Cinética de solidificación del Si mucho más rápida Al Temperatura (ºC) 200 400 600 800 1000 1200 1400 1600 660ºC α 1,6 12,6 Diagrama de equilibrio Al-Si. Eutécticos anormales o disociados La microestructura no es laminar 26
- 27. Hypoeutectic Eutectic Hypereutectic 27 Eutécticos anormales, disociados o irregulares. Sistema Al-Si: SILUMINIOS
- 28. Las morfologías angulosas producen concentración de tensiones, favoreciendo la rotura Cristales aciculares de silicio Baja tenacidad Aladar Pacz (1920) Adición de pequeñas cantidades de Na antes de colar (0,02%) Modificación de siluminios El Na produce subenfriamiento y desplaza la composición de la eutéctica hasta el 14% de Si el Si solidifica como formas redondeadas e interconectadas entre los brazos dendríticos del Al Siluminios modificados 28
- 29. Aleación hipoeutéctica Estructura más fina y redondeada Menor efecto de entalla Mayor tenacidad (microscopio metalográfico) Sin modificar (microscopio electrónico) Modificado Morfología de los cristales de silicio (SEM) Siluminios modificados Estructura del siluminio modificado Al-12Si-0.02Na αproE E modificado 29
- 30. 30
- 31. Tema 4: Diagrama de Fases I Índice • Constitución de aleaciones • Diagrama de fases de solubilidad total: • Ley de Gibbs. Aplicación a los diagramas de equilibrio binarios • Composición y cantidades relativas de las fases en equilibrio. Regla de la palanca • Diagrama de equilibrio Cu-Ni Enfriamiento en condiciones de equilibrio. Evolución de la microestructura Enfriamiento en condiciones de no- equilibrio. Microsegregación • Insolubilidad total. Reacción eutéctica • Solubilidad parcial: •Diagrama Pb-Sn – Morfología eutéctico •Diagrama Al-Si - Eutécticos disociados - Modificación •Diagrama Al-Cu – Fortalecimiento por precipitación • Diagramas con fases de fusión congruente • Reacción peritéctica: Diagrama de equilibrio Cu-Zn • Transformaciones en estado sólido: Reacción eutectoide
- 32. • Basic Concepts • Isomorphous phase diagrams (complete solubility) Cooling curve. Gibbs phase rule Lever rule: Determination of phase amounts Development of microstructure-Equilibrium cooling Non equilibrium cooling – Microsegregation: coring Copper-Nickel alloys. Solid solution strengthening • Insolubility in the solid state: Eutectic phase diagrams • Partial solubility: Pb-Sn Diagram: eutectic morphology Al-Si Diagram: irregular eutectics. Modification Al-Cu Diagram: precipitation strengthening • Congruent phase transformations • Peritectic reaction: Cu-Zn diagram • Solid state transformations Allotropic transformations Eutectoid transformation Contents Lesson 4: Binary Phase diagrams (I) 32
- 33. Endurecimiento por precipitación. Aleaciones bifásicas: Al-Cu 600 T ºC 700 500 0 10 20 30 40 33,2 5,65 Teutéctica 548 ºC TS AL= 660 ºC % en peso de Cu E αs L α L + α L + θ (Al2Cu) α + θ 400 300 540 4,5 L (33,2 %Cu) α (5,65 %Cu) + θ (50%Cu) El endurecimiento por precipitación se basa en dificultar el avance de las dislocaciones mediante la generación de una dispersión muy fina de precipitados en la microestructura del material. Para aplicar este tratamiento térmico el diagrama debe mostrar solubilidad sólida parcial. Aplicaciones: Ampliamente utilizado en Aeronáutica por su elevada resistencia especifica (R/d) DURALUMINIOS Al-4%Cu Solubilidad parcial + fase intermedia Diagrama Al-Cu 33 Solidificación incongruente Descubierto por Alfred Wilm en el Dürener Metallwerke AG, en 1903
- 34. θ Al2Cu (θ) precipitado de equilibrio 34 Liq + α Liq α α + θ T tiempo Tamb ⇒ Precipitado incoherente con la matriz ⇒ Precipitado duro… pero… • Poco endurecimiento ← poco % de fase secundaria • Fragilización de límites de grano Diagrama Al-Cu Enfriamiento de equilibrio
- 35. Fase de equilibrio Al2Cu (θ): tetragonal e incoherente con la matriz (no existe relación entre las estructuras cristalinas) Estructuras de transición coherente con la matriz (existen relaciones cristalinas con la matriz). La formación de estas zonas conduce a una importante distorsión de la red Fortalecimiento de la aleación. Distorsión máxima: Zonas de Guinier Preston (Zonas G-P) Precipitados Coherentes e Incoherentes Endurecimiento por precipitación Age hardening 35
- 36. 1.- Matriz dúctil y blanda + precipitado resistente y duro ⇒ freno a las dislocaciones 2.- Matriz continua y precipitado discontinuo 3.- Partículas pequeñas y numerosas incrementan la interferencia 4.- La resistencia de la aleación aumenta con el contenido de precipitado 5.- Las partículas redondeadas no actúan como concentradores de tensiones ⇒ no fragilizan Endurecimiento por precipitación: Consideraciones generales 36
- 37. 1 2 3 Temple Solución sólida sobresaturada Maduración Artificial/natural Etapas del tratamiento térmico de endurecimiento por precipitación Bonificado = Hipertemple + Maduración T t θ Microestructura inicial T-t θ 37 Solución sólida Precipitación
- 38. Curvas de maduración (TEM x 60.000) Fina dispersion de partículas no visible al microscopio óptico (Endurecimiento estructural ) Fortalecimiento más efectivo También llamado fortalecimiento por maduración o por envejecimiento Las aleaciones de aluminio de mayor resistencia (series: 2xxx, 6xxx y 7xxx) se producen por este mecanismo de fortalecimiento Sobremadurado 38 GP zones Máx dureza S.S.S. S.S.S.
- 39. 39
- 40. Tema 4: Diagrama de Fases I Índice • Constitución de aleaciones • Diagrama de fases de solubilidad total: • Ley de Gibbs. Aplicación a los diagramas de equilibrio binarios • Composición y cantidades relativas de las fases en equilibrio. Regla de la palanca • Diagrama de equilibrio Cu-Ni Enfriamiento en condiciones de equilibrio. Evolución de la microestructura Enfriamiento en condiciones de no- equilibrio. Microsegregación • Insolubilidad total. Reacción eutéctica • Solubilidad parcial: •Diagrama Pb-Sn – Morfología eutéctico •Diagrama Al-Si - Eutécticos disociados - Modificación •Diagrama Al-Cu – Fortalecimiento por precipitación • Diagramas con fases de fusión congruente • Reacción peritéctica: Diagrama de equilibrio Cu-Zn • Transformaciones en estado sólido: Reacción eutectoide
- 41. Temperatura (ºC) Composición (% peso Pb) Mg Pb Las fases intermedias pueden tratarse como otro componente en el diagrama. El diagrama puede simplificarse estudiando las diferentes regiones por separado Solubilidad parcial en estado sólido: Diagramas con fases de fusión congruente Diagrama de equilibrio Mg- Pb Composición (peso Li) Temperatura (ºK) Al Li Mg2Pb Congruente y estequiométrico AlLi Congruente y no-estequiométrico Línea vertical en el diagrama Región delimitada por máximo y mínimo de solubilidad Diagrama de equilibrio Al-Li 41
- 42. 42 Reacción peritéctica β →Incongruente y no-estequiométrica Reacción peritéctica: L ( CL %B) + α (Cα %B) β (CP %B) TP Solidificación condiciones de equilibrio Pt Ag
- 43. 43 Reacción peritéctica Solidificación en condiciones de equilibrio Todo el líquido reacciona con toda la fase sólida α para producir la fase sólida β β L α β α L Solidificación en condiciones fuera de equilibrio Enfriamientos rápidos ⇓ Difusión atómica más lenta ⇓ Transformación incompleta ⇓ Fase α no desaparecerá, quedará rodeada por la fase β Encapsulamiento o cercado de la fase α β L α α L β α Aleaciones peritécticas Peligro de microsegregación
- 44. Diagrama de equilibrio Cu-Zn Temperatura (ºC) Cu Composición (% peso Zn) Zn α β α+β 44 Fases intermedias = β, γ, δ, ε Incongruentes y no-estequiométricas
- 45. Aleaciones Cu-Zn. LATONES. Características y aplicaciones 45 Latón 70/30, de cartuchería
- 46. 46 Reacción eutectoide Composición (% atómico de Zn) Transformación en estado sólido. A Te hay tres fases solidas en equilibrio Te δ γ ε e Líquido Cγ Te Cε Cδ Te Reacción eutectoide: δ (Cδ %Zn) γ (Cγ %Zn) + ε (Cε%Zn) Continuará Tema 4-II
- 47. 47 Bibliografía Shackelford, James F, Introducción a la ciencia de materiales para ingenieros, 7ª, Pearson Educación, 2010 Montes J.M., Cuevas F.G., Cintas J., Ciencia e ingeniería de los materiales, 1ª, Paraninfo, 2014 1) Callister W.D., “Introducción a la Ciencia e Ingeniería de los Materiales”, Ed Reverté, S.A. (2016). Capítulo 11. Diagramas de fases 2) Donald R. Askeland, “Ciencia e ingeniería de los materiales” 7ª ed. Ed. Cengage Learning (2017) Capítulo 10: Soluciones sólidas y equilibrio de fases