More Related Content
PDF
PDF
PPT
PPT
Adición electrofílica a alquenos y alquinos PPTX
Clase 7-marcha del grupo 2 PPTX
Reacciones de precipitacion PPTX
Clase 11-cationes del grupo 4 PPTX
What's hot
PPT
Reacciones De DescomposicióN PPTX
Lista de cationes y aniones comunes PDF
Marcha analitica de cationes para grupo i PPT
Tablas de compuestos ionicos PPTX
PPTX
PPT
Clase de reacciones químicas PDF
PPTX
PPTX
PPT
DOC
Nomenclatura química de los compuestos inorgánicos2 PPTX
Clase 12 marcha analitica de los cationes del grupo iv PPTX
Clase 14 marcha analitica de los cationes del grupo v PPT
T6. Ácido Base Hidrolisis Sal de ácido débil y base débil PPTX
Clase 13 cationes del grupo v PDF
Problemas de electroquimica pv DOC
DOCX
Práctica#8 Intercambio de Anhídridos DOCX
Obtención de Cloruro de t-butilo More from Hermis Quispe
PPT
PPTX
Intercambiadores de calor PDF
PDF
PDF
PDF
DOCX
PDF
PDF
10 cultura organizacional PDF
PDF
Sistemas homogeneos gradodedisociacion[1] PDF
Sistemas homogeneos gradodedisociacion[1] PDF
PDF
PDF
P rroblemas hidrolisis[2] PDF
Msa iy ii-grupos
- 1.
UNIVERSIDAD NACIONAL DELCALLAO
FACULTAD DE INGENIERÍA QUÍMICA
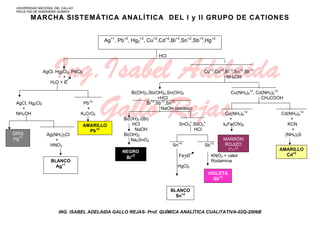
MARCHA SISTEMÁTICA ANALÍTICA DEL I y II GRUPO DE CATIONES
Ag+1, Pb+2, Hg2+2, Cu+2,Cd+2,Bi+3,Sn+2,Sb+3,Hg+2
Ag+1, Pb+2, Hg2+2, Cu+2,Cd+2,Bi+3,Sn+2,Sb+3
HCl
AgCl, Hg2Cl2, PbCl2 Cu+2,Cd+2,Bi+3,Sn+2,Sb+3
+ NH4OH
H2O + C
Bi(OH)3,Sb(OH)3,Sn(OH)2 Cu(NH3)4+2, Cd(NH3)4+2
+HCl CH3COOH
AgCl, Hg2Cl2 Pb+2 Bi+3,Sb+3,Sn+2
+ + NaOH (exceso)
NH4OH K2CrO4 Cu(NH3)4+2 Cd(NH3)4+2
Bi(OH)3 /(Bi) + +
AMARILLO HCl SnO3=,SbO2= k4Fe(CN)6 KCN
Pb+2 NaOH HCl +
GRIS Ag(NH3)2Cl Bi(OH)3 (NH4)2S
Hg+2 + Na2SnO2 MARRÓN
+4 +3 ROJIZO
HNO3 Sn Sb
NEGRO Cu+2 AMARILLO
3 Fe+C KNO2 + calor Cd+2
Bi+
BLANCO Rodamina
Ag+1 HgCl2
VIOLETA
Sb+3
BLANCO
Sn+2
ING. ISABEL ADELAIDA GALLO REJAS- Prof. QUÍMICA ANALÍTICA CUALITATIVA-02Q-2006B