สรุปGassolidliquid
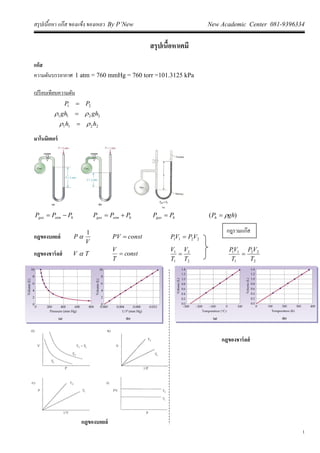
- 1. สรุปเนื้อหา แก๊ส ของแข็ง ของเหลว By P’New New Academic Center 081-9396334 1 สรุปเนื้อหาเคมี แก็ส ความดันบรรยากาศ 1 atm = 760 mmHg = 760 torr =101.3125 kPa เปรียบเทียบความดัน 21 PP 2211 ghgh 2211 hh มาโนมิเตอร์ hatmgas PPP hatmgas PPP hgas PP )( ghPh กฎของบอยล์ V P 1 constPV 2211 VPVP กฎของชาร์ลส์ TV const T V 2 2 1 1 T V T V 2 22 1 11 T VP T VP กฎรวมแก๊ส กฎของบอยล์ กฎของชาร์ลส์
- 2. สรุปเนื้อหา แก๊ส ของแข็ง ของเหลว By P’New New Academic Center 081-9396334 2 กฎเกย์ลุสแซก TP const T P 2 2 1 1 T P T P กฎอะโวกาโดร nV const n V 2 2 1 1 n V n V สมการแก๊สอุดมคติ nRTPV ความหนาแน่น RT PM V nM d ความดันย่อย tt t PXP n n P 1 1 1 tt t PXP n n P 2 2 2 กฎการแพร่ของ Graham 2/1 2 2/1 1 2 1 1 2 1 2 2 1 )/3( )/3( )( )( MRT MRT v v d d M M r r rms rms ของเหลว 1. แรงยึดเหนี่ยวระหว่างโมเลกุล(Intermolecular Forces) 1) แรงแวนเดอร์วาลส์ (Van der Waal Forces) เกิดจากการเหนี่ยวนา แรงขั้วคู่-ขั้วคู่ (dipole-dipole forces) แรงแผ่กระจาย (dispersion forces) แรงขั้วคู่-ขั้วคู่เหนี่ยวนา (dipole-induced dipole forces) แรงไอออน-ขั้วคู่เหนี่ยวนา (ion-induced dipole forces) 2) แรงไฟฟ้าสถิตย์(Electrostatic Forces) -- ion-dipole force (แรงไอออน-ขั้วคู่) 3) H-bond (พันธะไฮโดรเจน) – แรงขั้วคู่-ขั้วคู่ (dipole-dipole force) มี F-H, N-H, O-H 2. แรงยึดเหนี่ยวภายในโมเลกุล (Intramolecular Forces) 1) พันธะไอออนิก (Ionic Bond) โลหะ + อโลหะ 2) พันธะโควาเลนต์ (Covalent Bond) อโลหะ + อโลหะ 3) พันธะโลหะ (Metallic Bond) โลหะ + โลหะ แรงยึดเหนี่ยวระหว่างโมเลกุล < แรงยึดเหนี่ยวภายในโมเลกุล P1 + P2 = Pt Real gas จะมีพฤติกรรม เข้าใกล้ideal gas ที่ T สูง P ต่า
- 3. สรุปเนื้อหา แก๊ส ของแข็ง ของเหลว By P’New New Academic Center 081-9396334 3 แรงระหว่างโมเลกุลน้อย - แรงตึงผิวน้อย - ความดันไอมาก - จุดเดือดจุดหลอมเหลวต่า ของแข็ง ชนิดของของแข็ง ผลึกของแข็ง (Crystalline solid) ของแข็งอสัณฐาณ (Amorphous Solid) มีรูปทรงเรขาคณิตแน่นอน ไม่มีรูปทรงเรขาคณิตแน่นอน การจัดเรียงตัวของ อะตอม โมเลกุล หรือ ไอออน อย่างเป็นระเบียบ เกิดจากการจัดเรียงตัวของ อะตอม โมเลกุล หรือ ไอออน อย่างไม่เป็นระเบียบ คุณสมบัติ Anisotropy คุณสมบัติ Isotropy (เท่ากันทุกทิศทาง) Ex: เพชร น้าตาลทราย ควอทซ์ Ex: แก้ว พลาสติก ยาง
