Report
Share
Recommended
Formulario

Relaciones entre diferentes magnitudes químicas que son útiles para el cálcula en disoluciones y en estequiometría
Energia, calor i temperatura

Tipos de energía, atributos, conservación de la energía mecánica, trabajo, balances de energía, energía interna, calor y temperatura
Tema7laterraalunivers2part

El documento describe el Sistema Solar y el lugar del Sol y la Tierra en él. Explica que el Sistema Solar se formó hace unos 5.000 millones de años a partir de una nube de gas y polvo, y está compuesto por el Sol y varios objetos como planetas, asteroides y cometas que orbitan alrededor del Sol. También describe brevemente la evolución de las estrellas, incluido el Sol, las nebulosas y los agujeros negros.
Recommended
Formulario

Relaciones entre diferentes magnitudes químicas que son útiles para el cálcula en disoluciones y en estequiometría
Energia, calor i temperatura

Tipos de energía, atributos, conservación de la energía mecánica, trabajo, balances de energía, energía interna, calor y temperatura
Tema7laterraalunivers2part

El documento describe el Sistema Solar y el lugar del Sol y la Tierra en él. Explica que el Sistema Solar se formó hace unos 5.000 millones de años a partir de una nube de gas y polvo, y está compuesto por el Sol y varios objetos como planetas, asteroides y cometas que orbitan alrededor del Sol. También describe brevemente la evolución de las estrellas, incluido el Sol, las nebulosas y los agujeros negros.
FORCES I PRESSIÓ

concepto de fuerza, suma de fuerzas, ley de Hook, concepto de presión, presión atmosférica
Taller pressió

Experiencias sobre los conceptos de presión, presión atmosfèrica y presión hidrostática
Pauacidobasesolubilitat

Este documento contiene varios ejercicios de ácido-base, incluyendo cálculos de pH, grados de disociación y fuerza relativa de ácidos y bases. En los ejercicios se proporcionan constantes de acidéz para ácidos como ácido acético, fórmico, benzoico y láctico, y se piden determinar el pH resultante de mezclar diferentes disoluciones ácidas y básicas.
Equilibripau2016

Este documento presenta varios problemas de equilibrio químico tomados de exámenes de selectividad (PAU) de Química de 2o de Bachillerato en España. Incluye ejercicios sobre cálculo de constantes de equilibrio, determinación de composiciones de mezclas gaseosas en equilibrio, y efectos de cambios de condiciones sobre el desplazamiento del equilibrio.
Paucinetica2016

Este documento contiene varios problemas de cinética química de exámenes de química de 2o de bachillerato. Los problemas cubren temas como leyes de velocidad, órdenes de reacción, constantes de velocidad y cálculos de velocidades para diferentes concentraciones.
Selectivitattermoquimica

Ejercicios PAU de la Comunidad Valenciana de 2000 a 2015 del tema de Termoquímica clasificados por tipo de ejercicio.
Comoidentifcartipodecompuesto

Este documento describe cómo identificar el tipo de compuesto químico a partir de su fórmula o nombre. Explica que los compuestos binarios contienen dos elementos, los hidróxidos tienen la estructura Metal(OH)x, y los ácidos hidrádicos y oxoácidos siguen estructuras específicas. También indica que los nombres de los compuestos binarios terminan en -uro, los ácidos hidrádicos se llaman ácido NoMetal-Hídrico o NoMetal-uro de hidrógeno, y los nombres
Selectivitatenllaç

Este documento presenta varias preguntas sobre la estructura electrónica, geometría molecular y polaridad de diferentes moléculas. Se proporcionan estructuras de Lewis, geometrías moleculares y se determina si las moléculas son polares o apolares para especies como BF3, NF3, F2CO, H2O, CO2, NH3, CH4, PCl3, SF6, HF y SF6 entre otras a lo largo de varios ejercicios. También se discute el origen de la polaridad de los enlaces covalentes y se ordenan
Provespauestructuraatomica

actividades de las pruebas PAU de Química de Valencia de los temas "Estructura atòmica y Tabla Periódica" de 2001 a 2015
ACTIVITATS TEMA ESTRUCTURA ATÒMICA I TAULA PERIÒDICA

actividades sobre la estructura atómica, la tabla periódica y propiedades periódicas para 2 Bachiller
More Related Content
More from Jose Maria Bleda Guerrero
FORCES I PRESSIÓ

concepto de fuerza, suma de fuerzas, ley de Hook, concepto de presión, presión atmosférica
Taller pressió

Experiencias sobre los conceptos de presión, presión atmosfèrica y presión hidrostática
Pauacidobasesolubilitat

Este documento contiene varios ejercicios de ácido-base, incluyendo cálculos de pH, grados de disociación y fuerza relativa de ácidos y bases. En los ejercicios se proporcionan constantes de acidéz para ácidos como ácido acético, fórmico, benzoico y láctico, y se piden determinar el pH resultante de mezclar diferentes disoluciones ácidas y básicas.
Equilibripau2016

Este documento presenta varios problemas de equilibrio químico tomados de exámenes de selectividad (PAU) de Química de 2o de Bachillerato en España. Incluye ejercicios sobre cálculo de constantes de equilibrio, determinación de composiciones de mezclas gaseosas en equilibrio, y efectos de cambios de condiciones sobre el desplazamiento del equilibrio.
Paucinetica2016

Este documento contiene varios problemas de cinética química de exámenes de química de 2o de bachillerato. Los problemas cubren temas como leyes de velocidad, órdenes de reacción, constantes de velocidad y cálculos de velocidades para diferentes concentraciones.
Selectivitattermoquimica

Ejercicios PAU de la Comunidad Valenciana de 2000 a 2015 del tema de Termoquímica clasificados por tipo de ejercicio.
Comoidentifcartipodecompuesto

Este documento describe cómo identificar el tipo de compuesto químico a partir de su fórmula o nombre. Explica que los compuestos binarios contienen dos elementos, los hidróxidos tienen la estructura Metal(OH)x, y los ácidos hidrádicos y oxoácidos siguen estructuras específicas. También indica que los nombres de los compuestos binarios terminan en -uro, los ácidos hidrádicos se llaman ácido NoMetal-Hídrico o NoMetal-uro de hidrógeno, y los nombres
Selectivitatenllaç

Este documento presenta varias preguntas sobre la estructura electrónica, geometría molecular y polaridad de diferentes moléculas. Se proporcionan estructuras de Lewis, geometrías moleculares y se determina si las moléculas son polares o apolares para especies como BF3, NF3, F2CO, H2O, CO2, NH3, CH4, PCl3, SF6, HF y SF6 entre otras a lo largo de varios ejercicios. También se discute el origen de la polaridad de los enlaces covalentes y se ordenan
Provespauestructuraatomica

actividades de las pruebas PAU de Química de Valencia de los temas "Estructura atòmica y Tabla Periódica" de 2001 a 2015
ACTIVITATS TEMA ESTRUCTURA ATÒMICA I TAULA PERIÒDICA

actividades sobre la estructura atómica, la tabla periódica y propiedades periódicas para 2 Bachiller
More from Jose Maria Bleda Guerrero (20)
ACTIVITATS TEMA ESTRUCTURA ATÒMICA I TAULA PERIÒDICA

ACTIVITATS TEMA ESTRUCTURA ATÒMICA I TAULA PERIÒDICA
Formulario
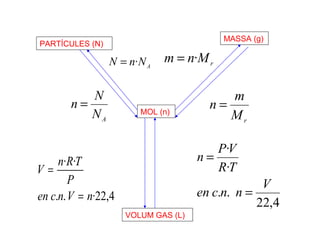
- 1. MOL (n) PARTÍCULES (N) A NnN ·= AN N n = MASSA (g) rM m n = rMnm ·= VOLUM GAS (L) 4,22·.. ·· nVncen P TRn V = = 4,22 .. · · V nncen TR VP n = =
- 2. MOLARIDAD (mol/L) t s V n M =100·% t s m m = t s V m c = PERCENTATGE EN MASSA CONCENTRACIÒ EN g/L FRACCIÓ MOLAR t s n n =χ dst mmm += r s s M m n = t t t V m d = dst nnn +=
- 3. 4 Fe (s) + 3 O2 (g) → 2 Fe2O3 (s) 1) Mescla (puresa) 100·% t Fe m m Fe = 100·% 2 2 t O V V O = 22 3 4 O Fe n n Omol Femol = mFe VO2 nFe nO23) Reactiu limitant 2) Passar a mols 4) Relacionar reactiu limitant amb el producte 2 32 2 32 3 2 O OFe n n Omol OFemol = són mols teòrics Relacionen substàncies pures 5) Passen de producte teòric a producte real 100·(%)dimRe 32 32 teòricaOFequantitat realOFequantitat entn =