Report
Share
Recommended
Examen de-química-ii

Este documento presenta una lista de términos químicos importantes como cationes, aniones y compuestos químicos comunes. Incluye los nombres y fórmulas de iones como cloruro, nitrato y sulfuro, así como los nombres de metales como zinc, cadmio y tantalio. También enumera compuestos como sulfato de sodio, óxido de azufre (VI), carbonato de litio y sulfuro de mercurio (I) junto con sus fórmulas químicas y si son poliatómicos o monoató
Tarea portal-cch-quimica

El documento presenta información sobre el carbono y sus formas alotrópicas, así como un cuestionario sobre macronutrientes y micronutrientes. El carbono es un elemento químico que se encuentra en diversas formas como el grafito o el diamante. El cuestionario contiene preguntas sobre los elementos que componen las proteínas, lípidos, vitaminas y carbohidratos, así como las diferencias entre estos.
Estequiometria 4

Este documento presenta cuatro problemas estequiométricos relacionados con la obtención de fertilizantes nitrogenados como el nitrato de amonio y la urea a partir de reacciones químicas. Los problemas incluyen calcular la masa de producto obtenido a partir de una masa dada de reactivo y calcular la cantidad de mol de producto obtenido a partir de una cantidad dada de mol de reactivo.
Examen de-química-ii-1

Este documento presenta una lista de sustancias químicas incluyendo sus nombres, fórmulas químicas y cargas iónicas. Se enumeran los aniones y cationes comunes como cloruro, sulfuro y nitrato junto con los elementos químicos como zinc, cadmio, plomo y sus compuestos. También se incluyen algunos óxidos, sulfatos y carbonatos con sus fórmulas químicas.
Tarea de-portal-acdemico-quimica

Este documento proporciona instrucciones para un proyecto escolar en el que los estudiantes construirán modelos de hidrocarburos usando gomitas y palillos. Los estudiantes tomarán fotos de sus modelos y las pegarán en una tabla junto con el nombre y la estructura química de cada hidrocarburo, incluyendo metano, butino, penteno, propino, pentano, etino, eteno, butano y propano.
Anexo 61

Este documento presenta una tabla en blanco para que el estudiante dibuje el número de electrones en la capa externa de cada elemento de acuerdo a su posición en los grupos representativos de la tabla periódica. El estudiante debe llenar la tabla con el número de electrones correspondiente a cada elemento listado en las filas y columnas de la tabla.
Recommended
Examen de-química-ii

Este documento presenta una lista de términos químicos importantes como cationes, aniones y compuestos químicos comunes. Incluye los nombres y fórmulas de iones como cloruro, nitrato y sulfuro, así como los nombres de metales como zinc, cadmio y tantalio. También enumera compuestos como sulfato de sodio, óxido de azufre (VI), carbonato de litio y sulfuro de mercurio (I) junto con sus fórmulas químicas y si son poliatómicos o monoató
Tarea portal-cch-quimica

El documento presenta información sobre el carbono y sus formas alotrópicas, así como un cuestionario sobre macronutrientes y micronutrientes. El carbono es un elemento químico que se encuentra en diversas formas como el grafito o el diamante. El cuestionario contiene preguntas sobre los elementos que componen las proteínas, lípidos, vitaminas y carbohidratos, así como las diferencias entre estos.
Estequiometria 4

Este documento presenta cuatro problemas estequiométricos relacionados con la obtención de fertilizantes nitrogenados como el nitrato de amonio y la urea a partir de reacciones químicas. Los problemas incluyen calcular la masa de producto obtenido a partir de una masa dada de reactivo y calcular la cantidad de mol de producto obtenido a partir de una cantidad dada de mol de reactivo.
Examen de-química-ii-1

Este documento presenta una lista de sustancias químicas incluyendo sus nombres, fórmulas químicas y cargas iónicas. Se enumeran los aniones y cationes comunes como cloruro, sulfuro y nitrato junto con los elementos químicos como zinc, cadmio, plomo y sus compuestos. También se incluyen algunos óxidos, sulfatos y carbonatos con sus fórmulas químicas.
Tarea de-portal-acdemico-quimica

Este documento proporciona instrucciones para un proyecto escolar en el que los estudiantes construirán modelos de hidrocarburos usando gomitas y palillos. Los estudiantes tomarán fotos de sus modelos y las pegarán en una tabla junto con el nombre y la estructura química de cada hidrocarburo, incluyendo metano, butino, penteno, propino, pentano, etino, eteno, butano y propano.
Anexo 61

Este documento presenta una tabla en blanco para que el estudiante dibuje el número de electrones en la capa externa de cada elemento de acuerdo a su posición en los grupos representativos de la tabla periódica. El estudiante debe llenar la tabla con el número de electrones correspondiente a cada elemento listado en las filas y columnas de la tabla.
Sopa de-letreas-quimica

This document contains a series of scrambled words and letters with no context. The words include types of chemicals and compounds such as isomers, isometros, alqueno, molecular, carbonos, pentano, acido, insoluble, isopentano. It also includes the names of group members Leon Cruz Mayela, Nora Breton, Berenice Hernandez, Monica Valencia, Diego Mondragon, Itzel Castillo who make up Equipo 1.
Estequiometria 2

Este documento presenta cinco problemas de cálculos estequiométricos que involucran reacciones químicas. Cada problema proporciona una ecuación química y una cantidad de reactivo y pregunta por la cantidad de producto obtenido.
Micronutrientes y-macronutrientes

Los micronutrientes son sustancias que el organismo necesita en pequeñas cantidades y son indispensables para diferentes procesos, mientras que los macronutrientes son aquellos nutrientes que suministran la mayor parte de la energía metabólica del organismo.
Estruct e imag_hidrocarb-putitaaa

La tabla proporciona las estructuras químicas e imágenes de varios hidrocarburos, incluidos metano, butino, penteno, propino, pentano, etino, eteno y butano. Se pide completar las últimas dos columnas identificando el tipo de enlace (sencillo, doble o triple) y si el hidrocarburo es saturado o insaturado para cada compuesto.
Anexo 70-equipo-1

El documento explica diferentes tipos de enlaces químicos. Un enlace interatómico une átomos dentro de una molécula, mientras que un enlace intermolecular une moléculas separadas. Un enlace covalente polar se forma cuando los átomos en un enlace covalente tienen diferentes electronegatividades, resultando en polos positivos y negativos en la molécula. El agua contiene dos enlaces covalentes polares entre el oxígeno y los átomos de hidrógeno. Además del enlace covalente, las molé
Jugo de-aniones-y-cationes

Este documento lista los principales cationes y aniones que se encuentran en soluciones iónicas. Los cationes incluyen sodio, potasio, calcio, magnesio, hierro (II), hierro (III) y amonio. Los aniones incluyen cloruro, sulfuro, nitrato, carbonato, sulfato, fosfato y cobre o cubrico.
Juego proiedades-del-carbono

The document discusses properties of carbon including key terms related to carbon chemistry. It provides a word search puzzle containing terms like alkanes, alkenes, alkynes, double bonds, linear chains, and periods to find definitions and understand carbon compounds.
Rúbrica de-evaluación

La rubrica evalúa el desempeño de estudiantes en la resolución de problemas químicos en diferentes aspectos como escribir ecuaciones correctamente, balancear ecuaciones químicas, calcular moles, convertir entre moles y gramos, y hacer proporciones o reglas de tres. Cada aspecto se califica de 0 a 2 puntos dependiendo del nivel de desempeño del estudiante. La rubrica muestra los resultados de la evaluación de un estudiante que obtuvo un total de 9 de 10 puntos.
Anexo 65.docx-diego

El documento proporciona una tabla con la diferencia de electronegatividad entre los elementos de varias moléculas comunes. Solicita determinar el tipo de enlace y el átomo con carga negativa. La tabla muestra que moléculas como OF2, H2S y NH3 tienen enlaces covalentes polares, mientras que moléculas como MgCl, Li3N y SrF2 forman enlaces iónicos.
Practica 2

Este documento presenta una práctica de laboratorio sobre el suelo. El objetivo es que los estudiantes observen muestras de suelo bajo un microscopio para determinar si es una mezcla heterogénea o homogénea. Se describen los materiales y procedimientos necesarios, incluida la recolección de una muestra de suelo, observación microscópica y pruebas como agregar agua y calentar la muestra.
Anexo 631

El documento contiene 14 preguntas sobre tipos de enlaces químicos. Explica la diferencia entre enlaces iónicos y covalentes, dando ejemplos de cada uno. También cubre enlaces covalentes polares y no polares, enlaces múltiples, por qué el nitrógeno tiene un triple enlace y el oxígeno doble, y clasifica varios compuestos químicos según su tipo de enlace.
Evasum07 21-1 (1)

El documento presenta un paquete de evaluación para el curso de Química II con preguntas sobre diversos temas como los tipos de sustancias que constituyen los alimentos, las propiedades del carbono y las sales. El paquete fue elaborado por un grupo de profesores coordinados para evaluar de manera sumativa las primeras tres unidades del programa de Química II en el plantel Naucalpan de la ENCH.
Minerales visita-a-museos-virtuales-semi-completo

El documento clasifica los componentes sólidos del suelo en material orgánico e inorgánico. El material orgánico está compuesto de restos de plantas y animales en descomposición, que forman humus. El material inorgánico son partículas de roca desgastadas que constituyen la mayor parte del suelo. Se dividen los minerales inorgánicos en primarios de la roca madre y secundarios formados por su alteración.
Practica de-alimentos

Este documento describe procedimientos para identificar carbohidratos, lípidos y proteínas en alimentos. Se utilizan pruebas de lugol y Benedict para identificar almidón y glucosa (carbohidratos), pruebas de Biuret para identificar proteínas, y colorantes como Sudan II o III para identificar lípidos que no se mezclan con el agua. El objetivo es identificar experimentalmente estas biomoléculas fundamentales en diferentes alimentos.
Expo balanceo-de-ecuacione-redox

El documento presenta una ecuación química original y los pasos para balancearla mediante el método de valencia. Primero se multiplica la valencia de cada átomo por sus subíndices para obtener una ecuación balanceada. Luego se indica que algunos átomos se oxidan y otros se reducen para alcanzar el balanceo final.
Practica 4-minerales

El documento describe las propiedades de 12 minerales comunes, incluyendo que la anastasa es un óxido, la litioforita es un hidróxido, la azurita es un carbonato básico de cobre, la vonsenita es un borato, la esfalerita es un sulfuro metálico, el yeso es un sulfato, el apatito es un fosfato, la halita es un cloruro, la caliza es un nitrato, la cianita es un silicato, y la rodonita es un silicato. También proporciona los
Juego aniones y cationes

The document contains a jumbled table that needs to be ordered and filled in correctly with monoatomic and polyatomic ions. It lists key words like sulfide, formula, oxides, hydroxide, acids, cations and anions to help identify the ions and place them in the proper columns for cations and anions.
Practica monedas-y-globo

Este documento describe una práctica de laboratorio realizada por estudiantes para observar el comportamiento de objetos cuando son sometidos a diferentes acciones. La práctica incluyó tres experimentos: 1) ver qué sucede cuando se derrama agua cerca de un globo inflado, 2) contar cuántas monedas caben en un vaso lleno de agua, y 3) contar cuántas gotas de agua o alcohol caben en una moneda. Los estudiantes realizaron los experimentos y anotaron sus observaciones.
Expo balanceo-de-ecuacione-redox (1)

El documento presenta una ecuación química original y los pasos para balancearla mediante el método de iones-electrones, incluyendo multiplicar la valencia por los subíndices y oxidar o reducir los átomos para igualar la carga en ambos lados de la ecuación.
Examen de-estequiometria

El documento presenta los cálculos estequiométricos realizados por el Equipo 4 sobre varias reacciones químicas. Realizan cálculos de masa-masa para determinar la cantidad de productos obtenidos a partir de una cantidad dada de reactivos. También calculan la masa molar de cada sustancia involucrada y aplican la ley de conservación de la materia. Por último, resuelven problemas estequiométricos sobre la obtención de fertilizantes como el nitrato de amonio y la urea.
More Related Content
Viewers also liked
Sopa de-letreas-quimica

This document contains a series of scrambled words and letters with no context. The words include types of chemicals and compounds such as isomers, isometros, alqueno, molecular, carbonos, pentano, acido, insoluble, isopentano. It also includes the names of group members Leon Cruz Mayela, Nora Breton, Berenice Hernandez, Monica Valencia, Diego Mondragon, Itzel Castillo who make up Equipo 1.
Estequiometria 2

Este documento presenta cinco problemas de cálculos estequiométricos que involucran reacciones químicas. Cada problema proporciona una ecuación química y una cantidad de reactivo y pregunta por la cantidad de producto obtenido.
Micronutrientes y-macronutrientes

Los micronutrientes son sustancias que el organismo necesita en pequeñas cantidades y son indispensables para diferentes procesos, mientras que los macronutrientes son aquellos nutrientes que suministran la mayor parte de la energía metabólica del organismo.
Estruct e imag_hidrocarb-putitaaa

La tabla proporciona las estructuras químicas e imágenes de varios hidrocarburos, incluidos metano, butino, penteno, propino, pentano, etino, eteno y butano. Se pide completar las últimas dos columnas identificando el tipo de enlace (sencillo, doble o triple) y si el hidrocarburo es saturado o insaturado para cada compuesto.
Anexo 70-equipo-1

El documento explica diferentes tipos de enlaces químicos. Un enlace interatómico une átomos dentro de una molécula, mientras que un enlace intermolecular une moléculas separadas. Un enlace covalente polar se forma cuando los átomos en un enlace covalente tienen diferentes electronegatividades, resultando en polos positivos y negativos en la molécula. El agua contiene dos enlaces covalentes polares entre el oxígeno y los átomos de hidrógeno. Además del enlace covalente, las molé
Jugo de-aniones-y-cationes

Este documento lista los principales cationes y aniones que se encuentran en soluciones iónicas. Los cationes incluyen sodio, potasio, calcio, magnesio, hierro (II), hierro (III) y amonio. Los aniones incluyen cloruro, sulfuro, nitrato, carbonato, sulfato, fosfato y cobre o cubrico.
Juego proiedades-del-carbono

The document discusses properties of carbon including key terms related to carbon chemistry. It provides a word search puzzle containing terms like alkanes, alkenes, alkynes, double bonds, linear chains, and periods to find definitions and understand carbon compounds.
Rúbrica de-evaluación

La rubrica evalúa el desempeño de estudiantes en la resolución de problemas químicos en diferentes aspectos como escribir ecuaciones correctamente, balancear ecuaciones químicas, calcular moles, convertir entre moles y gramos, y hacer proporciones o reglas de tres. Cada aspecto se califica de 0 a 2 puntos dependiendo del nivel de desempeño del estudiante. La rubrica muestra los resultados de la evaluación de un estudiante que obtuvo un total de 9 de 10 puntos.
Anexo 65.docx-diego

El documento proporciona una tabla con la diferencia de electronegatividad entre los elementos de varias moléculas comunes. Solicita determinar el tipo de enlace y el átomo con carga negativa. La tabla muestra que moléculas como OF2, H2S y NH3 tienen enlaces covalentes polares, mientras que moléculas como MgCl, Li3N y SrF2 forman enlaces iónicos.
Practica 2

Este documento presenta una práctica de laboratorio sobre el suelo. El objetivo es que los estudiantes observen muestras de suelo bajo un microscopio para determinar si es una mezcla heterogénea o homogénea. Se describen los materiales y procedimientos necesarios, incluida la recolección de una muestra de suelo, observación microscópica y pruebas como agregar agua y calentar la muestra.
Anexo 631

El documento contiene 14 preguntas sobre tipos de enlaces químicos. Explica la diferencia entre enlaces iónicos y covalentes, dando ejemplos de cada uno. También cubre enlaces covalentes polares y no polares, enlaces múltiples, por qué el nitrógeno tiene un triple enlace y el oxígeno doble, y clasifica varios compuestos químicos según su tipo de enlace.
Evasum07 21-1 (1)

El documento presenta un paquete de evaluación para el curso de Química II con preguntas sobre diversos temas como los tipos de sustancias que constituyen los alimentos, las propiedades del carbono y las sales. El paquete fue elaborado por un grupo de profesores coordinados para evaluar de manera sumativa las primeras tres unidades del programa de Química II en el plantel Naucalpan de la ENCH.
Minerales visita-a-museos-virtuales-semi-completo

El documento clasifica los componentes sólidos del suelo en material orgánico e inorgánico. El material orgánico está compuesto de restos de plantas y animales en descomposición, que forman humus. El material inorgánico son partículas de roca desgastadas que constituyen la mayor parte del suelo. Se dividen los minerales inorgánicos en primarios de la roca madre y secundarios formados por su alteración.
Practica de-alimentos

Este documento describe procedimientos para identificar carbohidratos, lípidos y proteínas en alimentos. Se utilizan pruebas de lugol y Benedict para identificar almidón y glucosa (carbohidratos), pruebas de Biuret para identificar proteínas, y colorantes como Sudan II o III para identificar lípidos que no se mezclan con el agua. El objetivo es identificar experimentalmente estas biomoléculas fundamentales en diferentes alimentos.
Expo balanceo-de-ecuacione-redox

El documento presenta una ecuación química original y los pasos para balancearla mediante el método de valencia. Primero se multiplica la valencia de cada átomo por sus subíndices para obtener una ecuación balanceada. Luego se indica que algunos átomos se oxidan y otros se reducen para alcanzar el balanceo final.
Practica 4-minerales

El documento describe las propiedades de 12 minerales comunes, incluyendo que la anastasa es un óxido, la litioforita es un hidróxido, la azurita es un carbonato básico de cobre, la vonsenita es un borato, la esfalerita es un sulfuro metálico, el yeso es un sulfato, el apatito es un fosfato, la halita es un cloruro, la caliza es un nitrato, la cianita es un silicato, y la rodonita es un silicato. También proporciona los
Juego aniones y cationes

The document contains a jumbled table that needs to be ordered and filled in correctly with monoatomic and polyatomic ions. It lists key words like sulfide, formula, oxides, hydroxide, acids, cations and anions to help identify the ions and place them in the proper columns for cations and anions.
Practica monedas-y-globo

Este documento describe una práctica de laboratorio realizada por estudiantes para observar el comportamiento de objetos cuando son sometidos a diferentes acciones. La práctica incluyó tres experimentos: 1) ver qué sucede cuando se derrama agua cerca de un globo inflado, 2) contar cuántas monedas caben en un vaso lleno de agua, y 3) contar cuántas gotas de agua o alcohol caben en una moneda. Los estudiantes realizaron los experimentos y anotaron sus observaciones.
Viewers also liked (20)
More from AlejandraBerenice2108
Expo balanceo-de-ecuacione-redox (1)

El documento presenta una ecuación química original y los pasos para balancearla mediante el método de iones-electrones, incluyendo multiplicar la valencia por los subíndices y oxidar o reducir los átomos para igualar la carga en ambos lados de la ecuación.
Examen de-estequiometria

El documento presenta los cálculos estequiométricos realizados por el Equipo 4 sobre varias reacciones químicas. Realizan cálculos de masa-masa para determinar la cantidad de productos obtenidos a partir de una cantidad dada de reactivos. También calculan la masa molar de cada sustancia involucrada y aplican la ley de conservación de la materia. Por último, resuelven problemas estequiométricos sobre la obtención de fertilizantes como el nitrato de amonio y la urea.
Evasum07 21-1

Las sales son compuestos iónicos formados por cationes y aniones. Son mayoritariamente solubles en agua y tienen puntos de fusión y ebullición altos. El carbono permite la formación de una gran cantidad de compuestos orgánicos debido a su capacidad de formar enlaces covalentes múltiples y dobles.
Estequiometria 3

El documento explica cómo realizar cálculos estequiométricos utilizando relaciones mol-mol. Explica cómo calcular la cantidad de productos formados a partir de una cantidad dada de reactivos usando la relación estequiométrica de la reacción química balanceada. Proporciona dos ejemplos: 1) calcular la cantidad de NaCl formado a partir de una cantidad dada de FeCl3, y 2) calcular la cantidad de sulfato de amonio formado a partir de una cantidad dada de hidróxido de amonio.
Carbohidratos

El documento habla sobre los carbohidratos, su fórmula general, el proceso de fotosíntesis y los monosacáridos. Explica que los carbohidratos son compuestos orgánicos formados por carbono, hidrógeno y oxígeno, que las plantas los producen mediante fotosíntesis y que los monosacáridos más simples son las aldosas y cetosas.
Conceptos de-estequiometria-equipo-1

Este documento presenta conceptos fundamentales de estequiometría como masa molecular, masa atómica, peso formula, unidad de masa atómica (uma), mol y masa molar. Explica que la masa molecular es la suma de las masas atómicas de los átomos de una molécula, mientras que la masa atómica es el peso relativo de los átomos de los elementos. También define el peso formula como la masa de los pesos atómicos de los elementos de una fórmula química. Finalmente, introduce el mol como
Estequiometria 1

Este documento presenta dos ejemplos de cálculos estequiométricos de masa-masa. El primer ejemplo muestra cómo calcular las masas de los reactivos y productos involucrados en una reacción química dada sus fórmulas moleculares y el número de moles. El segundo ejemplo resuelve un problema estequiométrico determinando la masa de producto que se formará a partir de una masa dada de un reactivo limitante.
El suelo-9

Este documento no contiene información sustancial para resumir. Consiste únicamente en una serie de puntos vacíos sin contenido.
Construcción del-ion-sodio

Este documento describe un experimento para representar los iones de sodio y cloruro usando plastilina de diferentes colores. Explica que se usarán bolas de plastilina amarilla para representar los iones de sodio y cloruro, bolas rojas para representar átomos con carga positiva, y bolas blancas más pequeñas para átomos con carga negativa. Estas se unirán con palillos para mostrar la estructura iónica del sodio y el cloruro. El objetivo es enseñar a los estudiantes sobre la natur
More from AlejandraBerenice2108 (9)
Alcanos
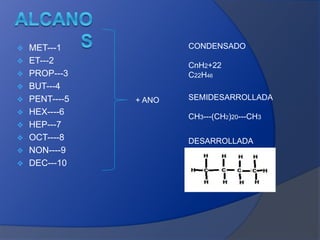
- 1. MET---1 ET---2 PROP---3 BUT---4 PENT----5 HEX----6 HEP---7 OCT----8 NON----9 DEC---10 + ANO CONDENSADO CnH2+22 C22H46 SEMIDESARROLLADA CH3---(CH2)20---CH3 DESARROLLADA
- 2. Metano CH4 Etano C2H6 CH3-----CH3 Propano C3H8 CH3—CH2---CH3 Butano C4H10 CH3—CH2—CH2—CH3 Pentano C5H12 CH3—CH2—CH2—CH2---CH3 Hexano C6H14 CH3—CH2—CH2—CH2--CH2— CH3 Heptano C7H16 CH3—CH2—CH2—CH2—CH2— CH2—CH3