3 eso.t2.la naturaleza de la materia
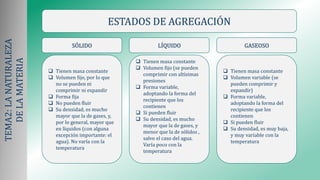
- 1. TEMA2:LANATURALEZA DELAMATERIA ESTADOS DE AGREGACIÓN SÓLIDO LÍQUIDO GASEOSO Tienen masa constante Volumen fijo, por lo que no se pueden ni comprimir ni expandir Forma fija No pueden fluir Su densidad, es mucho mayor que la de gases, y, por lo general, mayor que en líquidos (con alguna excepción importante: el agua). No varía con la temperatura Tienen masa constante Volumen fijo (se pueden comprimir con altísimas presiones Forma variable, adoptando la forma del recipiente que los contienen Si pueden fluir Su densidad, es mucho mayor que la de gases, y menor que la de sólidos , salvo el caso del agua. Varía poco con la temperatura Tienen masa constante Volumen variable (se pueden comprimir y expandir) Forma variable, adoptando la forma del recipiente que los contienen Si pueden fluir Su densidad, es muy baja, y muy variable con la temperatura
- 2. DENSIDAD (RECORDATORIO) Esta magnitud física da idea de cómo de agrupada se encuentra la materia. Exactamente, indica la relación existente entre la masa de un cuerpo y el volumen que ocupa Matemáticamente: 𝜌 = 𝑚 𝑉 (𝑆𝐼: 𝑘𝑔 𝑚3) TEMA2:LANATURALEZA DELAMATERIA
- 3. ESTADO GASEOSO Debido a las características de los gases, resulta complicado manejar masas. Los científicos recurren a otras magnitudes (presión, temperatura y volumen), ya que definen el estado del gas, y, por tanto, permiten determinar la masa de dicho gas Relaciona la fuerza ejercida por unidad de superficie: 𝑝 = 𝐹 𝑆 La unidad de presión en SI es el Pascal (Pa), aunque también se utilice el bar y la atmósfera (atm): 1𝑏𝑎𝑟 = 105 𝑃𝑎 1𝑎𝑡𝑚 = 101325 𝑃𝑎 = 760𝑚𝑚𝐻𝑔 El volumen de un gas, dadas las características de estos, será el del recipiente. En SI, el patrón es el 𝑚3 , pero es muy común utilizar unidades de capacidad: 1𝑚3 = 1000𝐿 1𝑑𝑚3 = 1𝐿 1𝑐𝑚3 = 1𝑚𝐿 Es una medida del calor ganado o perdido por un cuerpo; en ningún caso debe confundirse con calor. Existen distintas escalas: • CELSIUS (℃) • KELVIN (K), usada en el SI 𝐾 = ℃ + 273´15 • FARENHEIT (℉) PRESIÓN TEMPERATURAVOLUMEN TEMA2:LANATURALEZA DELAMATERIA
- 4. LEYES DE LOS GASES El estudio de los gases en los siglos XVII y XVIII condujeron a unas leyes que explicaban el comportamiento de los gases. Entre ellas se encuentran: Ley de Boyle-Mariotte Ley de CharlesLey de Gay-Lussac TEMA2:LANATURALEZA DELAMATERIA
- 5. LEY DE BOYLE-MARIOTTE Esta ley relaciona la presión y el volumen de un gas, CUANDO LA TEMPERATURA ES CONSTANTE (es decir, no varía) “A temperatura constante, para una misma masa de gas, el producto de la presión de un gas por el volumen que ocupa es un valor constante” Matemáticamente: 𝑝. 𝑉 = 𝑐𝑡𝑒 (𝑇𝑐𝑡𝑒) 𝑝1. 𝑉1 = 𝑝2. 𝑉2 (𝑇𝑐𝑡𝑒) p (atm) V (L) p.V (atm.L) 4 1 4 2 2 4 1 4 4 8 8 20 0´25 TEMA2:LANATURALEZA DELAMATERIA
- 6. LEY DE GAY-LUSSAC Esta ley relaciona la presión y la temperatura absoluta, CUANDO EL VOLUMEN OCUPADO POR UN GAS ES CONSTANTE (es decir, no varía) “A volumen constante, para una misma masa de gas, el cociente entre de la presión de un gas y la temperatura a la que se encuentra es un valor constante” Matemáticamente: 𝑝 𝑇 = 𝑐𝑡𝑒 (𝑉𝑐𝑡𝑒) 𝑝1 𝑇1 = 𝑝2 𝑇2 (𝑉𝑐𝑡𝑒) p (atm) T (K) p/T (atm/K) 1 400 0´0025 0´75 300 0´0025 0´5 200 0´0025 0´25 100 0´0025 800 1´5 2 TEMA2:LANATURALEZA DELAMATERIA
- 7. LEY DE CHARLES Esta ley relaciona el volumen ocupado por un gas y la temperatura absoluta a la que se encuentra, CUANDO LA PRESIÓN EJERCIDA POR EL GAS ES CONSTANTE (es decir, no varía) “A presión constante, para una misma masa de gas, el cociente entre el volumen de un gas y la temperatura a la que se encuentra es un valor constante” Matemáticamente: 𝑉 𝑇 = 𝑐𝑡𝑒 (𝑃𝑐𝑡𝑒) 𝑉1 𝑇1 = 𝑉2 𝑇2 (𝑃𝑐𝑡𝑒) V (L) T (K) V/T (L/K) 1 500 0´002 0´75 375 0´002 0´5 250 0´25 1000 1´5 2 TEMA2:LANATURALEZA DELAMATERIA
- 8. TEORÍA CINÉTICO-MOLECULAR También llamado Modelo Cinético-Molecular, fue desarrollada en el siglo XIX, y aunque en un principio trataba de explicar el comportamiento de los gases, fue ampliándose hasta explicar el comportamiento de sólidos y líquidos, así como los cambios de estado. Se basa en unos postulados muy simples: La materia está formada por partículas muy pequeñas, que consideraremos esféricas Las partículas se hallan en constante movimiento (traslación, vibración, rotación), que aumentará con la temperatura El movimiento de las partículas estará determinado por dos tipos de fuerzas antagónicas: Fuerzas de cohesión: son atractivas, y tienden a mantener unidas las partículas Fuerzas de repulsión, tendente a dispersar y alejar dichas partículas TEMA2:LANATURALEZA DELAMATERIA
- 9. TCM Y ESTADO SÓLIDO ¿Cómo es su estructura interna? ¿Cómo se explican sus propiedades? Las fuerzas de cohesión son muy grandes, y las partículas están muy próximas entre sí. Los movimientos de las partículas son de vibración (que aumentarán con la temperatura, y viceversa) Al ser las fuerzas que mantienen unidas las partículas muy fuertes, estas no pueden separarse, cambiar de posición, ni tampoco aproximarse entre sí. De ahí que el volumen y forma de los sólidos sean constante, que no puedan comprimirse, expandirse ni deformarse. Al hallarse muy próximas las partículas, la densidad de los sólidos será, por lo general, mayor que la de líquidos y gases Dado que al aumentar la temperatura las partículas vibran más fuertemente, estas se separarán algo más. Esto explica la dilatación de los sólidos. Al disminuir la temperatura, sucederá lo contrario. TEMA2:LANATURALEZA DELAMATERIA
- 10. TCM Y ESTADO LÍQUIDO ¿Cómo es su estructura interna? ¿Cómo se explican sus propiedades? Las fuerzas de cohesión son menores que en sólidos. Las partículas se encuentran en grupos que pueden deslizarse entre sí. Los movimientos de las partículas son de traslación y vibración (que aumentarán con la temperatura, y viceversa) Al ser aún fuertes las fuerzas entre partículas, estas no pueden separarse, por lo que los líquidos no se expanden. La ligera compresión se explica porque las partículas podrán aproximarse ligeramente al no estar rígidamente unidas. Al deslizarse entre sí los grupos de partículas, podrán adaptarse a la forma del recipiente La densidad de los sólidos será, por lo general, menor que la de sólidos, pero mayor que la de gases Dado que al aumentar la temperatura las partículas vibran más, y los desplazamientos de grupos de partículas serán mayores, la densidad disminuirá. Al disminuir la temperatura, sucederá lo contrario. TEMA2:LANATURALEZA DELAMATERIA
- 11. TCM Y ESTADO GASEOSO ¿Cómo es su estructura interna? ¿Cómo se explican sus propiedades? Las fuerzas de cohesión son muy débiles, por lo que las partículas se mueven libremente (por todo el recipiente). Como consecuencia, estarán muy separadas Los movimientos de las partículas son de traslación (que aumentarán con la temperatura, y viceversa) Al ser casi nulas las fuerzas entre partículas, y estar muy separadas entre sí, un cambio en el volumen no modificará las condiciones. Por ello los gases pueden comprimirse y expandirse Por la misma razón, un cambio en la forma del recipiente, no modificará las condiciones. Por ello los gases adoptar la forma del recipiente La densidad de los gases será muy baja, al hallarse las partículas muy dispersas (muy poco agrupadas) Al aumentar la temperatura las partículas se moverán más, aumentando la separación entre ellas, con lo cual la densidad disminuirá. Al disminuir la temperatura, sucederá lo contrario. TEMA2:LANATURALEZA DELAMATERIA
- 13. CAMBIOS DE ESTADO FUSIÓN-SOLIDIFICACIÓN Cambios de estado entre sólido y líquido, que se producen A LA MISMA TEMPERATURA, llamada PUNTO DE FUSIÓN (o temperatura de fusión), cuyo valor depende del tipo de sustancia) VAPORIZACIÓN-CONDENSACIÓN Es el cambio general de estado entre líquido y gas. Si el cambio de líquido a gas se realiza únicamente en la superficie del líquido, a cualquier temperatura, el proceso se denomina EVAPORACIÓN Si el cambio de líquido a gas se realiza en todo el líquido, y a una temperatura fija (TEMPERATURA O PUNTO DE EBULLICIÓN), el proceso se denomina EBULLICIÓN TEMA2:LANATURALEZA DELAMATERIA
- 14. CURVAS DE CALENTAMIENTO • TRAMO A-B: A medida que se calienta el sólido, este aumenta su temperatura, pero permanece en ese estado. Las partículas aumentan su vibración • TRAMO B-C: Cambio de estado, y como puede verse, NO HAY CAMBIO DE TEMPERATURA mientras se produce. El calor se “invierte” en romper la estructura del sólido • TRAMO C-D: A medida que se calienta el líquido, este aumenta su temperatura, pero permanece en ese estado. Las partículas se mueven más rápido • TRAMO D-E: Cambio de estado, y de nuevo, NO HAY CAMBIO DE TEMPERATURA mientras se produce. El calor se “invierte” en romper la estructura del líquido. • TRAMO E-F: A medida que se calienta el gas, este aumenta su temperatura, pero permanece en ese estado. Las partículas se mueven más rápido TEMA2:LANATURALEZA DELAMATERIA
- 15. (SABER MÁS) OTROS ESTADOS DE LA MATERIA • ¿Qué es el plasma? LINK1 • ¿Cómo funcionan los televisores de plasma? LINK2 PLASMA • ¿Qué son los cristales líquidos? LINK1 • ¿Cómo funcionan las pantallas LCD? LINK2 CRISTALES LÍQUIDOS TEMA2:LANATURALEZA DELAMATERIA