Estudo dos gases
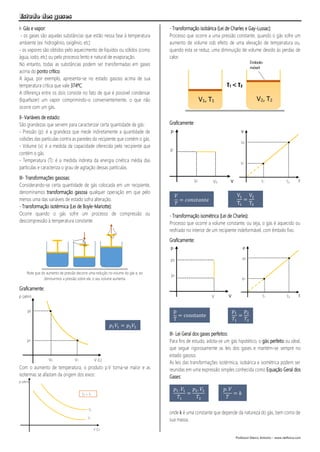
- 1. Estudo dos gases Professor Marco Antonio – www.netfisica.com I- Gás e vapor: - os gases são aquelas substâncias que estão nessa fase à temperatura ambiente (ex: hidrogênio, oxigênio, etc) - os vapores são obtidos pelo aquecimento de líquidos ou sólidos (como água, iodo, etc) ou pelo processo lento e natural de evaporação. No entanto, todas as substâncias podem ser transformadas em gases acima do ponto crítico. A água, por exemplo, apresenta-se no estado gasoso acima de sua temperatura crítica que vale 374ºC. A diferença entre os dois consiste no fato de que é possível condensar (liquefazer) um vapor comprimindo-o convenientemente, o que não ocorre com um gás. II- Variáveis de estado: São grandezas que servem para caracterizar certa quantidade de gás: - Pressão (p): é a grandeza que mede indiretamente a quantidade de colisões das partículas contra as paredes do recipiente que contém o gás. - Volume (v): é a medida da capacidade oferecida pelo recipiente que contém o gás. - Temperatura (T): é a medida indireta da energia cinética média das partículas e caracteriza o grau de agitação dessas partículas. III- Transformações gasosas: Considerando-se certa quantidade de gás colocada em um recipiente, denominamos transformação gasosa qualquer operação em que pelo menos uma das variáveis de estado sofra alteração. - Transformação isotérmica (Lei de Boyle-Mariotte): Ocorre quando o gás sofre um processo de compressão ou descompressão à temperatura constante. Note que do aumento de pressão decorre uma redução no volume do gás e, ao diminuirmos a pressão sobre ele, o seu volume aumenta Graficamente: Com o aumento de temperatura, o produto p.V torna-se maior e as isotermas se afastam da origem dos eixos: - Transformação isobárica (Lei de Charles e Gay-Lussac): Processo que ocorre a uma pressão constante, quando o gás sofre um aumento de volume sob efeito de uma elevação de temperatura ou, quando esta se reduz, uma diminuição de volume devido às perdas de calor. Graficamente - Transformação isométrica (Lei de Charles): Processo que ocorre a volume constante, ou seja, o gás é aquecido ou resfriado no interior de um recipiente indeformável, com êmbolo fixo. Graficamente: III- Lei Geral dos gases perfeitos: Para fins de estudo, adota-se um gás hipotético, o gás perfeito ou ideal, que segue rigorosamente as leis dos gases e mantém-se sempre no estado gasoso. As leis das transformações isotérmica, isobárica e isométrica podem ser reunidas em uma expressão simples conhecida como Equação Geral dos Gases: onde k é uma constante que depende da natureza do gás, bem como de sua massa. 𝑉 𝑇 = 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒 V1 T1 = V2 T2 p T = constante 𝑝1 𝑇1 = 𝑝2 𝑇2 𝑝1. 𝑉1 𝑇1 = 𝑝2. 𝑉2 𝑇2 𝑝. 𝑉 𝑇 = 𝑘 𝑝1 𝑉1 = 𝑝2 𝑉2
- 2. Estudo dos gases Professor Marco Antonio – www.netfisica.com IV- Condições normais de temperatura e pressão (CNTP): Foram estabelecidas pela União Internacional de Química Pura e Aplicada (IUPAC) para estabelecer um estado de referência para o gás ideal, adotando-se como valores referenciais: - pressão: 1 atm = 105 Pa (pressão atmosférica ao nível do mar) - Temperatura: 0º C = 273 K Aplicação: ER1. Certo gás perfeito à temperatura de 25 °C, sob pressão de 1,6 atm, ocupa o volume de 20 litros em um recipiente provido de êmbolo móvel. Caso o gás sofra uma compressão isotérmica e o seu volume se reduza à metade, qual será a nova pressão no interior do recipiente? ER2. O diagrama abaixo (fora de escala) mostra duas isotérmicas, A e B, de uma mesma massa de um gás perfeito. Levando-se em conta os dados do diagrama, determine: a) a pressão p; b) a temperatura absoluta TB; c) o volume V. ER3. Certa massa gasosa, contida em um recipiente rígido de volume variável, inicialmente nas CNTP, ocupa um volume de 5 L. Fornecendo calor ao gás, sua temperatura sobe "isobaricamente" para 409,5 °C. Calcule o novo volume ocupado pelo gás. ER4. Determinada massa de gás perfeito está sob pressão de 6.105 Pa, ocupando um volume de 10 litros, à temperatura de 27 °C. Se o volume for reduzido à metade e a pressão dobrada, determine a temperatura final do gás, em °C. V- Teoria cinética dos gases: - Energia cinética média: A energia cinética média é diretamente proporcional à temperatura absoluta do gás. Onde: - n é o número de mols de partículas do gás. Fazendo m = massa de gás e M = massa molecular, temos que n é dado pela expressão: - R é a constante universal dos gases ideais: R = 0,082 atm.L/mol.K - T é a temperatura absoluta (K) VI- Mistura de gases O químico e físico inglês John Dalton descobriu que as partículas dos gases podem interpenetrar-se e misturar-se em qualquer proporção, permanecendo separadas uma das outras, como no ar: Aplicação: ER8. Na figura, o balão A contém certa quantidade de gás perfeito A sob pressão de 2 atm, e o balão fi, outra quantidade de gás perfeito B sob pressão de 3 atm, ambos na mesma temperatura. Sabendo que o balão A possui o triplo da capacidade do balão B, calcule a pressão da mistura pouco depois de aberta a torneira que separa os dois gases, supondo que não houve variação na temperatura. VII- Exercícios: EP1. No fundo de um lago, onde a pressão é de 2,2 atm, forma-se uma bolha de ar com volume de 4,0 cm3 . Calcule o volume da bolha depois de ela subir à tona, onde a pressão atmosférica mede 1,0 atm. Admita que nessa transformação a massa do gás no interior da bolha e a temperatura permaneceram constantes. R: 8,8 cm3 EP2. O diagrama representa uma transformação isométrica de certa massa de gás ideal, inicialmente nas condições normais de temperatura e pressão (CNTP). Determine: a) a pressão do gás quando a temperatura do sistema atinge 491,4 °C. R: 2,8 atm b) a temperatura, em graus celsius, quando a massa gasosa estiver sob pressão de 0,8 atm. R: -54,6 °C EP3. Uma garrafa plástica maleável com capacidade de 2 L, vazia e bem vedada com a tampa de rosca, é colocada no congelador de um refrigerador durante algumas horas. Ao ser retirada, a garrafa provavel- mente estará: a) cheia de gelo. b) estourada. c) da mesma forma que foi colocada. d) deformada e murcha. e) deformada e inchada. EP4. Um gás,inicialmente sob temperatura de 25 °C e pressão atmosférica normal, teve o seu volume triplicado "isobaricamente". Determine a temperatura em que isso aconteceu. R: 621 °C EP5. Certa quantidade de gás carbónico contido em um recipiente de 32 L, sob pressão de 1,0 atm e temperatura de 27 °C, foi transferido 𝐸𝑐𝑚 = 3 2 𝑛. 𝑅. 𝑇 n= m M 𝑝𝑉 𝑇 = 𝑝 𝐴 𝑉𝐴 𝑇𝐴 + 𝑝 𝐵 𝑉𝐵 𝑇𝐵
- 3. Estudo dos gases Professor Marco Antonio – www.netfisica.com integralmente para outro recipiente de capacidade 40 L, sem que a pressão tenha sido alterada. Como ficou a temperatura do gás, em °C, imediatamente após a transferência? R: A temperatura aumentou para 102 °C. EP6. Um cilindro com êmbolo móvel contém 24 L de gás nitrogênio, sob pressão de 15 atm e temperatura de 27 °C. Qual será o novo volume do gás à temperatura de 127 °C e pressão de 30 atm? R: 16 L EP7. Em um recipiente de capacidade de 15,5 L são colocados 110 g de CO2 (M = 44 g), à temperatura de 37 °C. Sendo dada a constante universal dos gases perfeitos R = 0,082 atm.L/mol.K, determine: a) o número de mol do gás carbônico. R: 2,5 mol b) a pressão do gás no interior do recipiente. R: 4,1 atm EP8. Um recipiente indeformável, provido de uma válvula, contém 300 g de um gás ideal, na temperatura de 27 °C e sob pressão de 1,5 atm. Pela válvula são injetados mais 600 g do mesmo gás e o recipiente é aquecido até a temperatura de 127 °C. Nessas condições, determine a nova pressão no interior do recipiente. R: 6,0 atm EP9. Determine a energia cinética média de 2 mol de gás perfeito que se encontram sob a temperatura de 57 °C. Para a constante universal dos gases perfeitos, use R = 8,31 J/mol.K. R: 8.226,9 J EP10. Calcule a energia cinética média de uma molécula de gás ideal que se encontra na temperatura de 87 °C. Dada a constante de Boltzmann k = 1,38 • 10"23 J/K. R: 7,45.10-21 J VIII- Aprofundamento e Revisão: 1. (EFOA-MG) Um gás perfeito, a uma pressão de 10 atm, ocupa um volume de 4 litros. Ele sofre uma transformação isotérmica e seu volume atinge 10 litros. A nova pressão exercida pelo gás é de: a) 4 atm b) 25 atm c) 100 atm d) 10 atm e) 250 atm 2. Um gás perfeito a 27 °C sofre uma expansão isotérmica de A para B, caindo sua pressão a 1/5 do valor inicial, conforme o gráfico a seguir. Determinar, para o estado B, o volume, a pressão e a temperatura do gás. TA = TB = 300 K = 27 °C, pB = 4 atm, VB = 50 L 3. Um cilindro de paredes rígidas e êmbolo móvel sem atrito contém um certo gás em seu interior, conforme indica a figura. Quando a temperatura é 27 °C, o volume ocupado pelo gás é 5 litros. Qual deve ser a temperatura para que o volume do gás seja 8 litros, mantendo a pressão constante? T2 = 207 °C 4. Dentro de um botijão existe determinada massa de gás ocupando o volume de 5 litros a 300 K e à pressão de 6 atmosferas. O botijão é esfriado até 200 K. Determine a pressão final, supondo invariável o volume do botijão. p2 = 4 atm 5. (UFIt-MG) Um motorista calibrou os pneus do seu carro à temperatura de 27 °C. Depois de rodar bastante, ao medir novamente a pressão, encontrou um resultado 20% superior ao valor da calibração inicial. Supondo-se invariável o volume das câmaras, a temperatura do ar comprimido deve ter atingido: a) 32 °C b) 320 K c) 360 K d) 300 K e) não temos dados para calculá-la 6. Uma dada massa de gás perfeito está num recipiente de volume 8,0 litros, à temperatura de 7,0 °C, exercendo a pressão de 4,0 atm. Reduzindo-se o volume a 6,0 L e aquecendo-se o gás, a sua pressão passou a ser 10 atm. Determine a que temperatura o gás foi aquecido. T2 = 525 K ou T2 = 252 °C 7. Determinada massa de gás num estado inicial A sofre a transformação ABC indicada no diagrama: Determine TB e VC. TB = 400 K e VC = 8L 8. O gráfico ilustra a isoterma de uma certa quantidade de gás que é levado do estado A para o estado C. Determine: a) o volume do gás no estado B; VB = 8 L b) a pressão do gás no estado C. pC = 2 atm
