Nefropatía membranosa: causas, manifestaciones clínicas y tratamiento
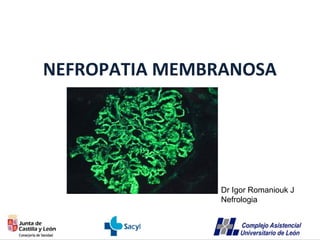
- 1. NEFROPATIA MEMBRANOSA Dr Igor Romaniouk J Nefrologia
- 2. NEFROPATÍA MEMBRANOSA • La GNM es la causa más común de síndrome nefrótico en adultos. • La incidencia es de 5-10 casos por cada millon de habitantes. 1.Korbet SM, Genchi RM, Borok RZ, Schwartz MM. The racial prevalence of glomerular lesions in nephrotic adults. Am J Kidney Dis 2008; 27:647.
- 3. NEFROPATÍA MEMBRANOSA • “Adultos caucasicos”. • “La glomeruloesclerosis focal y segmentaria es la más común en afroamericanos e hispánicos”.
- 4. NEFROPATÍA MEMBRANOSA • Esta enfermedad responde por aproximadamente el 21- 35% de casos de síndrome nefrótico en adultos y 1,5-9% en niños. • Muchas series muestran mayor frecuencia de GNM en hombres, con una relación H:M de 2:1. Arias LF, et al. Glomerular diseases in a Hispanic population: review of a regional renal biopsy database. Sao Paulo Med J. 2009;127(3):140-4.
- 5. NEFROPATÍA MEMBRANOSA • Es una enfermedad caracterizada por depósitos inmunes subepiteliales y la formación de proyecciones perpendiculares de material similar a la membrana basal glomerular (MBG) en la parte externa de ésta.
- 6. NEFROPATÍA MEMBRANOSA • Se caracteriza por atrapamiento de complejos inmunes, inmunoglobulinas y la formacion de complejo de ataque de membrana. Murtas C, Allegri L, Ghiggeri GM. Circulating antipodocyte antibodies in membranous nephropathy: new findings. Am J Kidney Dis. 2013;62(1):12-5. [PubMed link]
- 7. ETIOLOGÍA a) NM PRIMARIA - La mayoría (62-86% en diferentes series). - Anticuerpos contra antígenos del podocito: 70-80% Autoanticuerpos frente al receptor tipo M de la fosfolipasa A2 secretora (Ac anti-PLA2R) expresado en podocitos. * NM congénita: madre con deficiencia de EPN presente en los podocitos, se sensibiliza y transfiere IgG anti-EPN al feto.
- 8. ETIOLOGÍA • Las madres se hacen inmunizadas porque tienen deficiencia de endopeptidasa neutra debido a mutaciones en su gen. • Ronco P, Debiec H. New insights into the pathogenesis of membranous glomerulonephritis. Curr Opin Nephrol Hypertens. 2006;15:258-63. [PubMed link]).
- 9. b) NM SECUNDARIA Formación in situ de los complejos inmunes en el espacio subepitelial
- 10. NM SECUNDARIA • Seroalbúmina bovina: más frecuente en la infancia, asociada a la leche de vaca. • Antigeno en la vertiente externa de la pared capilar, como responsables de GM del niño. • Desaparece con la interrupción del alimento Debiec H, Lefeu F, Kemper MJ y cols. Early-childhood membranous nephropathy due to cationic bovine serum albumin. N Engl J Med 2011; 364:2101-2110 [Pubmed]
- 11. PATOGENIA 1. Formación in situ de inmunocomplejos en la zona subepitelial. Tres mecanismos posibles: a) Antígenos del podocito (idiopática): PLA2R,EPN (endopeptidasa neutra) , Thrombospondin type-1 domain-containing 7ª THSD7A. Antigenos Vs aldose reductase, superoxide dismutase 2, and alpha- enolase. b) Antígenos (pequeño tamaño, catiónicos)que atraviesan la barrera y se unen con Ig en zona subepitelial (seroalbúmina bovina). c) Inmunocomplejos que se disocian , atraviesan la barrera y vuelven a reconstituirse en zona subepitelial
- 12. PATOGENIA 2. Los depósitos de IC, activan el complemento que alteran la estructura del podocito provocando proteinuria masiva mediante la formacion de CAM. No se observa infiltrado celular inflamatorio ni lisis celular. 3. Engrosamiento de la MBG por sobreproduccion de varios componentes de la matriz extracelular. Parece que es por el aumento de TGF-β por parte del podocito y aumento de los receptores de TGF- β en respuesta a C5b-C9
- 13. PATOGENIA 4. Afectación tubulointersticial es la común a todas las glomerulopatías proteinúricas con sobrecarga proteica a nivel tubular y activación de la células tubulares (sobreexpresión de genes proinflamatorios y profibrogénicos y reclutamiento de células inflamatorias a nivel intersticial)
- 14. ETIOLOGÍA • Enf neoplásicas- 5-10% de todas las NM. • 10-20% de todas las nefritis lúpicas (son de clase V ). Algunas sólo presentan afectación renal. • AR: 7% de los tratados con penicilamina, 3% de los tratados con sales de oro, y también en ausencia de estos fármacos. • VHB: áreas endémicas (Asia) y generalmente en niños
- 15. ANATOMÍA PATOLÓGICA Microscopio óptico: -Engrosamiento difuso de la MBG que puede no ser identificada en las estadíos iniciales (I,II). -Las tinciones que mejor valoran la MBG son el PAS y la metamina argénticas (“spikes”) - Resto del glomérulo es normal, si hay hipercelularidad orienta a causa secundaria (LES). - El grado de afectación túbulointersticial marca el grado de insuficiencia renal y el pronóstico
- 16. Glomérulo sin proliferación ni infiltración celular Membranas engrosadas de forma difusa y global
- 17. “Spikes” de la membrana basal (Tinción de metamina argéntica)
- 18. Inmunofluorescencia. • Patrón granular en capilares glomerulares difusa y global (IgG,C3) • Pueden aparecer inmunoreacción en menor cuantía con IgA, cad ligeras yƙ ʎ • IgG4 predomina en idiopáticas • IgG1,2,3 predominan en las secundarias • La presencia de depósitos en otras localizaciones y la inmunoreactividad con otros anticuerpos y fracciones del complemento es caracteristica de secundarias (LES).
- 19. IgG Patrón granular a nivel de las asas capilares
- 20. Estadio I: Depósitos subepiteliales con leve reacción de membrana basal. En este estadio no forman “spikes”
- 21. Estadio II: Numerosos depósitos subepiteliales y reacción de membrana, “spikes”
- 22. Estadio III: Englobamiento de todo el depósito por la membrana basal. Estadio IV: reabsorción de los depósitos
- 23. Depositos subepiteliales : causa primaria La presencia de depósitos mesangiales y/o subendoteliales sugieren una secundaria.
- 24. MANIFESTACIONES CLINICAS - NM idiopática aparece en >30 años ( 80-95%) - La incidencia máxima es en la 5ª década y más en varones. 2H:1M. - Presentación clínica: - Sd nefrótico (80%). - Proteinuria asintomática +/- hematuria (20%). - HTA (30%, generalmente asociada a insuficiencia renal). - Trombosis de vena renal (20%)
- 25. MANIFESTACIONES CLINICAS - Grado variable de ERC - Deterioro agudo de función renal: * Hipovolemia grave secundaria a SN * Trombosis de vena renal
- 26. LABORATORIO - Proteinuria - Hematuria microscópica ( frecuente) - Anticuerpos antiPLA2R: importancia diagnóstica y se asocia con la actividad clínica. - Aunque tenga participación del complemento en la patogenia, generalmente los niveles del complemento son normales y la hipocomplementemia sugiere una causa secundaria. - Niveles elevados urinarios de C5b-C9 indican que está en fase activa.
- 27. LABORATORIO - Predisposición genética: HLA-DR3, HLA-B8. *En pacientes japoneses, fuerte asociación con HLA-DR2. - En la NM idiopática no deberían hallarse: ni crioglobulinas ni anas, ni ancas, ni fr.
- 28. EVOLUCIÓN Y PRONÓSTICO Remisión espontánea completa: • Niños (la mayoría) ENP,seroalbúmina bovina… • Adultos(20% y remisión parcial otro 20%. Puede ser retardada: 18-24 meses)
- 29. Spontaneous Remission of Nephrotic Syndrome in Idiopathic Membranous Nephropathy. • En un estudio multicéntrico español reciente, que revisó la evolución a largo plazo de más de 300 casos de NM con síndrome nefrótico que no habían sido tratados con corticosteroides u otros inmunosupresores, se confirmaron estos datos, pero se observó también que la aparición de remisión espontánea puede verse en pacientes con graves proteinurias al comienzo de la enfermedad. Polanco N, Gutiérrez E, Covarsí A y cols. Spontaneous Remission of Nephrotic Syndrome in Idiopathic Membranous Nephropathy. J Am Soc Nephrol 2010; 21:697-704. [Pubmed]
- 30. Spontaneous Remission of Nephrotic Syndrome in Idiopathic Membranous Nephropathy. • Otros aspectos interesantes a destacar son que la gran mayoría de remisiones aparecieron en los primeros dos años de la enfermedad y que la proteinuria no desapareció abruptamente, sino que mostró un descenso gradual. • Los factores que significativamente predijeron una remisión espontánea fueron la función renal y la cuantía de la proteinuria en el momento del diagnóstico de la enfermedad, el tratamiento con IECA ó ARB y la reducción de más de un 50% de la proteinuria basal durante el primer año de evolución. • El pronóstico a largo plazo de los enfermos con remisión espontánea completa o parcial fue excelente, con muy escasas recaídas (6%) y una supervivencia renal del 100%. No se conocen los mecanismos implicados en estas remisiones espontáneas.
- 31. EVOLUCIÓN Y PRONÓSTICO Recidivas 15-30% (tanto en remisiones espontáneas como en las inducidas por el tratamiento) ERC terminal 14% a los 5 años y 35% a 10 años
- 32. Factores de mal pronóstico: - Proteinuria persistente - Elevación de creatinina plasmática al diagnóstico - Afectación túbulointersticial en el momento del diagnóstico - Varones - Edad avanzada - HTA - El grado de la afectacion histologica no se correlaciona con el peor pronostico.
- 33. Factores de buen pronóstico: - Mujeres, niños - Jóvenes - Proteinuria no nefrótica - Función renal normal en los primeros 3 años.
- 34. TRATAMIENTO
- 35. a) Recomendaciones generales - Dieta hiposódica - BSRAA (dosis máxima que tolere, vigilando la función renal, K y la PA) - Diuréticos si precisa - Control DLP (LDL<100 mg/dl) - Control de la PA (<130/80). b) Tratamiento específico (NM idiopática) Terapia muy debatida debido al alto porcentaje (30-35%) de remisiones espontáneas.
- 36. 1. Corticoides - Históricamnete fueron el pilar fundamental. - Se ha demostrado que no tienen un mayor impacto en la evolución de la NM, exceptuando un subgrupo que es sensible a los CE. No dar CE en monoterapia
- 37. Tratamiento • KDIGO recomiendan la instauración de tratamiento inmunosupresor solamente en aquellos pacientes que mantienen proteinuria nefrótica tras un período de observación de al menos 6 meses y siempre que la proteinuria no tenga una clara tendencia a la disminución durante dicho período. • Se excluyen pacientes con incremento de crea >30% durante periodo observacional. FG<30, complicaciones del Sx nefrotico.
- 38. Tratamiento • Aticuagulacion: • KDIGO recomiendan su instauración en pacientes con hipoalbuminemia importante (<2-2.5 g/dl) que presenten además otros factores de riesgo para trombosis: obesidad, antecedentes previos de trombosis o predisposición genética a la misma, insuficiencia cardiaca congestiva, inmovilización ó cirugía abdominal u ortopédica reciente. Kidney Disease:Improving Global Outcomes (KDIGO) Glomerulonephritis Work Group. KDIGO Clinical Practice Guideline for Glomerulonephritis. Kidney Int Supplements 2012; 2: 139274.http://www.kdigo.org/clinical_practice_guidelines/pdf/CKD/KDIGO_2012 _CKD_GL.pdf
- 39. 2. Corticoides+alquilantes -40% RC -30% RP -Insuf renal progresiva 10% -Seguimiento 10 años. -Mayor probabilidad de RC o RP (88%vs 47%) y de mejor sobrevida renal (92% vs 60%) en comp con placebo. *MPS 1 g x 3 dias y PDN 0,5 mg/kg/d (meses 1,3,5). *Clorambucil o ciclofosfamida oral 1,5-2 mg/kg/d meses (2,4,6) -Resultados que se han confirmado con otros estudios * Ponticelli et al. A 10-year follow-up of a randomized study with methylprednisolone and chlorambucil in membranous nephropathy.Kidney Int 1995;48:1600-4
- 40. 3. Ciclosporina (menos complicaciones) 51 pacientes *3,5 mg/kg/d CsA + PDN 0,15 mg/kg ( 26 sem) *RC,RP 75% *Tras observación 78 sem, persistían en remisión 39% * Cattran et al. Cyclosporin in idiophatic glomerular disease associated with the nephrotic syndrome: workshop recommendations.Kidney Int 2007;72:1429
- 41. 4. Tacrolimus - Estudio prospectivo, multicéntrico, controlado. - Monoterapia con TCR 0,5 mg/kg/d separados en dos dosis dia hasta los 6 meses, luego retirada lenta hasta los 12 meses. ( pauta nstra consulta) (25 pacientes) vs grupo control (23 pacientes) - 12 meses - Remisión 94% a 18 meses frente al 35% * Praga et al. Tacrolimus monotherapy in membranous nephropathy:a randomized controlled trial. Kidney Int 2007;71:924-30
- 42. 5. MMF Pequeños estudios controlados: a)Similares resultados de MMF+ CE con el régimen de Ponticelli (41 pacientes) b)Similares resultados al manejo conservador (36 pacientes) No eficaces en monoterapia
- 43. 6. Rituximab Anti CD 20. Bx renal CD20. • RC o RP 60% con 4 dosis semanales 375 mg/m2 (2 series de 23 pacientes) • RC o RP 80% a los 24 meses con 4 dosis semanales y retratamiento a los 6 meses * Ruggenenti et al. Effects of rituximab on morphofunctional abnormalities of membranous glomerulopathy. Clin J Am Soc Nephrol 2008;3:1652-9. * Fervenza et al. Rituximab therapy in idiopathic membranous nephropathy:a2-year study. Clin J Am Soc Nephrol 2010;5:2188-98
- 44. Mas rituximab. • A trial of rituximab can be considered after a careful evaluation of the potential risks and benefits of further immunosuppression. Weak evidence suggests that a clinically relevant response to rituximab may be less likely in patients with a creatinine clearance below 75 mL/min per 1.73 m2 . • La proteinuria no selectiva tan elevada de estos pacientes podría llevar a una pérdida teórica del rituximab por la orina y, por lo tanto, disminuir la eficacia del fármaco. Literature review current through: Mar 2016. | This topic last updated: Nov 12, 2015.
- 45. Objetivos • Es importante recalcar que, mientras que en otras entidades como la nefropatía IgA el pronóstico de pacientes con proteinuria >1g/24h es desfavorable, en la NM existe una tolerancia mayor a cuantías superiores de proteinuria.
- 46. Objetivos • De hecho la inducción de remisión parcial (proteinuria <3.5 g/24h) se asocia a una supervivencia renal significativamente superior a la no remisión, y el mantenimiento de proteinurias entre 1-3.5 g/24h a lo largo del seguimiento no se asocia al deterioro de función renal observable en otras nefropatías. • Por tanto, aunque el objetivo óptimo sería la consecución de una remisión completa, la obtención de remisión parcial puede considerarse satisfactoria.
- 47. Tratamiento de GN membranosa: 1º Periodo de observación (6 meses) con BSRAA. Remiten espontáneamente el 30% 1b 2º Si persiste proteinuria de rango nefrótico y eFG >30 ml/min: 1 b a) CFM+CE 6 meses (Ponticelli) b) ICN 12 meses (retirada gradual) No tto IS si cr>3,5 mg/dl o FG< 30 ml/min Recaídas: mismo régimen que en el que consiguió remisión ( CFM+CE sólo una vez más) - No monoterapia con CE ni MMF - No recomendación RTX
- 48. Casos especiales MPS 1 g por 3 dias y PDN 0,5mg/kg/dia ( meses 1,3,5+ CFM oral 1,5-2mg kg/dia meses 2,4,6. (Ponticelli) Recaidas: Misma pauta que se uso en el tratameinto que se logro la remision. Si se uso la pauta de CE y CFM repetir una sola vez.
- 49. NM Y TX RENAL - Recidiva varía según series: 10%-40% - No parece que la IS postrasplante proteja - Hallazgos histológicos son previos a la aparición de Proteinuria. - No clara relación con títulos de Ac antiPLA2R antes del Tx. - parece que los titulos de Ac antiPLA2R postrasplante puede predecir la recidiva y la respuesta al tratamiento.
- 50. NM Y TX RENAL • NM de novo en Tx - 30% de sd nefrótico en Tx (después de la glomerulopatía del Tx) - Patogenia desconocida - Se asocia con rechazo crónico no con Ac antiPLA2R
- 51. Conclusiones • GNM: es la causa más común de síndrome nefrótico en adultos. • La patogenia: PLA2R. • La clinica es variable. • Presenta un alto porcentaje de remision espontanea. • Objetivos de tratamiento. • Tratamiento inmunosupesor consigue buenos resultados
- 52. Gracias!
