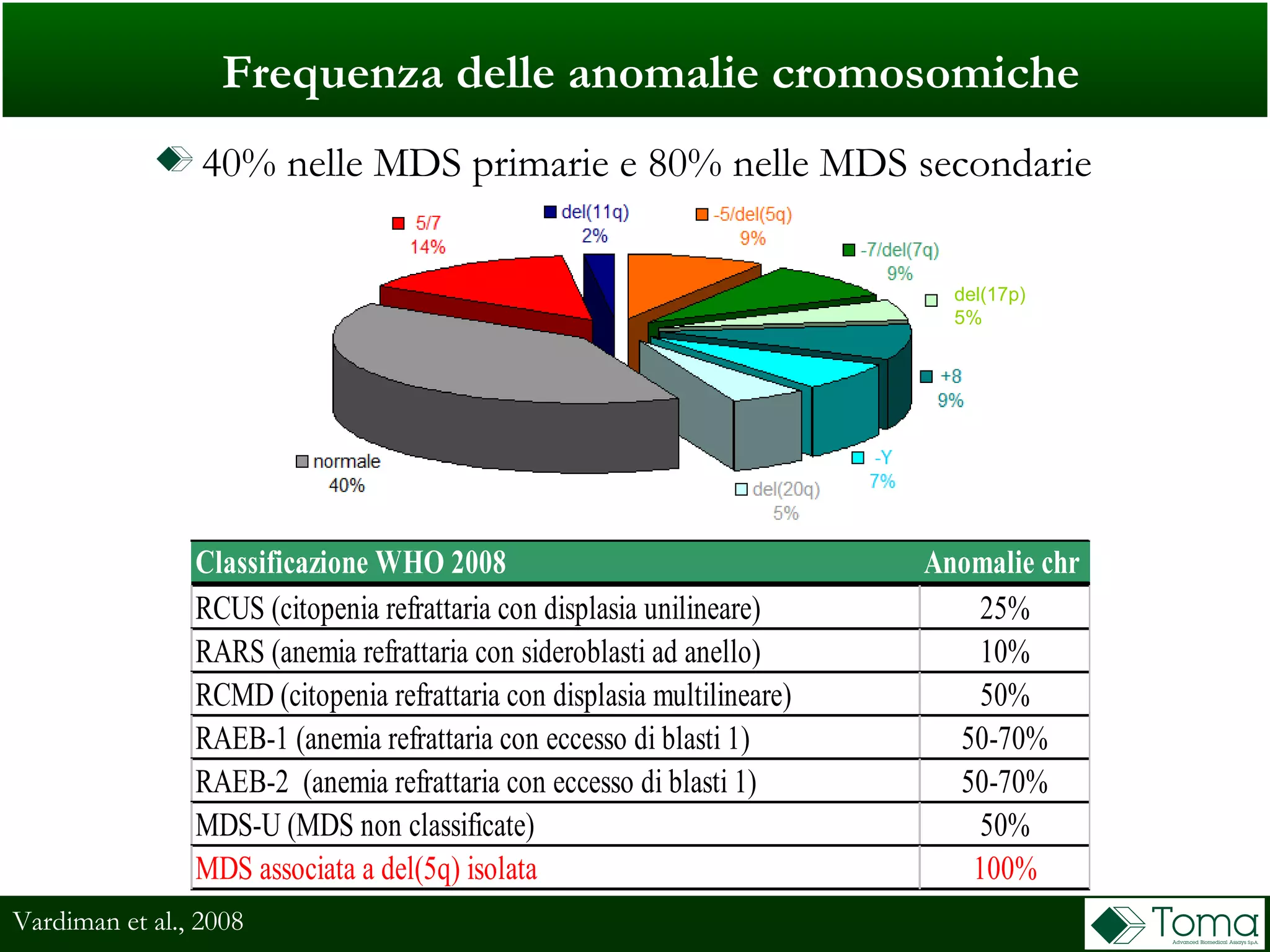
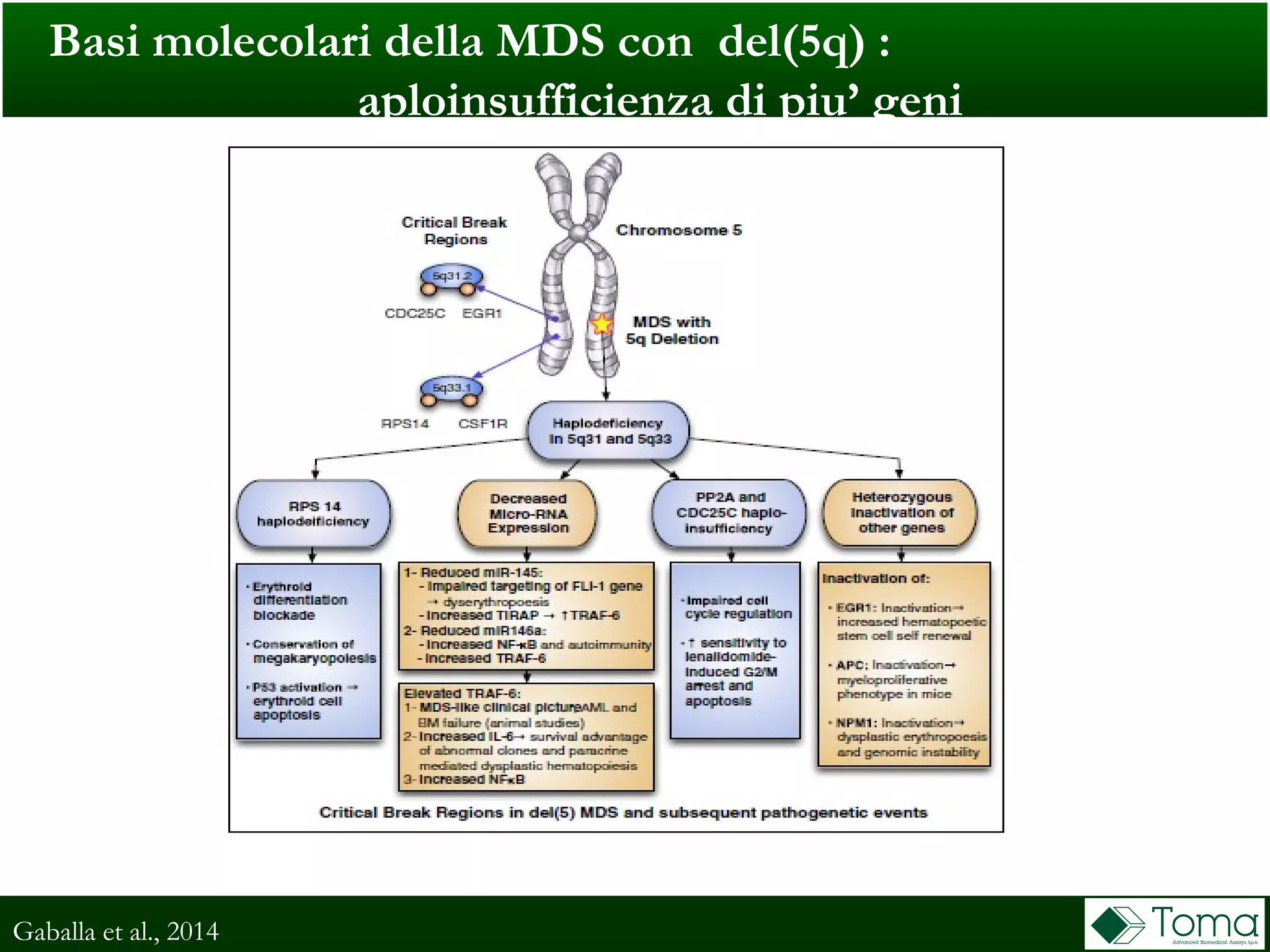
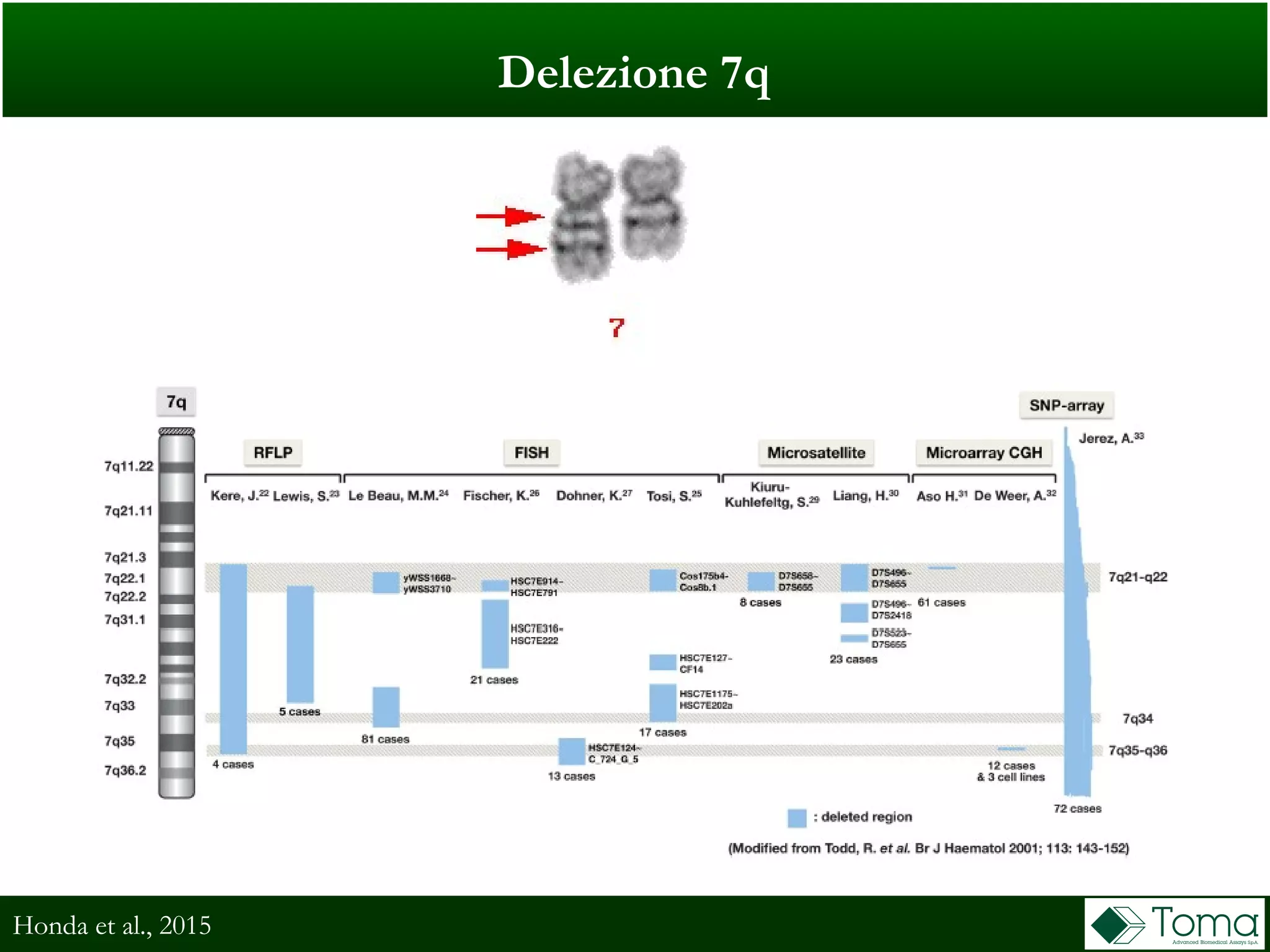
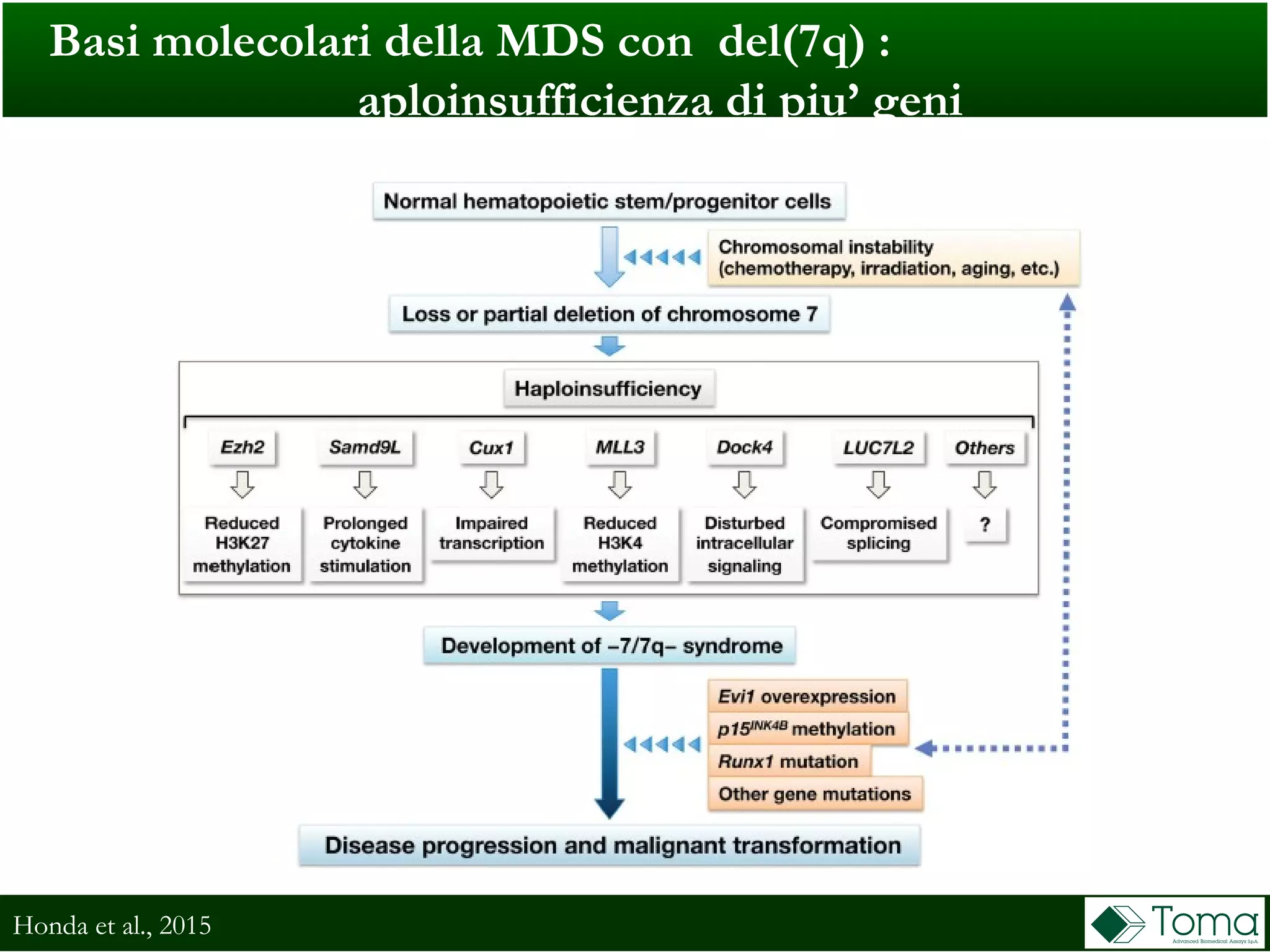
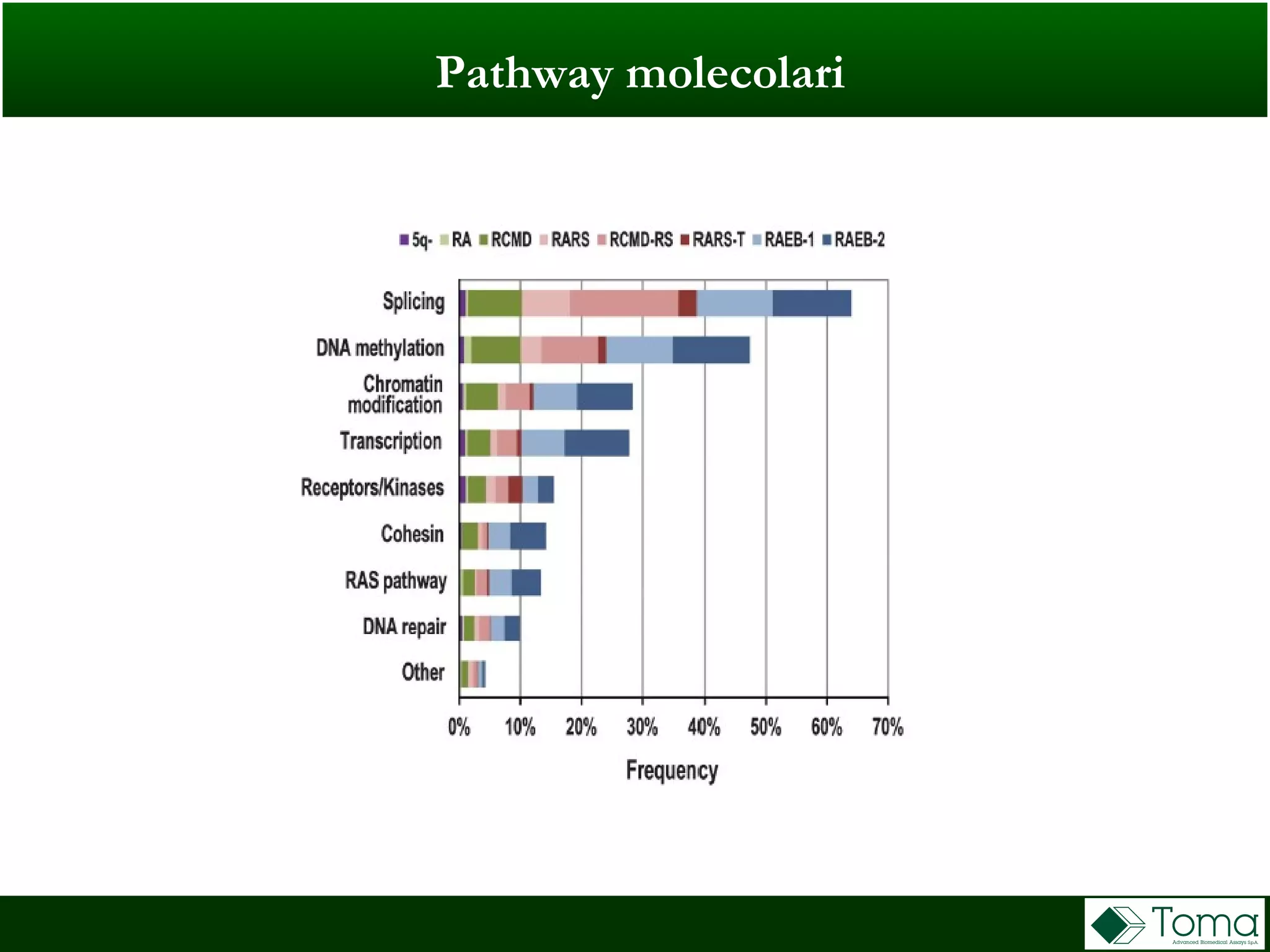
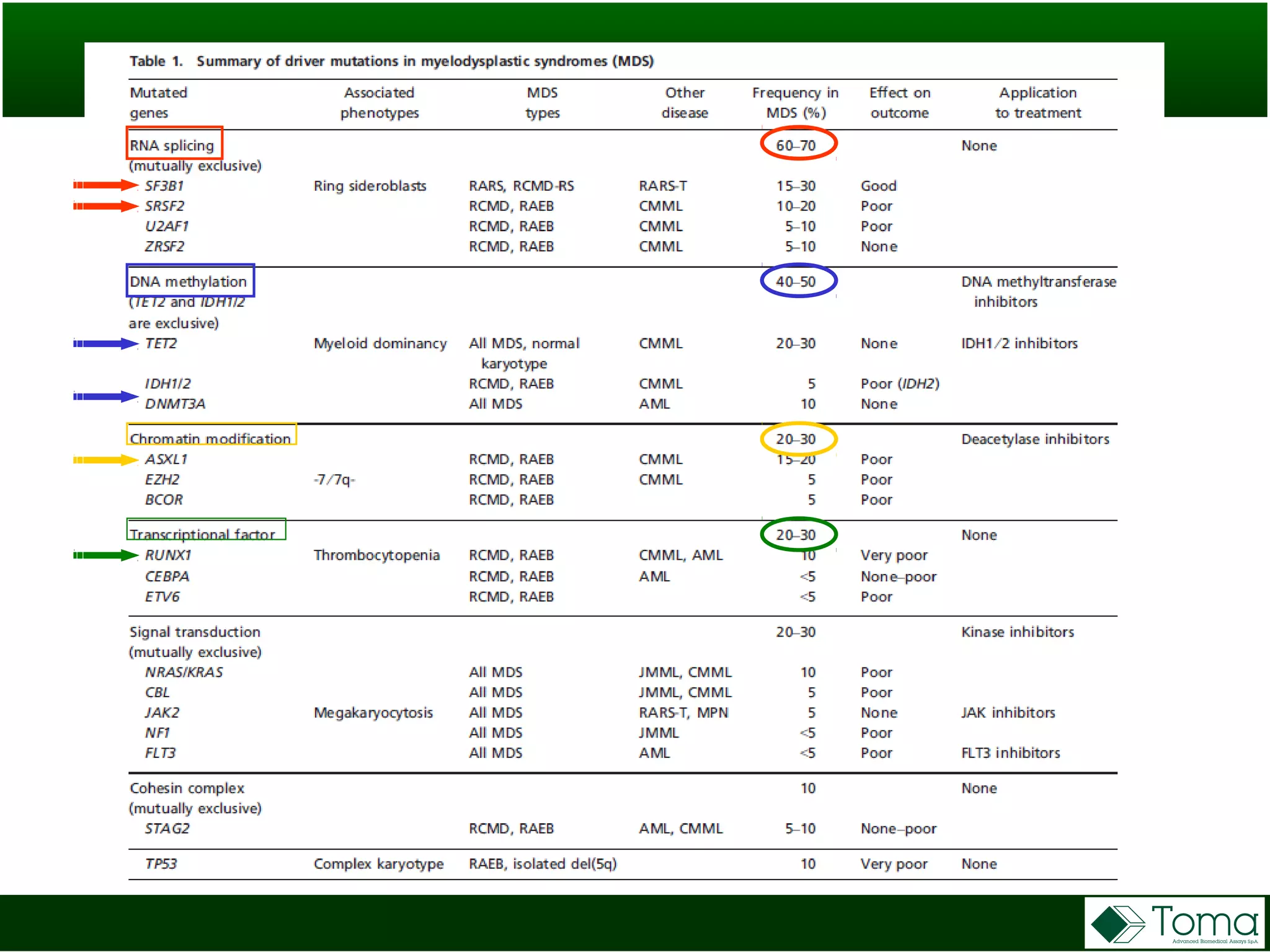
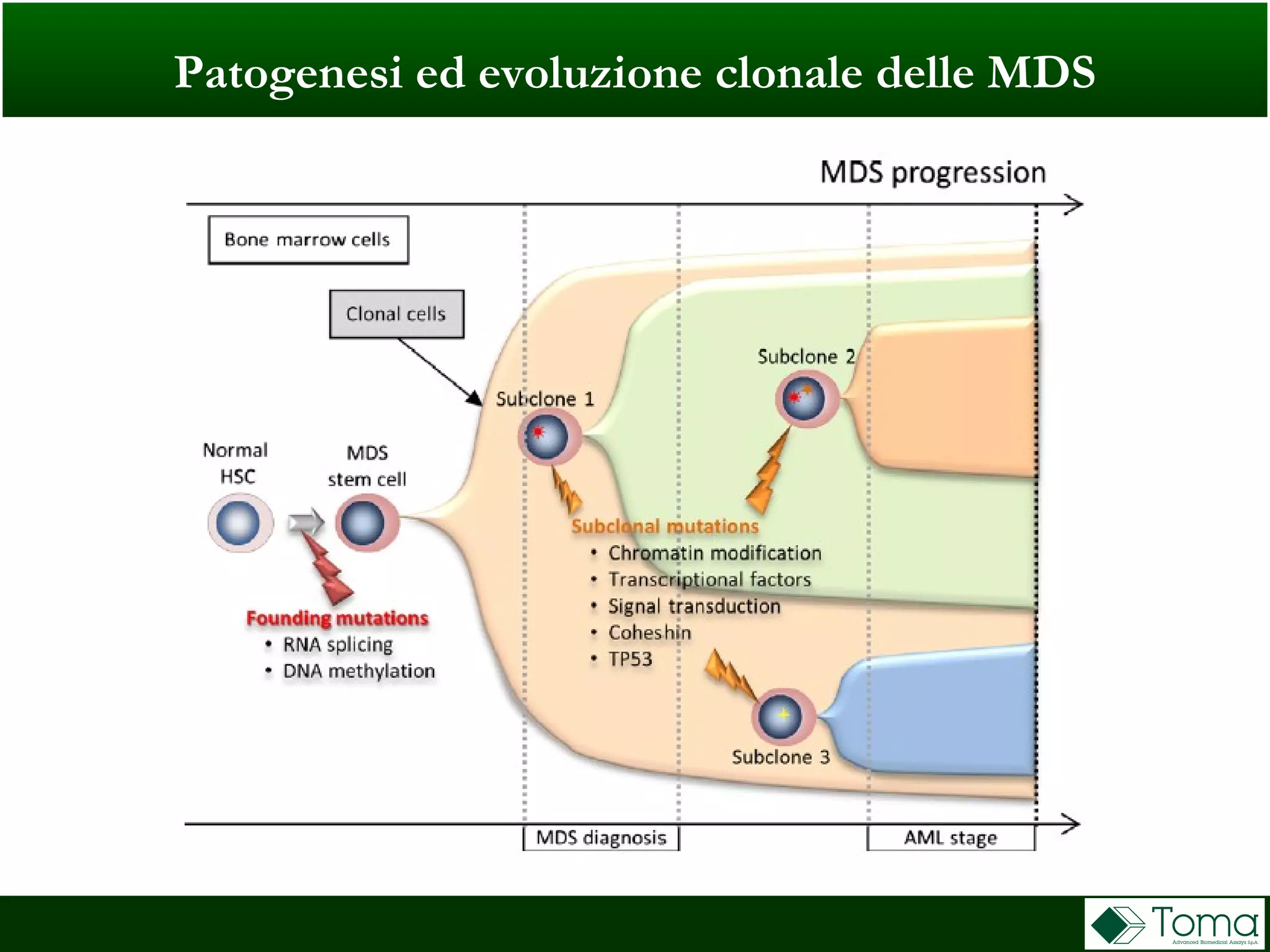
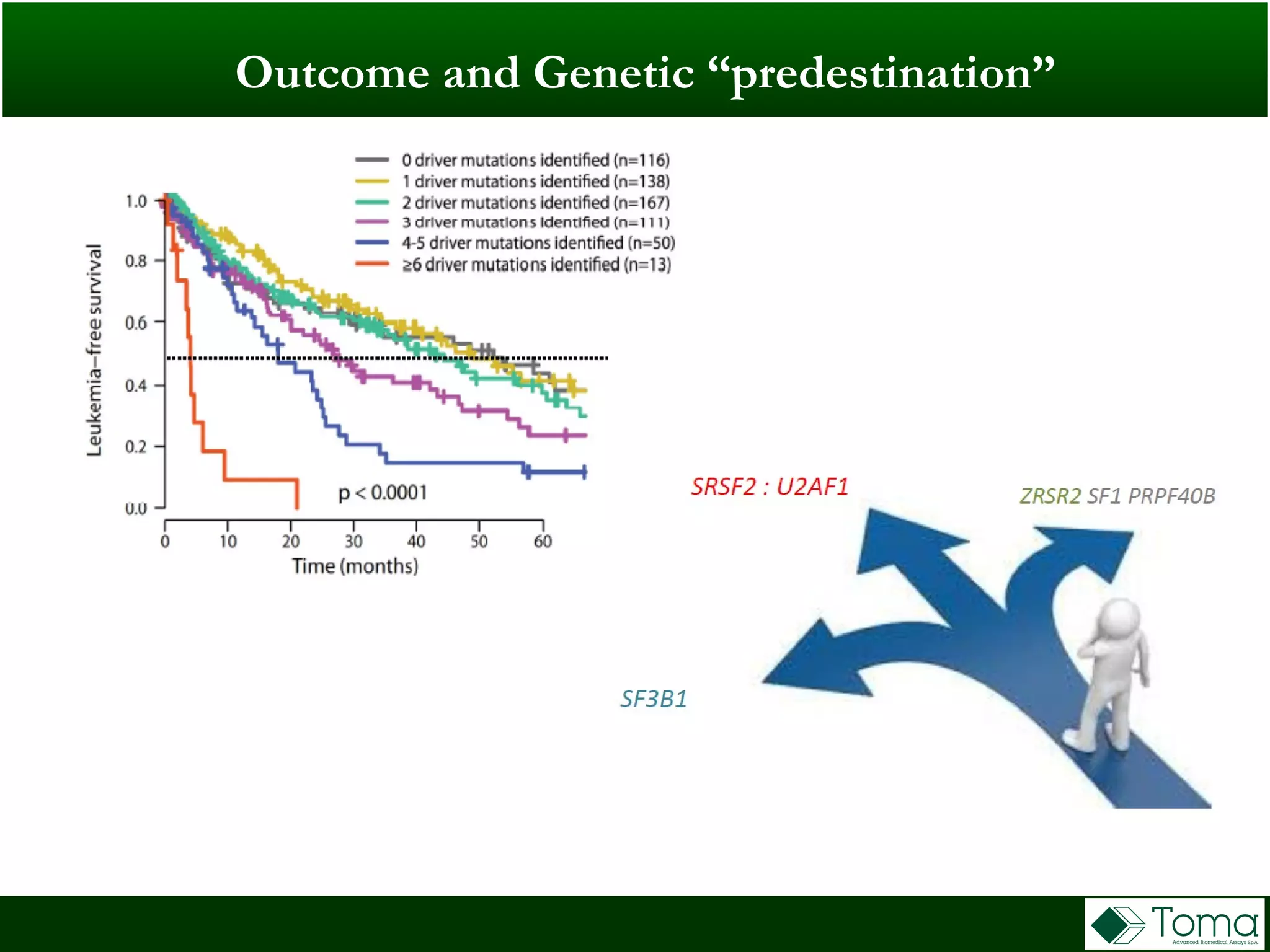
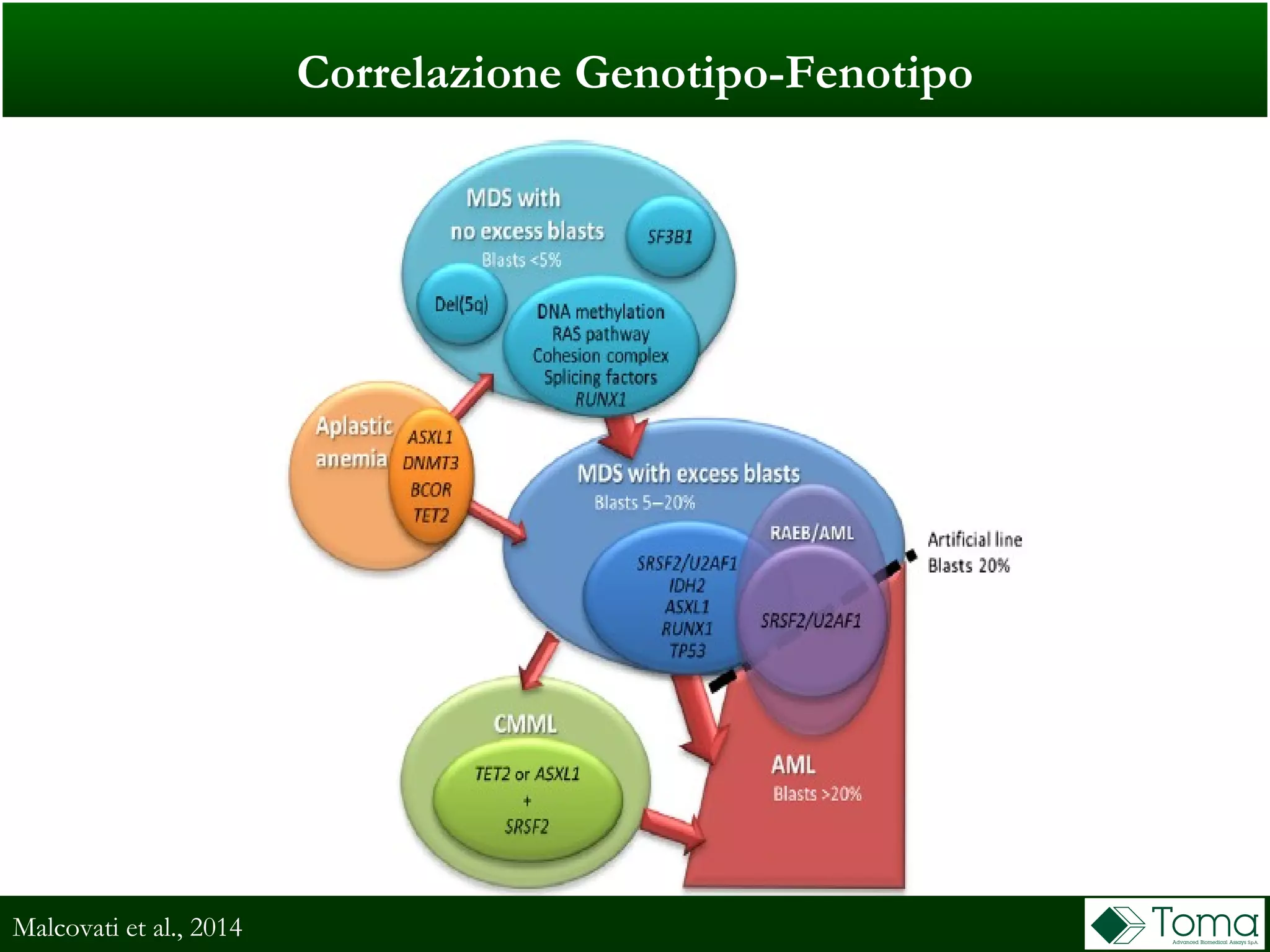
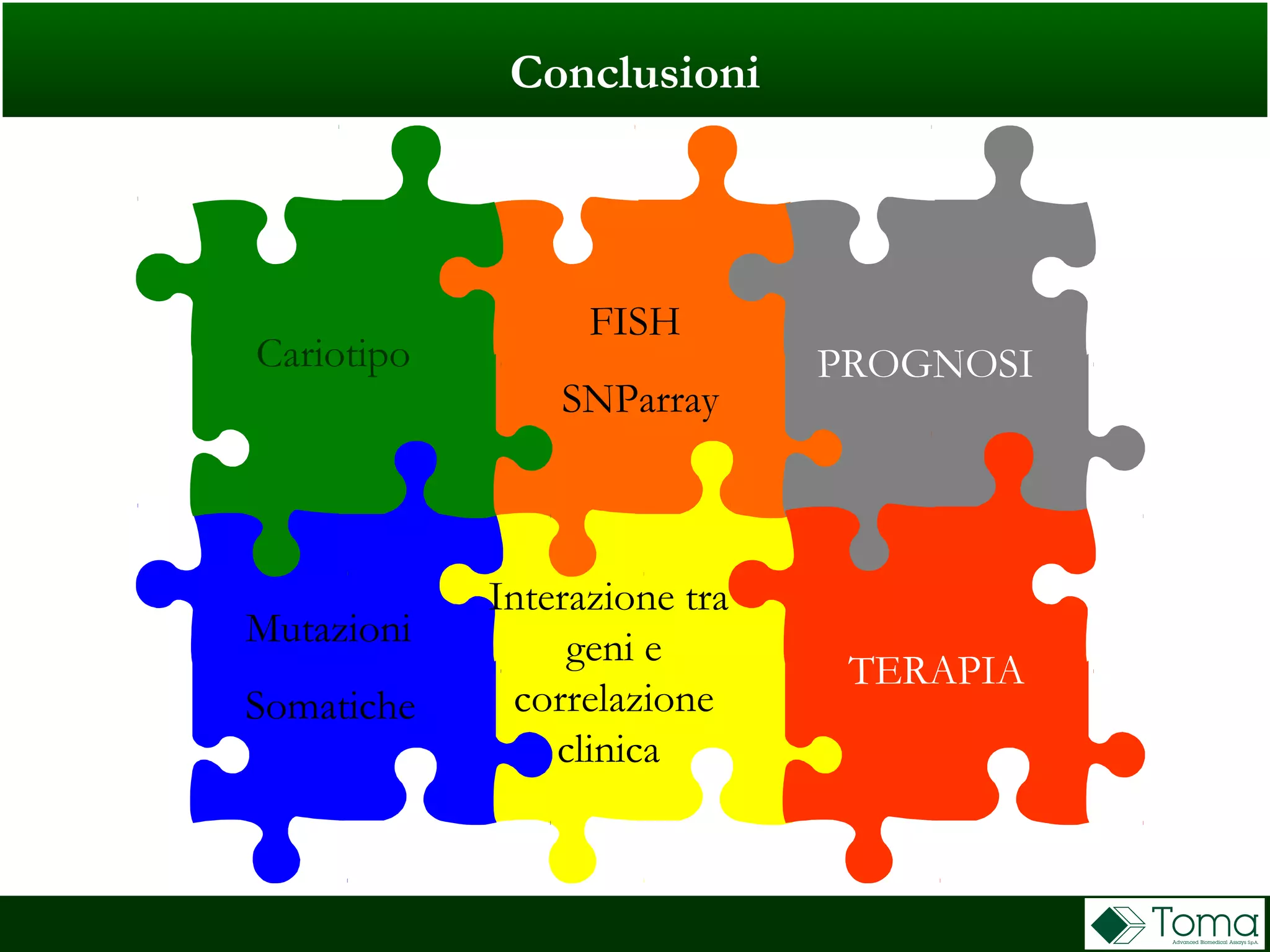
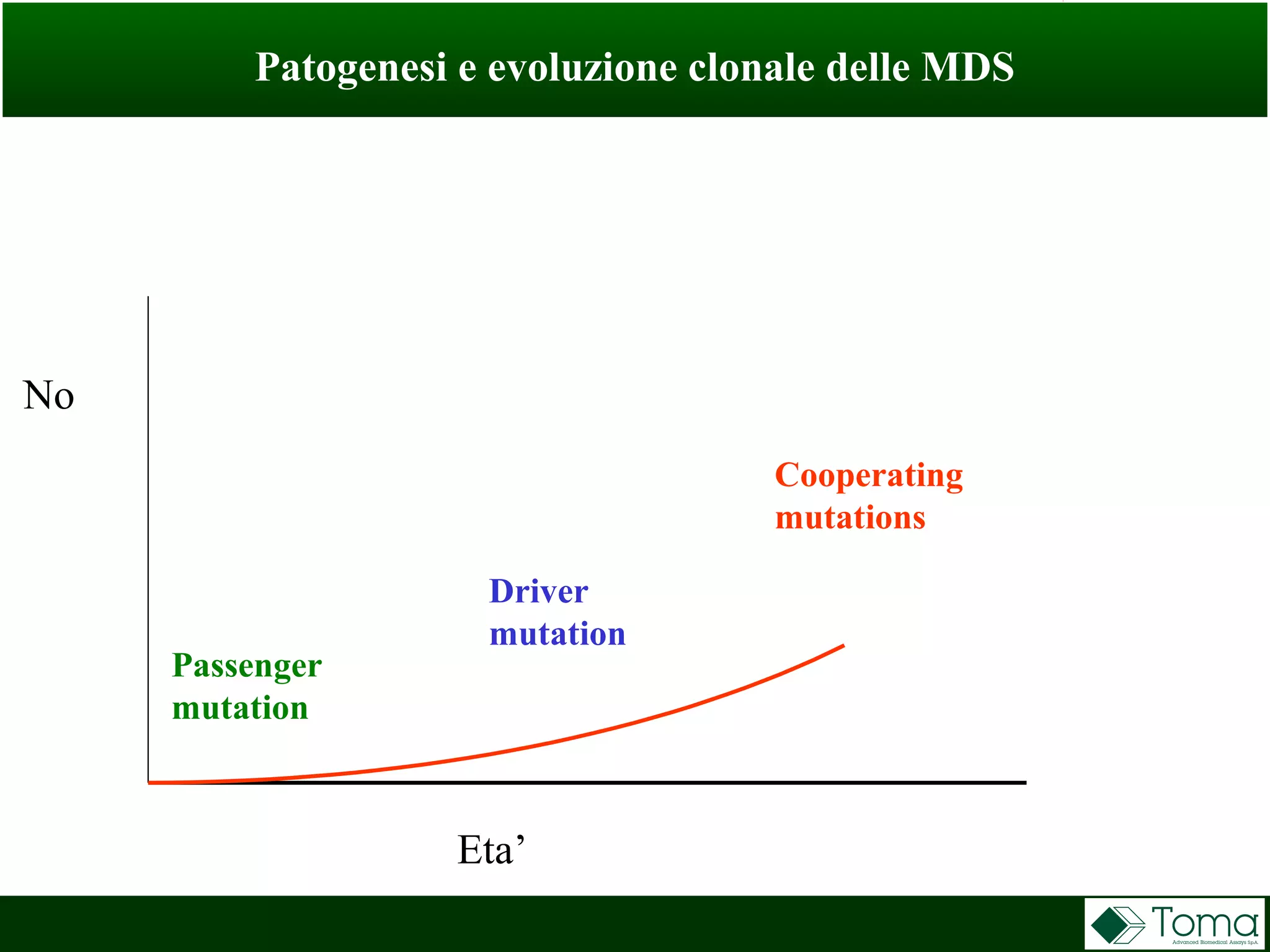
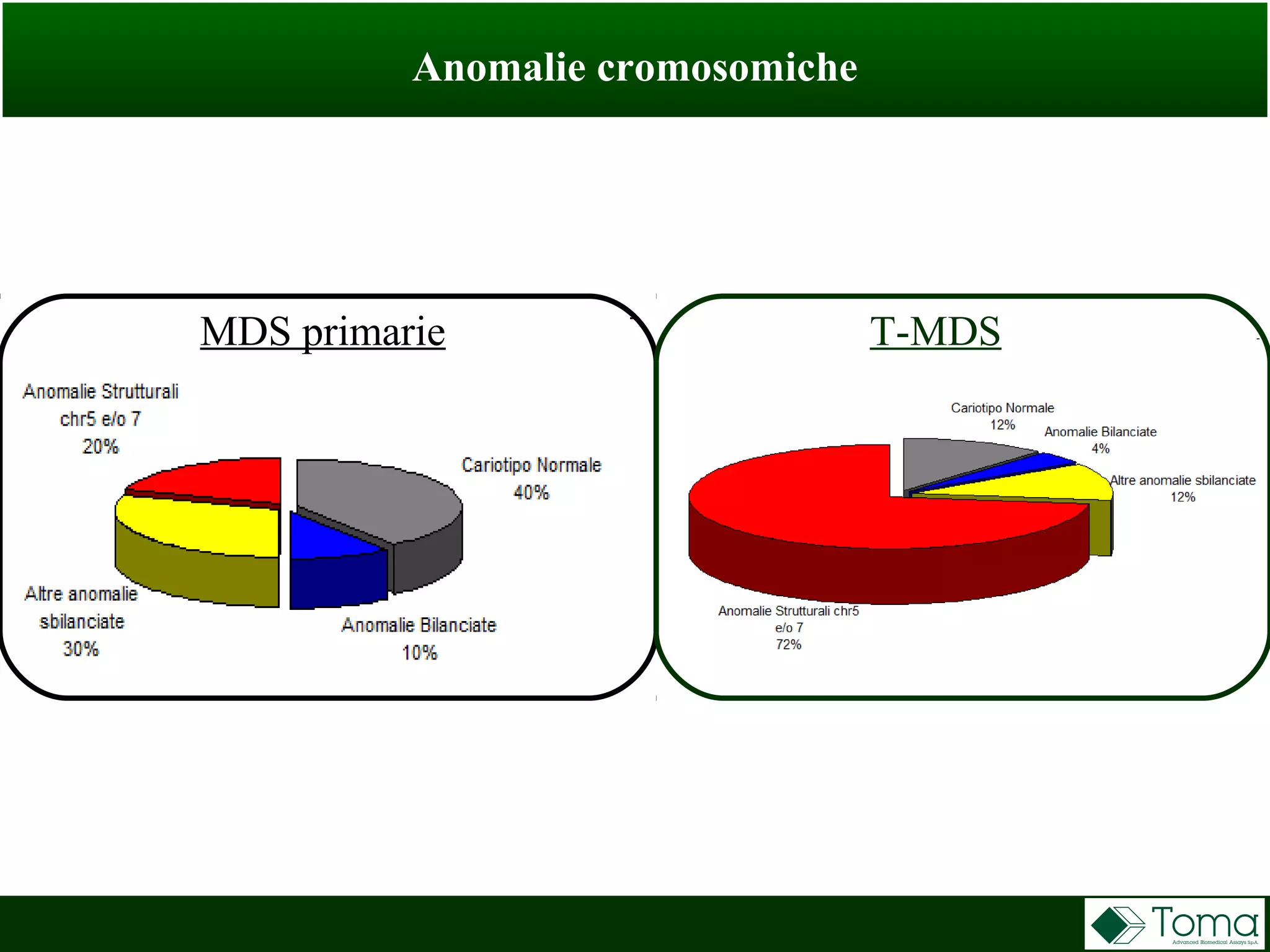
Il documento discute il primo incontro di genetica oncologica, focalizzandosi su come il cariotipo e le tecniche molecolari come il NGS stiano trasformando la diagnosi delle sindromi mielodisplastiche (MDS). Sono analizzati il ruolo delle anomalie cromosomiche e delle mutazioni somatiche nella prognosi e patogenesi delle MDS, insieme a raccomandazioni diagnostiche e classificazioni aggiornate. Infine, si evidenziano le tecniche di laboratorio per la diagnosi e la prognosi delle MDS, inclusi metodi innovativi come il FISH su cellule CD34+ e le analisi cromosomiche alternative.