Síntesis glucosa hígado
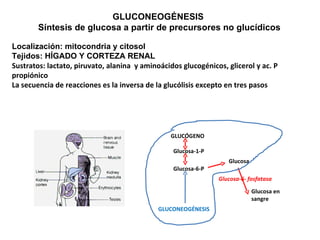
- 1. GLUCONEOGÉNESIS Síntesis de glucosa a partir de precursores no glucídicos Localización: mitocondria y citosol Tejidos: HÍGADO Y CORTEZA RENAL Sustratos: lactato, piruvato, alanina y aminoácidos glucogénicos, glicerol y ac. P propiónico La secuencia de reacciones es la inversa de la glucólisis excepto en tres pasos GLUCÓGENO Glucosa-1-P Glucosa-6-P Glucosa Glucosa en sangre GLUCONEOGÉNESIS Glucosa-6- fosfatasa
- 2. 2ATP + 2NADH - 4ATP – 2GTP - 2NADH 1º Rodeo 2º Rodeo 3º Rodeo
- 3. Precursores de la síntesis de glucosa Alanina
- 4. 1º Rodeo LACTICO PIRUVATO ALANINA Biotina: coenzima transportador de CO 2 . Deriva de vit.B8
- 5. Piruvato carboxilasa: mecanismo catalítico Piruvato + CO 2 + H 2 O + ATP -> oxalacetato + ADP + Pi + 2 H + Δ G´º = - 2,1 KJ/mol
- 6. Fosfoenolpiruvato carboxiquinasa: Mecanismo catalítico Oxalacetato + GTP ↔ fosfoenolpiruvato + CO 2 + GDP Δ G´º = 2,9 KJ/mol
- 7. 2º Rodeo Conversión de la fructosa-1-6-bifosfato en fructosa-6-fosfato (fructosa-1-6,bifosfatasa, FBPasa). Fructosa-1,6-bifosfato + H 2 O -> fructosa-6-fosfato + Pi ΔG´º = - 16,3 KJ/mol Conversión de la glucosa-6-fosfato en glucosa (glucosa-6-fosfatasa). 3º Rodeo Glucosa 6-fosfato + H 2 O -> Glucosa + Pi ΔG´º = - 13,8 KJ/mol
- 8. Balance global de la gluconeogénesis 2 piruvato + 4 ATP + 2 GTP + 2 NADH + 6 H 2 O glucosa + 4 ADP + 2 GDP + 6 Pi + 2 NAD + + 2H + Δ G = - 16 Kj/ mol
- 9. Regulación Glucoólisis y Gluconeogénesis
- 10. FRUCTOSA-1,6-BP FRUCTOSA-6-P FRUCTOSA-6-P FRUCTOSA-1,6-BP FRUCTOSA-1,6-BI-FOSFATASA PFK-1 [Fructosa-2,6-BP] H 2 O Pi ATP ADP + - FRUCTOSA-6-P FRUCTOSA-2,6-BP Fructosa-2,6- BI-fosfatasa PFK-2 ↑ FRUCTOSA-2,6-BP GLUCOLISIS GLUCONEO GÉNESIS + - ↓ FRUCTOSA-2,6-BP GLUCOLISIS GLUCONEO GÉNESIS - + PFK-2 (activa) FBPasa (inactiva) PFK-2 (inactiva) FBPasa (activa) OH O- P Glucagón PKA Fosfoprotein fosfatasa Fructosa 6 P
- 13. La fase oxidativa genera por cada molécula de glucosa; 2 moléculas de NADPH, 1 molécula de ribulosa-5-fosfato y una molécula de CO 2 . Consta de tres reacciones: La fase no oxidativa convierte 3 azúcares fosfato de 5 carbonos; en 2 azúcares fosfato de 6 carbonos y 1 azúcar fosfato de 3 carbonos
- 14. fase oxidativa Reacción 1 . Oxidación de la glucosa-6-fosfato a 6-fosfogluconolactona (glucosa-6-fosfato deshidrogenasa)
- 15. Reacción 2. Hidrólisis de la lactona a fosfogluconato (lactonasa). H 2 O Mg 2+
- 16. Reacción 3. Descarboxilación oxidativa a ribulosa-5-fosfato (6-fosfogluconato deshidrogenasa). La oxidación del grupo hidroxilo en C3 origina un β-cetoácido que se descarboxila con facilidad
- 17. La fase no oxidativa Isomerización y epimerización de la ribulosa 5-fosfato Las reacciones de la ribulosa 5- fosfato isomerasa y epimerasa tienen lugar con intervención de intermediarios enediol. En la reacción de la isomerasa, una base situada en el enzima elimina un protón de C1 de Ru5P a fin de formar un 1,2-enediolato y después adiciona un protón a C2 para formar R5P. En la reacción de la epimerasa, una base situada en el enzima elimina un protón en C3 para formar un 2,3-enediolato. A continuación se añade un protón al mismo átomo de carbono pero con inversión de la configuración para rendir Xu5P
- 18. Diagrama esquemático simplificado que muestra la ruta de seis pentosas (5C) a cinco hexosas (6C). Esquema de las reacciones no oxidativas de la ruta de las pentosas fosfato. Estas reacciones convierten pentosas fosfato de nuevo en hexosas fosfato, permitiendo que continúen las reacciones de oxidación. Los enzimas transaldolasa y transcetolasa son específicos de esta ruta; los otros enzimas también actúan en las rutas glucolítica o gluconeogénica. Cada reacción es reversible; las flechas unidireccionales sólo se utilizan para clarificar la dirección durante la oxidación constante de la glucosa 6-P.
- 19. Balance global 3 glucosa 6-P + 6 NADP + + 3 H 2 O -> 2 fructosa 6-P + gliceraldehído 3-P + 6 NADPH + 6 H + + 3 CO 2
- 20. Trancetolasa La trancetolasa cataliza la transferencia de un fragmento de dos carbonos (C1 y C2) desde un dador cetosa a un aceptor aldosa Carbanión estabilizado mediante unión al TPP
- 21. La rotura de un enlace carbono-carbono deja a menudo un par de electrones libre o carbanión en uno de los productos; la fuerte tendencia del carbanión a formar un nuevo enlace da lugar generalmente a un intermedio inestable. El anillo de tiazolio de la TPP estabiliza el intermedio carbanión al proporcionar una estructura electrofílica (deficiente en electrones) en la que los electrones del carbanión pueden deslocalizarse por resonancia. A las estructuras con estas propiedades se las llama frecuentemente “sumideros de electrones” La transcetolasa utiliza como coenzima al pirofosfato de tiamina con objeto de estabilizar el carbanión formado en la ruptura del enlace C2-C3 de la Xu5P. La reacción ocurre con los siguientes pasos: 1) Ataque nucleofílico del radical TPP al carbono carbonilito y posterior protonación. 2) desprotonación de C3 y rotura del enlace C2-C3, que da como productos G3P y el enzima unido a 2- (1,2-dihdroxietil)-TPP, que es un carbanión estabilizado por resonancia. 3) El carbanión C2 ataca al carbono aldehído de la R5P formando un aducto S7P-TPP. 4) Se elimina TPP con producción de S7P.
- 22. Transaldolasa La transaldolasa cataliza la transferencia de un fragmento de 3 carbonos desde un dador cetosa a un aceptor aldosa Carbanión estabilizado mediante formación de una base de Schiff protonada
- 23. El centro activo de la aldolasa (clase I), esta formado por un residuo de lisina para formar una base de Schiff con el carbono carbonilo, un residuo de cisteina que acepta un protón del grupo hidroxilo en el C4, que lo devuelve a un residuo de histidina tras la ruptura entre C3 y C4 Mecanismo de reacción: 1) El grupo ε-amino del resto de Lys forma una base de Schiff con el grupo carbonilo de 7SP. 2) Se forma un carbanión en C3 que es una base de Schiff estabilizada, en la ruptura aldólica entre C3 y C4 que elimina E4P. 3) El carbanión estabilizado por resonancia unido al enzima se adiciona al átomo de C carbonilico de GAP formando F6P ligado al enzima a través de una base de Schiff. 4) La base de Schiff se hidroliza regenerando el enzima activo y se libera F6P.
- 24. Regulación El NADPH regula el destino de la glucosa 6P
