EL AGUA 2º Bachillerato - Ver.2014
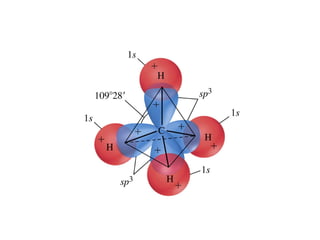
- 2. La molécula de agua. Forma y polaridad. Estructura electrónica del oxígeno y del hidrógeno. Hibridación del oxígeno En la molécula de agua. Forma de la molécula de agua. Polaridad de la molécula de agua.
- 3. La molécula de agua: puentes de hidrógeno.
- 5. La molécula de agua: puentes de hidrógeno.
- 6. La molécula de agua. Propiedades físicas. •Elevado calor específico: el calor específico del agua (la cantidad de calor, medida en julios, necesaria para elevar 1 °C la temperatura de 1 kg de agua) es muy elevado: gran parte del calor absorbido se usa para romper los puentes de hidrógeno que mantienen juntas las moléculas de agua. •Elevado calor latente de vaporización: los puentes de hidrógeno atraen las moléculas de agua líquida entre sí y hacen difícil el escape de éstas como vapor: por tanto se necesita un aporte relativamente alto de energía para vaporizar el agua y ésta tiene un punto de ebullición mucho más elevado que otras moléculas del mismo tamaño. •Movilidad molecular: la debilidad de los puentes de hidrógeno individuales significa que las moléculas individuales de agua se empujan continuamente unas a otras cuando están en fase líquida. •Cohesión y tensión superficial: los puentes de hidrógeno hacen que las moléculas de agua se «peguen» entre sí y también a otras moléculas (el fenómeno de la cohesión). En la superficie de un líquido, las fuerzas cohesivas que actúan hacia el interior producen una «tensión superficial», ya que las moléculas se atraen de forma especial entre sí.
- 7. La molécula de agua. Propiedades físicas. •Densidad y propiedades de congelación: a medida que el agua se enfría hacia su punto de congelación, las moléculas individuales se mueven más despacio, lo suficiente como para que cada una forme su máximo número de puentes de hidrógeno. Para ello, las moléculas de agua en el agua líquida deben apartarse dejando espacio suficiente para que quepan sus cuatro puentes de hidrógeno. Como resultado, el agua se expande según se congela, de modo que el hielo es menos denso que el agua líquida y, por tanto, flota sobre su superficie. •Formación de coloides: algunas moléculas tienen grandes fuerzas intramoleculares que impiden su disolución en agua, pero tienen superficies cargadas que atraen una cubierta de moléculas de agua. Esta cubierta asegura que las moléculas permanezcan dispersas por el agua, en vez de formando grandes agregados que podrían precipitar. Las partículas dispersas y el líquido que las rodea forman en conjunto un coloide.
- 8. La molécula de agua. Propiedades físicas. •Densidad y propiedades de congelación: a medida que el agua se enfría hacia su punto de congelación, las moléculas individuales se mueven más despacio, lo suficiente como para que cada una forme su máximo número de puentes de hidrógeno. Para ello, las moléculas de agua en el agua líquida deben apartarse dejando espacio suficiente para que quepan sus cuatro puentes de hidrógeno. Como resultado, el agua se expande según se congela, de modo que el hielo es menos denso que el agua líquida y, por tanto, flota sobre su superficie. •Formación de coloides: algunas moléculas tienen grandes fuerzas intramoleculares que impiden su disolución en agua, pero tienen superficies cargadas que atraen una cubierta de moléculas de agua. Esta cubierta asegura que las moléculas permanezcan dispersas por el agua, en vez de formando grandes agregados que podrían precipitar. Las partículas dispersas y el líquido que las rodea forman en conjunto un coloide.
- 11. La molécula de agua: cambios de estado.
- 12. Poder disolvente del agua.
- 13. Poder disolvente del agua.
- 14. Propiedades del agua. Capilaridad.
- 15. Poder disolvente del agua.
- 16. Poder disolvente del agua.
- 17. La molécula de agua. Importancia biológica. • Propiedades disolventes: permiten que el agua actúe como medio de transporte para solutos polares. Por ejemplo 1. movimientos de minerales en lagos y mares; 2. transporte por vía sanguínea y linfática en animales pluricelulares; 3. eliminación de desechos metabólicos tales como urea y amonio en la orina. • Flujo de transpiración: la columna continua de agua puede subir por el xilema de los vegetales a causa de la cohesión entre las moléculas de agua y la adhesión entre el agua y las paredes de los vasos del xilema. • Movilidad molecular: la naturaleza bastante débil de los puentes de hidrógeno individuales significa que las moléculas de agua se pueden mover fácilmente entre sí; esto permite que tenga lugar la osmosis (vital para la captación y movimiento del agua).
- 18. La molécula de agua. Importancia biológica. • Expansión por congelación: como el hielo flota, se forma en la superficie de charcas y lagos; aisla, por tanto, a los organismos del agua por debajo de él y permite que el hielo se descongele rápidamente cuando suben las temperaturas. Los cambios de densidad también mantienen la circulación en grandes masas de agua, favoreciendo el movimiento de nutrientes. ¡El hielo flotante significa, además, que los pingüinos y osos polares tienen donde estar de pie! • Funciones metabólicas: El agua se emplea directamente ... 1. Como reactivo (fuente de poder reductor) en la fotosíntesis. 2. Para hidrolizar macromoléculas en sus subunidades, en la digestión, por ejemplo. ... y es también el medio en que tienen lugar todas las reacciones bioquímicas. • Volatilidad/estabilidad: está equilibrada con las temperaturas de la Tierra, de forma que se mantiene un ciclo acuoso de evaporación, transpiración y precipitación. • Función de soporte: las fuerzas cohesivas entre moléculas de agua suponen que ésta no se comprime fácilmente y por eso es un excelente medio de soporte. Entre los ejemplos biológicos importantes se incluyen el esqueleto hidrostático (p. ej., la lombriz de tierra), la presión de turgencia (en partes herbáceas de plantas), el líquido amniótico (que soporta y protege el feto de mamíferos) y como medio general de soporte (en especial, para grandes mamíferos acuáticos como las ballenas).
- 19. La molécula de agua. Importancia biológica. • Propiedades lubricantes: las propiedades cohesivas y adhesivas del agua suponen que ésta es viscosa, convirtiéndola en un útil lubricante de sistemas biológicos. Por ejemplo, 1. líquido sinovial: lubrica muchas articulaciones de vertebrados; 2. líquido pleural: minimiza la fricción entre los pulmones y la caja torácica (costillas) durante la respiración; 3. mucus: permite el paso fácil de las heces por el colon y lubrica el pene y la vagina durante el coito. • Termorregulación: el elevado calor específico del agua supone que los cuerpos compuestos en gran parte de agua (las células son normalmente un 70-80 % agua) son muy termoestables y, por tanto, menos propensos al daño por calor con los cambios en las temperaturas ambientales. El elevado calor latente de vaporización del agua supone que un cuerpo puede enfriarse mucho con una mínima pérdida de agua. Este fenómeno es ampliamente utilizado por mamíferos (sudor) y reptiles (transpiración por la boca abierta), y puede ser importante en la refrigeración de hojas que transpiran. • Transparencia: el agua permite el paso de luz visible. Esto significa que la fotosíntesis (y las cadenas alimenticias asociadas) es posible en entornos acuáticos relativamente poco profundos.
