Ley de charles
•Download as DOC, PDF•
0 likes•1,491 views
documento y ejercicios sobre la ley de charles.
Report
Share
Report
Share
Recommended
More Related Content
What's hot
What's hot (19)
Cervantes canto lilianaelena_m12s3_unaleydelosgases

Cervantes canto lilianaelena_m12s3_unaleydelosgases
Viewers also liked
Viewers also liked (20)
Similar to Ley de charles
Similar to Ley de charles (20)
10 2-10-3 quimica- diana carolina burbano ruano guia no.4

10 2-10-3 quimica- diana carolina burbano ruano guia no.4
Clase termodinámica para colegio para docentes.pptx

Clase termodinámica para colegio para docentes.pptx
Recently uploaded
Recently uploaded (20)
Tema 19. Inmunología y el sistema inmunitario 2024

Tema 19. Inmunología y el sistema inmunitario 2024
2 REGLAMENTO RM 0912-2024 DE MODALIDADES DE GRADUACIÓN_.pptx

2 REGLAMENTO RM 0912-2024 DE MODALIDADES DE GRADUACIÓN_.pptx
Tema 10. Dinámica y funciones de la Atmosfera 2024

Tema 10. Dinámica y funciones de la Atmosfera 2024
Análisis de los Factores Externos de la Organización.

Análisis de los Factores Externos de la Organización.
La Sostenibilidad Corporativa. Administración Ambiental

La Sostenibilidad Corporativa. Administración Ambiental
🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx

🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx
PINTURA DEL RENACIMIENTO EN ESPAÑA (SIGLO XVI).ppt

PINTURA DEL RENACIMIENTO EN ESPAÑA (SIGLO XVI).ppt
SESION DE PERSONAL SOCIAL. La convivencia en familia 22-04-24 -.doc

SESION DE PERSONAL SOCIAL. La convivencia en familia 22-04-24 -.doc
Ley de charles
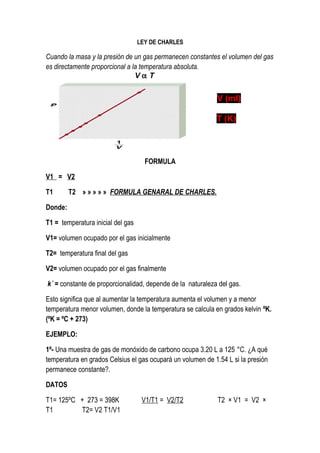
- 1. LEY DE CHARLES Cuando la masa y la presión de un gas permanecen constantes el volumen del gas es directamente proporcional a la temperatura absoluta. FORMULA V1 = V2 T1 T2 » » » » » FORMULA GENARAL DE CHARLES. Donde: T1 = temperatura inicial del gas V1= volumen ocupado por el gas inicialmente T2= temperatura final del gas V2= volumen ocupado por el gas finalmente k´ = constante de proporcionalidad, depende de la naturaleza del gas. Esto significa que al aumentar la temperatura aumenta el volumen y a menor temperatura menor volumen, donde la temperatura se calcula en grados kelvin ºK. (ºK = ºC + 273) EJEMPLO: 1º- Una muestra de gas de monóxido de carbono ocupa 3.20 L a 125 °C. ¿A qué temperatura en grados Celsius el gas ocupará un volumen de 1.54 L si la presión permanece constante?. DATOS T1= 125ºC + 273 = 398K V1/T1 = V2/T2 T2 × V1 = V2 × T1 T2= V2 T1/V1 V (ml) V α T T (K)
- 2. T2=? V1= 3.20L V2 = 1.54L T2= 1.54L × 398K = 612.92K = 191.54K 3.20L 3.20 K = ºC + 273 ºC = K – 273 ºC= 191.54 – 273 = -81.46ºC 2º- El volumen ocupado por una muestra de CO2 a 35 °C es 5,2 L. A qué temperatura en °C se debe llevar la muestra para que ocupe un volumen de 850 cm3. DATOS T1= 35ºC + 273 = 308K V1 = V2 T2 × V1 = V2 × T1 V1= 5.2L T1 T2 T2=? T2 = V2 × T1 V2= 850cm3 V1 850cm3 × 1ml × 1L = 0.85L 1cm3 1000ml T2= 085L × 3.08K = 50.35K 5.2L K = ºC + 273 ºC= K – 273
- 3. ºC= 50.35 – 273 = -222.65ºC Taller 1- un gas de helio ocupa un volumen de 28ml a 28ºc de temperatura que volumen ocupa el gas a una temperatura de 33ºc. 2- cuando un gas a 28ºk ocupa un volumen de 34L que temperatura ocupa el gas a 23ml. 3- Un globo es inflado con 325L de aire a una temperatura de 20ºc si la temperatura cambia a 23ºk que volumen expande el globo. 4- Si una pipeta de gas es llenada a una temperatura de 18ºk llega a 233ml si esa temperatura aumenta el triple cuál será su volumen inicial.
