Clase 19 aspergilosis y neumocystosis 2015
- 2. AspergilosisAspergilosis Aspergillus fumigatusAspergillus fumigatus Hongo filamentoso, tabicado, hialino
- 3. AspergillosisAspergillosis La aspergilosis es un espectro de enfermedades de los seres humanos y animales causadas por los miembros del género Aspergillus. Estos incluyen (1) Micotoxicosis debido a la ingestion de alimentos contaminados (2) Alergias y secuelas de la presencia de conidios o crecimiento del organismo en los orificios del cuerpo (3) Colonizacion sin extencion en cavidades y tejidos debilidados previamente (4) Enfermedad Invasiva, inflamatoria, granulomatosa y necrotizante del los pulmones y otros organos (5) Enfermedad diseminada sistemica y fatal. El tipo y severidad depende del estado fisiologico del huesped y de la especie de Aspergillus involucrado Distribucion: Mundial. Agentes etiologicos: Aspergillus fumigatus, A. flavus, A. niger, A. nidulans and A. terreus.
- 4. 029029
- 5. 030030
- 6. 031031
- 7. MANIFESTACIONES CLÍNICASMANIFESTACIONES CLÍNICAS Onicomicosis Otomicosis Sinusitis alérgica Aspergilosis broncopulmonar alérgica Aspergilomas Aspergilosis pulmonar invasiva Aspergilosis pulmonar necrosante crónica Sinusitis
- 9. ASPERGILOMAASPERGILOMA Es la forma más común de compromiso pulmonar por Aspergillus y se observa cuando se coloniza una cavidad preexistente en el pulmón, frecuentemente una secuela de tuberculosis. El aspergiloma es una masa de micelios, células inflamatorias, fibrina, restos de tejido, mucus, que conforman una bola fúngica dentro de la cavidad. Generalmente, es asintomático, pero puede causar hemoptisis como manifestación más frecuente. El diagnóstico se hace como hallazgo en un estudio radiológico solicitado por otros motivos o durante el estudio de una hemoptisis .
- 10. Sintomas: Tos Hemoptisis Disnea Fiebre Perdida de peso Fatiga Comunmente asociado : Infeccion oportunista SIDA Cancer patients Similar a : Cancer de pulmon tuberculosis otras infecciones pulmonares
- 11. ASPERGILOSIS BRONCOPULMONAR ALERGICAASPERGILOSIS BRONCOPULMONAR ALERGICA La aspergilosis broncopulmonar alérgica (ABPA) se ve en aproximadamente el 14% de los pacientes asmáticos severos y con menor frecuencia en pacientes con fibrosis quística. Hay evidencia de que sería una reacción de hipersensibilidad a los antígenos de A. fumigatus. Estos pacientes presentan infiltrados pulmonares recurrentes y eosinofilia, junto con elevación de IgE e IgG específicas. Destaca la presencia de bronquiectasias proximales, las que pueden faltar cuando el diagnóstico es precoz .
- 12. ImagenesImagenes Standart de rayos x de tórax o TC Pulmón lesión cavidad o bola fúngica (aspergiloma)
- 13. DIAGNÓSTICO DIRECTODIAGNÓSTICO DIRECTO La visualización de hifas Hifas hialinas septadas (tabicadas) de unos 2 µm de diámetro con ramificaciones dicotómicas en ángulos de 45º La visualización directa se realiza con KOH La visualización debe ser confirmada con el aislamiento en cultivo, ya que las hifas de Aspergillus son indistinguibles de las de Pseudallescheria boydii (Scedosporium apiospermum) o Fusarium spp.
- 14. Examen microscópico directoExamen microscópico directo Hifas hialinas, tabicadas, con división dicotómicasHifas hialinas, tabicadas, con división dicotómicas Examen en fresco - KOHExamen en fresco - KOH
- 15. 40 X
- 16. Hifas hialinas septadasHifas hialinas septadas 2 -8 um de diámetro con paredes paralelas y dicotomizadasdicotomizadas en 45° Giemsa
- 17. Sedimento de lavado broncoalveolar centrifugado coloreado con H-E y PAS
- 22. 033033
- 23. 035035
- 24. 036036
- 25. Medios de cultivoMedios de cultivo Aspergillus crece bien en casi todos los medios de cultivo, tanto para bacterias como para hongos, aunque muchas especies son sensibles a la cicloheximida. La temperatura óptima de crecimiento es de 37º C pudiendo ser visibles los micelios a las 48 horas de incubación. El aislamiento de Aspergillus de una muestra respiratoria debe siempre considerarse la posibilidad de contaminación
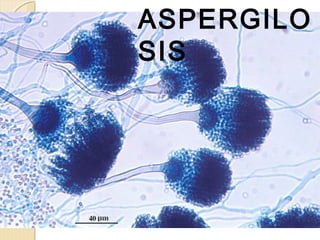
- 26. A. fumigatusA. fumigatus Colonia inicialmente blanca, luego se torna verde azulado a gris con la edad. En los cultivos viejos el color puede ser marrón oscuro a gris amarronado. La textura es aterciopelada, la colonia es chata o plegada. Crece bien a 37ºC e incluso algunas cepas a mayores temperaturas, hasta 65ºC. Cabezas columnares estrictamente uniseriadas, con vesículas piriformes a subclavadas. Las células conidiógenas (fiálides), se ubican en la mitad o tercio superior de la vesícula. Conidióforo de pared lisa y hialina, los conidios son globosos a levemente elipsoidales y finamente rugosos.
- 28. Aspergillus flavusAspergillus flavus Colonia de superficie color amarillo verdoso a verde amarillento, de textura rugosa o vellosa. Puede producir esclerocios inicialmente blancos, con el tiempo toman un color marrón oscuro a negro. El reverso es desde incoloro a marrón rojizo. Muchas cepas crecen mejor a 37ºC que a 28ºC. Cabezas uni y biseriadas, columnares y radiadas, respectivamente. Vesícula subglobosa, conidióforo rugoso, incoloro a marrón pálido. Conidios globosos a elipsoidales, lisos o finamente rugosos.
- 30. A. NigerA. Niger Colonia de superficie negra carbón, granular y chata, al principio es blanca. El reverso es incoloro a blanco. Cabezas estrictamente biseriadas y radiadas. Vesícula esférica cubierta en su totalidad por las métulas. Conidióforo hialino y liso, conidios globosos, de pared rugosa, ornamentados y de color negro a marrón oscuro
- 32. A. terreusA. terreus Las colonias son como la canela y la piel de ante de arena de color marrón con un color amarillo a lo profundo inverso marrón sucio. Cabezas conidios son compacto, columnar (hasta 500 x 30-50 micras de diámetro) y biseriados. Conidióforos son hialinos y paredes lisas. Los conidios son globosos a elipsoidales (1.5 a 2.5 m de diámetro), hialino o ligeramente amarillo y paredes lisas.
- 36. FialidesFialides CONIDIOFOROCONIDIOFORO CONIDIOSCONIDIOS VESICULAVESICULA AspergillusAspergillus
- 37. InmunologiaInmunologia Análisis de sangre ‘Prueba de precipitina aspergillus' Detecta anticuerpos para Aspergillus Detección de anticuerpos: IDD, ELISA, RAI, en suero o plasma . No son útiles en el diagnóstico de API. Detección de antígenos: galactomanano, d- manitol, tanto en el suero como en la orina u otros líquidos corporales Prueba cutánea Aspergillus Ag inyecta en la piel Reacción alérgica indica anticuerpos IgE circulantes específicos para aspergillus . .
- 38. Deteccion de antigeno de AspergillusDeteccion de antigeno de Aspergillus Aspergilosis La detección de galactomanano mediante un ELISA permite el diagnóstico de la aspergilosis invasora. Especificidad del 89,6% y sensibilidad del 87,5%. Esta prueba en algunos estudios se ha demostrado que es positiva antes de que aparezca la sintomatología clínica. Platelia Aspergillus EIA (Bio-Rad) La prueba es un ELISA que detecta galactomanano en suero utilizando el anticuerpo monoclonal EBA-2, que reconoce el galactomanano de A. fumigatus, A. flavus y A. niger. El límite de detección de la prueba es 1 ng/ml de suero
- 39. Deteccion de antigeno de AspergillusDeteccion de antigeno de Aspergillus Actualmente, se considera un resultado positivo cuando el paciente presenta dos muestras consecutivas con un índice ³0,5. La detección de galactomanano puede verse disminuída en pacientes con enfermedad granulomatosa crónica y Síndrome de Job El Platelia Aspergillus EIA no ha sido evaluado en profundidad en plasma, orina, BAL y LCR. La prueba puede dar positiva con hongos del género Penicillium, Alternaria y Paecylomyces. Alimentos como los cereales, pollo, pastas y productos lácteos pueden contener galactomanano que puede ser adsorbido en niños y pacientes con alteraciones en la barrera intestinal. Resultados falsos positivos en pacientes tratados con: piperacilina- tazobactam y amoxicilina-clavulánico
- 40. 048048
- 41. Pneumocystis sp.
- 42. Pneumocystis jiroveci (P. carinii f. sp. hominis) .
- 43. HISTORIA Descubierto por Carlos Chagas en 1909 al observar formas quísticas en pulmón de Cobayos infectados con Trypanosoma cruzi. Chagas lo describió como un estadio quístico de Trypanosoma, redefiniendo el género como Schizotrypanum. En 1910 Antonio Carinii, Biólogo italiano realizó la misma descripción en pulmones de ratas infectadas con T. lewesi . En 1911 Chagas evidenció el microorganismo al realizar una autopsia en un paciente.
- 44. En 1912 Walter E. L., continúo los trabajos de Carinii, encontrando más soportes a la teoría del ezquizonte como parte del ciclo evolutivo de los Trypanosomas. Las formas quísticas de los miembros del género Trypanosoma continuaron mal clasificadas hasta 1912, cuando en Francia los esposos Delanoes concluyeron con su separación. Bautizaron a este nuevo microorganismo como Pneumocyistis carinii en honor a Carinii. En la década de los 30, se encuentra, el primer reporte donde se involucra a P. carinii como productor de infecciones humanas.
- 45. Ammich O. (1930) y Benecke E. (1938), reconocen una única forma de Pneumonía Intersticial de Células Plasmáticas (PICP), sin poder demostrar su etiología. En 1940 dos suecos Van Der Meer y Brug S. demuestran histológicamente la asociación entre P. carinii y la PICP. En 1953 los checos Vanek, Jírovec y Lukes, reportan la etiología de PICP en niños menores de 10 años.
- 46. HISTORIAHISTORIA La Pneumonía por P . carinii (PCP), aparece en proporción epidémica en Europa Central durante y después de lI Guerra Mundial, involucrando niños mal nutridos y prematuros. Mejoran las condiciones de vida y termina la Epidemia al final de los 50. Entre los 1960 y 1964, se reportan casos esporádicos en niños y adultos con inmunodepresión diversa. En los primeros reportes de PCP, P. carinii era considerado intratable. En 1939 se describió el uso efectivo de la Pentamidina como antiprotozoario. Solo hasta 1958, encuentran que es eficaz contra P. carinii. Entre 1958 y 1962 se anunció disminución de la mortalidad por PCP en Europa, del 50% al 3.5%.
- 47. La Pentamidina se convirtió en la droga de elección contra P.carinii. En 1975, Hughes descubre la efectividad de Trimethoprim - Sulfamethoxazole contra P. carinii. Nuevamente, se consideró su uso como medio de profilaxis y tratamiento de PCP . En 1981, Sandra Ford, en el CDC, observó un uso exagerado de la Pentamidina en el tratamiento de PCP por P.carinii. Este hecho fue la pista para las primeras investigaciones del SIDA. Otras drogas han sido utilizadas como efectivas contra PCP : Pentamidina en aerosol Clindamicina – Primaquina Dapsona - Primethamina Atovaquona y Corticosteroides.
- 48. CICLO DE VIDA DEL P. jiroveci TROFOZOITO APLOIDE
- 49. Formas quísticas: redondos o en media luna, de 4-8 micras de diámetro. En su interior se encuentran los esporozoitos (endosporos) (cada quiste puede tener hasta 8). LUZ ALVEOLAR Trofozoitos (formas troficas): – FORMA INFECTANTE formas libres de Pneumocystis,ameboides, pequeñas (2-8mm con 1 núcleo), aparece frecuentemente en acúmulos Reproducción vegetativa por división binaria, varios ciclos Comienzo de ciclo sexuado (etapa prequística precoz, intermedia y tardía): cariogamia, fase diploide y meiosis (formación de 4-8 núcleos). Los prequistes son ovoides, de 3-6 micras, de pared celular gruesa de dos capas en la etapa tardía. EL CICLO SE REALIZA EN EL HOSPEDERO HUMANO O ANIMAL
- 50. Desde el principio de su descubrimiento este microorganismo ha tenido muchos problemas para su clasificación. Se consideró como Protozoario al ser incluido dentro de los Trypanosomas. Fue clasificado como miembro de los Sporozoa , al estudiar su morfología, ultraestructura y respuesta a las drogas terapéuticas. Hasta finales de los años 80 se consideró como protozoo, pero el análisis del ADN demostró en 1988 que es un hongo, y que los Pneumocystis de diferentes mamíferos son muy diferentes entre sí.
- 51. Estos descubrimientos han llevado a un cambio de nomenclatura, el Pneumocystis del ser humano (antes P. carinii f. sp. hominis) pasa a llamarse P. jiroveci (Frenkel 1999) y P. carinii se reserva para lo que antes era P. carinii f. sp. carinii. En 1976, Frenkel ya había señalado las diferencias fenotípicas entre el Pneumocystis del ser humano y otros Pneumocystis, proponiendo el nombre de P. jiroveci. Sin embargo, el nombre no se publicó de forma válida y no tuvo aceptación. El análisis del ADN estableció que el Pneumocystis del ser humano es muy diferente de los de otros animales La reacción en cadena de la polimerasa (PCR) con cebadores que amplifican el ADN de todas las especies conocidas de Pneumocystis reveló que de las muestras procedentes de humanos solo se obtiene ADN de P. jiroveci. Además, tampoco se ha encontrado ADN de P. jiroveci en muestras pulmonares de ningún otro mamífero.
- 52. El sistema trinomial denomina los diferentes tipos de Pneumocystis como formas especiales de P. carinii. Así, P. jiroveci se llamaba P. carinii formae specialis hominis (P. carinii f. sp. hominis). En el año 2001 ya no quedaban dudas de que el microorganismo que causa la neumonía por P. jiroveci en el ser humano debía ser reconocido como una especie distinta. Desde entonces es incorrecto, biológica y taxonómicamente, denominar P. carinii al Pneumocystis procedente del ser humano.
- 54. P. jiroveci es encontrado en los espacios alveolares en pacientes asintomáticos y con infección aguda. Pareciera ser un oportunista patógeno con habilidad de multiplicación por defectos de células T ayudadoras. Su multiplicación produce exudado alveolar espumoso sin células en un principio, luego acompañado de mononucleares. La enfermedad conocida como Pneumonía por Pneumocystis jiroveci (PCP) es una de las entidades que producen enfermedad y muerte en personas con inmunodeficiencia, incluyendo a niños desnutridos. La PCP por largo tiempo ha sido la infección oportunista más común en pacientes con SIDA.
- 55. La introducción de la terapia antiretroviral altamente activa (HAART - highly active antiretroviral therapy), se ha acompañado por una sustancial reducción en la mortalidad y en la incidencia de infecciones oportunistas, incluyendo a la PCP. A pesar de estos avances, el Pneumocystis permanece como el mayor patógeno en personas infectadas por HIV que no reciben o no responden al HAART, y en aquellos que ignoran su condición de infectados por el HIV. También la PCP, presenta importancia clínica en personas inmunocomprometidas por otras razones diferentes al HIV, como los que presentan transplantes de órganos o enfermedades malignas que se encuentran recibiendo quimioterapia. El inicio de la infección podría ser por adherencia de P. jiroveci con los pneumocitos Tipo I.
- 56. MICROSCOPIA ELECTRONICA DELMICROSCOPIA ELECTRONICA DEL P.P. jirovecijiroveci
- 57. Se observa un aumento en la permeabilidad de los alvéolos y capilares con posterior daño del epitelio y de la membrana basal. Por último, aparece hipertrofia e hiperplasia de las células epiteliales alveolares Tipo II.
- 58. DISEMINACION Es poco lo que se conoce sobre los mecanismos de diseminación. Podría ser: Vía aérea: lugares contaminados. Vía hematógena: se ha encontrado en nódulos linfáticos, hígado , bazo, médula ósea, entre otros. En localizaciones extrapulmonares, se han observado lesiones granulomatosas, (infiltrado mononucleares, neutrófilos y necrosis ).
- 59. PATOGENESISPATOGENESIS La Patogénesis de P. jiroveci es multifactorial. La Pentamidina en aerosol es un factor que contribuye a pneumotórax. P.jiroveci puede transmitirse de hombre a hombre por vía respiratoria. Los microorganismos encontrados en los animales son especies diferentes genotípica y fenotípicamente Las diferencias que son observadas entre Pneumocystis, se realizan con métodos Inmunológicos o de Biología Molecular. Morfológicamente son idénticos, sugiriendo diferencias de especies o variedades.
- 60. DIVERSIDAD GENETICA DE P. carinii Pneumocystis carinii sp. f. rattus Rata (variante) Pneumocystis carinii sp. f. carinii Rata (prototipo) Pneumocystis carinii sp. f. mustelae Hurón Pneumocystis carinii sp. f. muris Ratón Pneumocystis carinii sp. f. equi Caballo Pneumocystis carinii sp. f. suis Cerdo Pneumocystis carinii sp. f. oryctolagi Conejo III Worshop sobre Protistas Oportunistas. Cleveland, Ohio. USA.. Junio 1994
- 61. Estudios serológicos revelan una exposición alta en humanos sanos. Anticuerpos contra P. jiroveci aumentan rápidamente con la edad. Se ha encontrado pacientes con títulos altos desde los 4 años . No existen evidencias de transmisión de animal a hombre. Su hábitat podría ser el suelo; de allí su contaminación por el ambiente. Puede permanecer en estado de latencia hasta que aparezcan problemas y/o defectos inmunológicos.
- 62. El hecho de que el 80% de los pacientes con SIDA desarrollen PCP , soporta la idea de exposición general con el microorganismo. P. jiroveci se presenta causando otitis externa y media; esto sugiere una posible colonización que posteriormente podría diseminar y llegar a las vías aéreas superiores. Los macrófagos alveolares y las células T CD4+, juegan un rol importante en la defensa del huésped contra P.jiroveci. Receptores de membrana, (glicoproteina mayor de superficie) , son factores quimiotácticos para los monocitos humanos normales.
- 63. Receptores macrofágicos de manosa, fibronectina y probablemente receptores de Complemento estarían implicados en la adherencia del P. jiroveci con la células huésped y los procesos de fagocitosis. El complemento no es esencial , pero podría ayudar en una mejor fagocitosis mediada por anticuerpos.
- 65. Formas clinicas de neumocistosisFormas clinicas de neumocistosis 1) Asintomática, puede ser tanto infantil como del adulto inmunocompetente y representa la mayor parte de las infecciones 2) Neumocistosis infantil y al finalizar este conflicto, afectó a niños desnutridos y hacinados 3) Formas respiratorias esporádicas en inmunodeficientes, sería la forma más común en la cínica y la observada en los pacientes VIH positivos 4) Neumocistosis extrapulmonar, es poco frecuente y se caracteriza por fiebre, astenia, anorexia, pérdida de peso, hepatoesplenomegalia, intersticiopatía pulmonar y lesiones papulosas o nodulares en la piel
- 66. Puede presentarse generalmente, como una pneumonía aguda difusa. Variedad de presentaciones pulmonares: Lesión solitaria, infiltrado en lóbulos pulmonares, cavernas. De progreso lento , rápido o crónico. Puede no haber manifestaciones pulmonares, con diarreas que subsisten hasta el diagnóstico y tratamiento de PCP. En toda FOD, P. jiroveci debería ser siempre investigado.
- 67. MANIFESTACIONESMANIFESTACIONES EXTRAPULMONARESEXTRAPULMONARES Se presenta: Anemia, adenopatía, hepatoesplenomegalia, lesiones del conducto auditivo externo. Bacterias, hongos, parásitos, virus y otras patologías pueden confundir el diagnóstico. Estudio de la función pulmonar. Medición de gases arteriales en paciente hipoxémico. Rx. de tórax (infiltrado y otras lesiones). Medición de LDH. Ninguno es concluyente de PCP.
- 68. Examenes de laboratorioExamenes de laboratorio Diferentes estudios han mostrado: Valores elevados de lactato deshidrogenada (LDH), sensibilidad 82-100 %. Determinación sérica de 1-3 -D-glucano, es una prueba útil para el diagnóstico de la candidiasis y la aspergilosis invasiva, pero también puede emplearse para la PcP. Existe asociación entre el aumento de los niveles de la proteína C reactiva y la gravedad de la infección, con un peor pronóstico para los paciente con infección VIH y PcP.
- 72. Diagnostico de laboratorioDiagnostico de laboratorio MUESTRAS Lavado bronquial y broncoalveolar: visualización de P. jiroveci Biopsia transbronquial: detección de otros microorganismos, útil en PCP con tratamiento con Pentamidina en aerosol. Esputo inducido: Gran sensibilidad.
- 74. COLORACIONES DETECCION DE QUISTES Grocott - Gomori , Gram - Weigert , Azul de Toluidina, Hematoxilina – Eosina DETECCION DE TROFOZOITOS/ESPOROZOITOS Wright, Giemsa , todas las anteriores. INMUNOFLUORESCENCIA DIRECTA Anticuerpos monoclonales.
- 75. DIAGNOSTICO DIFERENCIAL C. NEOFORMANSP. JIROVECII
- 81. Giemsa Lavado broncoalveolar (BAL) 5-8 µm Formas quísticas Muestras • Esputo inducido baja recuperación (50- 90%) • LBA (Sensibilidad > 90%) • Punción, Biopsia pulmonar. Ex Directo • Fresco • Gram Weigert, Grocott, Giemsa Azul de Toluidina, Blanco de calcofluor
- 82. Coloración de GiemsaColoración de Giemsa
- 83. 4-7 µm Contienen 1 o más núcleos Formas tróficas (pre-quiste)
- 90. Comparación de métodosComparación de métodos 310 muestras310 muestras Tinción Sensibilida d Especificida d Diff-quick (Giemsa mod) 48,4% > 94% Blanco calcoflúor*Blanco calcoflúor* 73,8% > 94% Grocott*Grocott* 76,9% > 94% Inmunofluorescencia MF 90,8% >94% * Valor predictivo positivo y negativo > 90%* Valor predictivo positivo y negativo > 90% Procop GWProcop GW et alet al. J Clin Microbiol 2004, 42: 3333-5. J Clin Microbiol 2004, 42: 3333-5
- 92. Nuevas técnicas de laboratorio. Reacción en cadena de la polimerasa (PCR) y la inmunocitoquímica (ICQ), tienen, mayor sensibilidad y especificidad para detección de patógenos que las coloraciones tradicionales
Editor's Notes
- Text slide.
- Aspergiloma del pulmon encontrado postmorten de un niño con leucemia. Observe la bola fungica ocupando la cavidad
- Aspergiloma encontrado post-mortem en el pulmon de un niño con leucemia.
- Aspergilloma found at post-mortem in the lung of a child with leukaemia.
- Grocott’s methenamine silver (GMS) tejido teñido seccion del pulmon mostrando bola fungica de hifas de Aspergillus fumigatus.
- Grocott’s methenamine silver (GMS) stained tissue sections showing: Aspergillus fumigatus in lung tissue, note las cabezas conidiales formadas en el alveolo.
- 036. Grocott’s methenamine silver (GMS) stained tissue sections showing Aspergillus fumigatus in lung tissue, noete las cabezas conidiales en el alveolo.
- 043.Aspergillus niger on Czapek dox agar. Colonies consist of a compact white or yellow basal felt covered by a dense layer of dark-brown to black conidial heads.
- 048. Immunodiffusion test showing precipitins against Aspergillus.
