Estructura de la materia
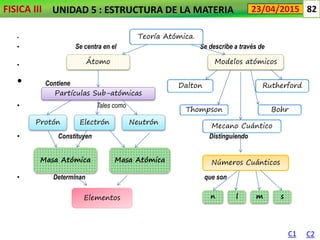
- 1. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 82 • • Se centra en el Se describe a través de • • Contiene que son • Tales como • Constituyen Distinguiendo • Determinan que son Teoría Atómica. Átomo Modelos atómicos Partículas Sub-atómicas Protón Electrón Neutrón Masa Atómica Masa Atómica Elementos Dalton Thompson Mecano Cuántico Rutherford Bohr Números Cuánticos n sml
- 2. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Fueron los filósofos griegos quienes comenzaron a interrogarse racionalmente, tratando de buscar explicaciones o principios que explicaran la naturaleza (physis) de las cosas. Tales de Mileto, postulaba que la sustancia fundamental del universo era el agua, que a partir de ella era posible explicar la constitución de todas las cosas. Empédocles (siglo v a. C.),, sostenía que eran cuatro las sustancias fundamentales: el agua, el aire, el fuego y la tierra, y que de la mezcla de ellas se podían obtener todos los elementos de la naturaleza. TEORIAS ATOMICAS 82 VUSBON
- 3. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015
- 4. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 84
- 5. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 DALTON Las sustancias se pueden dividir hasta partículas indivisibles y separadas llamadas átomos. Dos elementos se pueden combinar entre sí en más de una proporción para dar diferentes compuestos. 84
- 6. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Hipótesis de Avogadro Las últimas partículas de los gases elementales no son átomos sino agregados de átomos (en general dos), a los que dio el nombre de moléculas (del latín pequeñas moles o masas). LEY. En volúmenes iguales de todos los gases, medidos en las mismas condiciones de presión y temperatura, existen igual número de moléculas. G V 85
- 7. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 85
- 8. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Thomson introduce así las ideas : El átomo puede dividirse en las llamadas partículas fundamentales: a) Electrones con carga eléctrica negativa b) Protones con carga eléctrica positiva c) Neutrones, sin carga eléctrica y con una masa mucho mayor que las de los electrones y protones. Thomson considera el átomo como una gran esfera con carga eléctrica positiva, en la cual se distribuyen los electrones como pequeños puntos. 86 MTV V 2
- 9. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 ¿Por qué dedujo Thomson que los rayos catódicos estaban formados por partículas de carga negativa?
- 10. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 El descubrimiento de la radiactividad La radiactividad es la desintegración del núcleo de uno o más átomos. La radiactividad natural se presenta en todos los isótopos de elementos químicos cuyo número atómico es mayor a 83. Los átomos de los elementos radiactivos pueden emitir tres tipos de rayos alfa (α), beta (β) y gamma (γ). Los rayos alfa están constituidos por núcleos de helio, es decir son partículas con dos protones y dos neutrones, por tanto tienen carga positiva. Los rayos beta no son otra cosa que una corriente de electrones, entonces su carga es negativa. Los rayos gamma son energía sin masa, es energía electromagnética como la luz pero con frecuencias altísimas (son los más “energéticos”) 90
- 11. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Descubrimiento del núcleo atómico E. Rutherford realiza en 1911 un experimento con el que se trataba de comprobar la validez del modelo atómico de Thomson. Explicación del experimento de Rutherford: • La mayor parte de las partículas alfa traviesan los átomos sin desviarse (línea verde), la mayor parte del átomo es espacio vacío. • Si la partícula pasa cerca del núcleo (el tamaño del núcleo es 10.000 veces menor que el del átomo) es repelida por éste (línea azul). • Algunas partículas chocan directamente con el núcleo (probabilidad muy baja dada la pequeñez del núcleo), produciéndose un rebote. 90
- 12. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 87 Experimento de Millikan de la gota de aceite
- 13. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Partículas subatómicas Microscopio Atomizador Placa cargada positivamente Placa cargada negativamente Gas Gotita de aceite en suspensión Gotitas de aceite electrizadas Ajustando el voltaje se consigue dejar la gota en suspensión. + + ++ Robert Millikan midió la carga de la gota en suspensión y encontró que, para distintas gotitas, la carga era siempre múltiplo de una carga elemental. La carga del electrón es de 1,602 · 10−19 C. 91
- 14. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Experiencia de la lámina de oro Mineral de uranio Plomo Lámina de oro Película fotográfica Partículas α La mayoría de las partículas alfa atravesaba la lámina de oro sin desviarse. Una de cada 10 000 partículas alfa rebotaba al llegar a la lámina y volvía hacia atrás. Una pequeña proporción de partículas alfa atravesaba la lámina, pero sufrían una leve desviación. 91
- 15. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Modelo atómico de Rutherford El átomo está formado por un núcleo muy pequeño y una corteza. En el núcleo está concentrada toda su carga positiva y casi toda su masa; en la corteza están los electrones girando alrededor del núcleo. Núcleo Electrones Solo una pequeñísima proporción de partículas choca con un núcleo, es repelida y vuelve hacia atrás. Con el modelo de Rutherford queda totalmente explicada la experiencia de la lámina de oro. Partículas alfa que llegan a la lámina de oro y la atraviesan sin desviarse, ya que no encuentran ningún obstáculo. Partículas que pasan cerca de un núcleo y su trayectoria se desvía. 91
- 16. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Según el modelo atómico de Bohr, los electrones de la corteza giran alrededor del núcleo describiendo solo determinadas órbitas circulares. Núcleo Electrones Átomo de sodio (Na) Átomo de fósforo (P) Átomo de oxígeno (O) 91
- 17. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Iones CATIÓN ANIÓN Átomo de litio (Li) Átomo de oxígeno (O) 3 + 3 – Li neutro 8 + 8 – O neutro 3 + 2 – Li+ catión 8 + 10 – O2 – anión 91
- 18. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Cl17 35 Na 23 11 CLORO SODIO Número atómico, Z Número de protones Número de electrones Número de neutrones 17 11 1117 A – Z = 23 – 11 = 12A – Z = 35 – 17 = 18 Número másico, A 91
- 19. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Placa de aluminio Hormigón Radiactividad La pérdida o ganancia de algunas partículas subatómicas es el fenómeno de la radiactividad. Rayos α Rayos β Rayos γ 91
- 20. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Isótopos Se llaman isótopos los átomos que tienen el mismo número de protones y se diferencian en el número de neutrones. Por tanto, presentan el mismo Z y diferente A. Casi todos los elementos químicos presentan isótopos. Habitualmente, todos los isótopos de un elemento reciben el mismo nombre; como excepción, el hidrógeno tiene tres isótopos que poseen un nombre propio. Protio Deuterio Tritio H1 2 H1 1 H1 3 91
- 21. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Fisión y fusión nuclear La rotura del núcleo de ciertos isótopos de algunos elementos químicos para dar otros núcleos más pequeños se denomina fisión nuclear. neutrón núcleo
- 22. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 Fusión nuclear La fusión nuclear es un proceso en el que núcleos de átomos muy pequeños se unen para dar núcleos de átomos mayores. Dos átomos de hidrógeno pueden unir sus núcleos y convertirse en un átomo de helio. Este proceso se realiza continuamente en el Sol
- 23. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015
- 24. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015 En la imagen vemos una caja amarilla que se mueve en el interior de un tren. Dos observadores. Cada observador tiene su propio sistema de coordenadas y su reloj para estudiar el movimiento de la caja. Tratamos con dos sistemas de referencia en movimiento relativo. La Teoría Especial de la Relatividad de Einstein, publicada en 1905, se basó en dos postulados: I. Las leyes de la física son las mismas para todos los marcos de referencia que se mueven con velocidad constante uno con respecto al otro. II. La rapidez de la luz c en el espacio libre es constante para todos los observadores, independiente de sus estados de movimiento. (c = 3 x 108 m/s)
- 25. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015
- 26. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015
- 27. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015
- 28. FISICA III UNIDAD 5 : ESTRUCTURA DE LA MATERIA C1 C2 23/04/2015
